 是一种强氧化剂,紫红色晶体,可溶于水,遇乙醇即被还原。探究小组在实验室中按下图所示流程制取
是一种强氧化剂,紫红色晶体,可溶于水,遇乙醇即被还原。探究小组在实验室中按下图所示流程制取 晶体,并探究
晶体,并探究 的性质。
的性质。已知:
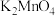 在强碱性溶液中呈绿色,但在弱碱性、中性、酸性溶液中发生歧化反应:
在强碱性溶液中呈绿色,但在弱碱性、中性、酸性溶液中发生歧化反应: 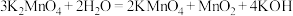 。
。
回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为 制取
制取 的化学方程式为
的化学方程式为(2)将固体研细并加入
 溶液的原因是
溶液的原因是(3)向绿色溶液中通入适量
 时,下列装置中最容易控制
时,下列装置中最容易控制 加入量的是___________(填标号)。
加入量的是___________(填标号)。A. | B. |
C.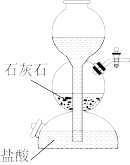 | D. |
 后,用提供的实验用品确认
后,用提供的实验用品确认 是否完全转化,应采取的实验操作是
是否完全转化,应采取的实验操作是(5)探究小组按如图所示过程探究
 的性质。
的性质。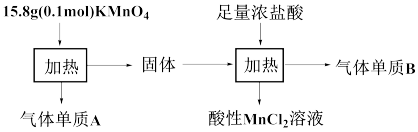
①若
 完全分解,生成的气体A、B在标准状况下的体积之和为
完全分解,生成的气体A、B在标准状况下的体积之和为②加入浓盐酸并加热时消耗溶质
 的物质的量为
的物质的量为
更新时间:2021-12-22 13:11:09
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】铬是不锈钢中一种重要的元素,铬的毒性与其存在的价态有关,低价铬对人体基本无害,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,有关含铬化合物的相互转化关系如图甲。
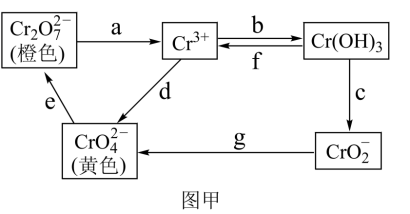
回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是___________ 氢氧化物(填“酸性”、“碱性”或“两性”),相关反应的离子方程式为___________ 。
(2)图甲中所示转化过程中需要加入氧化剂的是___________ (填写表示转化过程的小写字母)。
(3)在水溶液中橙色的 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是___________ 。
(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率( )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
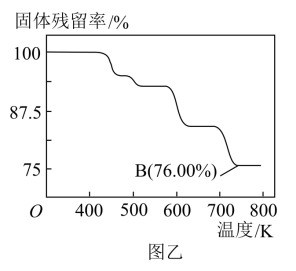
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是___________ 。
②图乙中B点所示固体的化学式是___________ 。

回答下列问题:
(1)从图甲中信息判断,Cr(OH)3是
(2)图甲中所示转化过程中需要加入氧化剂的是
(3)在水溶液中橙色的
 与黄色的
与黄色的 有下列平衡关系:
有下列平衡关系: +H2O
+H2O 2
2 +2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是
+2H+。向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率(
 )随温度的变化如图乙所示。
)随温度的变化如图乙所示。
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是
②图乙中B点所示固体的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】R、W、X、Y、M是原子序数依次增大的五种主族元素。R的最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2。工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度上导致地球表而平均温度升高,Y与X是同一主族的元素,且在元素周期表中与X相邻。
(1)WX2的电子式是_______ 。
(2)R2X、R2Y中,稳定性较高的是_______ (填化学式)。
(3)Se与Y是同一主族元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是_______ (填字母)。
A.Se的最高正化合价为+7 B. H2Se的还原性比H2Y强
C. H2SeO3的酸性比H2YO4强 D. SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为_______ 。
(4)科研人员从矿石中分离出一种氧化物。化学式可表示为M2O3。为确定M元素的种类。进行了一系列实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M2O3在碱性溶液中与Zn充分反应可得到M的简单氢化物。反应完全时,被M2O3氧化的Zn为0.06 mol。
综合以上信息推断,M可能位于元素周期表第_______ 族。
(1)WX2的电子式是
(2)R2X、R2Y中,稳定性较高的是
(3)Se与Y是同一主族元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是
A.Se的最高正化合价为+7 B. H2Se的还原性比H2Y强
C. H2SeO3的酸性比H2YO4强 D. SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为
(4)科研人员从矿石中分离出一种氧化物。化学式可表示为M2O3。为确定M元素的种类。进行了一系列实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M2O3在碱性溶液中与Zn充分反应可得到M的简单氢化物。反应完全时,被M2O3氧化的Zn为0.06 mol。
综合以上信息推断,M可能位于元素周期表第
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如图实验。已知: ;不考虑金、银发生类似反应。
;不考虑金、银发生类似反应。
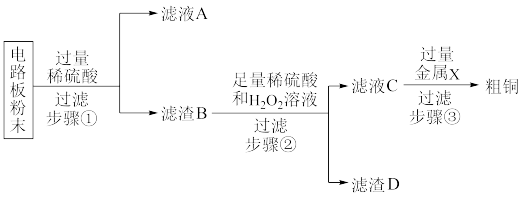
(1)将电路板粉碎成粉末的目的是___________ 。
(2)写出一个步骤①中发生反应的化学方程式___________ 。
(3)滤液 中的阳离子有
中的阳离子有___________ 。
(4)步骤②的目的是_______ 。
(5)要除去粗铜中的杂质,不能选用_______ 。(选填字母序号)
A.氯化铜溶液B.稀盐酸C.蒸馏水
 ;不考虑金、银发生类似反应。
;不考虑金、银发生类似反应。
(1)将电路板粉碎成粉末的目的是
(2)写出一个步骤①中发生反应的化学方程式
(3)滤液
 中的阳离子有
中的阳离子有(4)步骤②的目的是
(5)要除去粗铜中的杂质,不能选用
A.氯化铜溶液B.稀盐酸C.蒸馏水
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】稀土是元素周期表第ⅢB族的元素钪(Sc)、钇(Y)和镧系元素共17种化学元素的合称,是隐形战机、超导、核工业等高精尖领域必备的原料,但是稀土的开采和加工对环境破坏比较大。以富钇稀土矿(主要成分为 ,含有少量的
,含有少量的 、
、 、
、 等杂质)生产氧化钇的工艺流程如图,回答下列问题:
等杂质)生产氧化钇的工艺流程如图,回答下列问题:_____ 。
(2)在粉碎机中研磨粉碎的目的是_____ 。
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是_____ ,“酸溶”过程中, 发生反应的离子方程式为
发生反应的离子方程式为_____ 。
(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液Ⅰ中杂质,沉淀Ⅱ的主要成分是_____ (填化学式)。
(5)流程中“沉钇”发生反应的离子方程式为_____ 。
(6)流程中可循环使用的物质为_____ (填名称)。
 ,含有少量的
,含有少量的 、
、 、
、 等杂质)生产氧化钇的工艺流程如图,回答下列问题:
等杂质)生产氧化钇的工艺流程如图,回答下列问题:
(2)在粉碎机中研磨粉碎的目的是
(3)流程中操作Ⅰ、Ⅱ、Ⅲ的名称是
 发生反应的离子方程式为
发生反应的离子方程式为(4)向反应釜2中通入气体X使溶液呈碱性,调节溶液的pH除去滤液Ⅰ中杂质,沉淀Ⅱ的主要成分是
(5)流程中“沉钇”发生反应的离子方程式为
(6)流程中可循环使用的物质为
您最近一年使用:0次
【推荐2】以明矾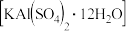 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
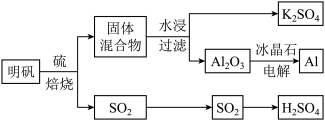
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式
写出明矾和硫单质混合焙烧发生反应的化学方程式______ .
 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、______ 、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______ .
 电解
电解 时加入冰晶石的作用是
时加入冰晶石的作用是______ .
 以Al和
以Al和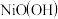 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时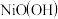 转化为
转化为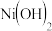 ,该电池反应的化学方程式是
,该电池反应的化学方程式是______ .
 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时:
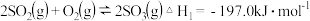

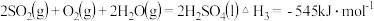
则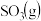 和
和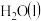 反应的热化学方程式是
反应的热化学方程式是______ .
 焙烧948吨明矾
焙烧948吨明矾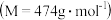 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为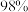 的硫酸?
的硫酸?
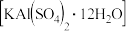 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式
写出明矾和硫单质混合焙烧发生反应的化学方程式 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、 电解
电解 时加入冰晶石的作用是
时加入冰晶石的作用是 以Al和
以Al和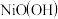 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时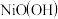 转化为
转化为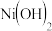 ,该电池反应的化学方程式是
,该电池反应的化学方程式是 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时: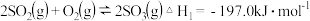

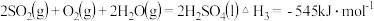
则
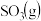 和
和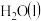 反应的热化学方程式是
反应的热化学方程式是 焙烧948吨明矾
焙烧948吨明矾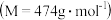 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为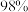 的硫酸?
的硫酸?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】我国是世界上稀土资源最丰富的国家,钇(Y)作为稀土元素之一,在激光材料和超导材料方面有着重要的应用。工业上通过钇矿石(主要成分为Y2FeBe2Si2O10)制取氧化钇和铍的工艺流程如下图所示:

已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的PH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
(1)Y2FeBe2Si2O10可用氧化物的形式表示为_______ 。
(2)已知将钇矿石与NaOH(s)在高温下共熔,生成的固体产物有Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2,试写出相关的化学反应方程式并配平_______ 。
(3)若向滤液Ⅱ中加入过量的氢氧化钠溶液发生的离子反应有_______ 。
(4)根据表中数据计算常温下Ksp[Y(OH)3]=_______ 。
(5)实验室洗涤过滤所得Y(OH)3沉淀的操作是_______ 。
(6)某同学设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为_______ 。

已知:①钇(Y)的常见化合价为+3;
②铍(Be)与铝化学性质相似;
③25℃时,相关金属离子形成氢氧化物沉淀的PH范围如下表:
(假设表中金属离子初始浓度co(Mn+)=0.01mol/L,当溶液中某种离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
离子 | 开始沉淀时的PH | 完全沉淀时的PH |
Fe3+ | 2.1 | 3.1 |
Y3+ | 6.5 | 7.5 |
(1)Y2FeBe2Si2O10可用氧化物的形式表示为
(2)已知将钇矿石与NaOH(s)在高温下共熔,生成的固体产物有Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2,试写出相关的化学反应方程式并配平
(3)若向滤液Ⅱ中加入过量的氢氧化钠溶液发生的离子反应有
(4)根据表中数据计算常温下Ksp[Y(OH)3]=
(5)实验室洗涤过滤所得Y(OH)3沉淀的操作是
(6)某同学设计用石墨棒和铜棒作两极,通过电解NaCl-BeCl2混合熔融盐来制备Be同时得到副产物Cl2,则铜棒上发生的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组在用CO还原Fe3O4的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引;已知:加热条件下Fe3O4能溶于浓盐酸。为探究X的成分(无Fe2O3),他们进行了如下实验。
I.定性检验
(1)实验②的目的是确认Fe3+是否存在,则实验②的“……”操作是___________ 。
(2)由上述实验现象推断,黑色粉末X的成分是___________ (填化学式);根据产物成分,CO还原Fe2O3发生反应的化学方程式为___________ 。
II.定量测定

(3)操作Z是___________ 、___________ 。下列仪器中,在灼烧沉淀时必须用到的是(填名称)___________ 。

(4)写出溶液Y中滴加足量H2O2溶液时发生反应的离子方程式___________ 。
(5)通过以上数据,得出2.376g黑色粉末X中各成分的物质的量之比为___________ 。
I.定性检验
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,注入浓盐酸,微热 | 黑色粉末逐渐溶解,溶液呈黄绿色;有少量气泡产生 |
| ② | …… | 溶液出现血红色 |
| ③ | 另取少量黑色粉末X放入试管2中,注入足量硫酸铜溶液,振荡,静置 | 有极少量红色物质析出,仍有较多黑色固体未溶解 |
(1)实验②的目的是确认Fe3+是否存在,则实验②的“……”操作是
(2)由上述实验现象推断,黑色粉末X的成分是
II.定量测定

(3)操作Z是

(4)写出溶液Y中滴加足量H2O2溶液时发生反应的离子方程式
(5)通过以上数据,得出2.376g黑色粉末X中各成分的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组用下列装置,模拟呼吸面具中的有关反应原理测定样品中Na2O2的纯度。

(1)装置A中盛放稀盐酸的仪器名称___________ ,a的作用是___________ ,装置A中发生的离子反应方程式 ___________ 。
(2)装置C中发生反应的化学方程式为___________ 。
(3)上述装置存在一处缺陷,会导致测定Na2O2的纯度偏高,改进的方法是___________ 。
(4)实验装置改进后,向C中加入10.0g样品进行实验,实验结束后共收集到标准状况下336mL气体,则样品中Na2O2的纯度___________ 。

(1)装置A中盛放稀盐酸的仪器名称
(2)装置C中发生反应的化学方程式为
(3)上述装置存在一处缺陷,会导致测定Na2O2的纯度偏高,改进的方法是
(4)实验装置改进后,向C中加入10.0g样品进行实验,实验结束后共收集到标准状况下336mL气体,则样品中Na2O2的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】绿矾(FeSO4•xH2O)是生血片的主要成分,某研究性学习小组拟对绿矾热分解产物进行探究。
【实验猜想】绿矾分解可能生成Fe、FeO、Fe2O3、SO2、SO3或H2O等。
【实验探究】该小组用如图所示装置进行实验(夹持仪器略)。

已知:
a.SO3沸点:44.8℃。
b.BaSO3是难溶于水的白色固体。
(1)为保证实验结果的准确性,点燃酒精灯之前的关键操作:____ (注:气密性已检验完)。
(2)【实验现象】
A中固体变红色,B中无水CuSO4____ (说实验现象,下同),C中蓝色石蕊试纸___ ,D中产生白色沉淀。
(3)反应结束后,取A中固体继续进行实验,实验的操作及现象如下:
①向固体样品中加入过量稀硫酸,固体完全溶解,且无气体放出;
②取①中溶液滴入少量高锰酸钾溶液,无明显现象;
③另取①中溶液,并向其中滴入KSCN溶液,溶液变红。
由此得出结论:红色固体为___ (写化学式),该物质的常见用途___ 。
(4)该实验中,加热5.56gFeSO4•xH2O,充分反应后A中得到红色固体1.60g,经过计算,x=___ 。
(5)D中白色沉淀的成分:____ (写化学式)。
(6)根据实验结果,写出FeSO4•xH2O热分解的化学方程式____ 。
【实验猜想】绿矾分解可能生成Fe、FeO、Fe2O3、SO2、SO3或H2O等。
【实验探究】该小组用如图所示装置进行实验(夹持仪器略)。

已知:
a.SO3沸点:44.8℃。
b.BaSO3是难溶于水的白色固体。
(1)为保证实验结果的准确性,点燃酒精灯之前的关键操作:
(2)【实验现象】
A中固体变红色,B中无水CuSO4
(3)反应结束后,取A中固体继续进行实验,实验的操作及现象如下:
①向固体样品中加入过量稀硫酸,固体完全溶解,且无气体放出;
②取①中溶液滴入少量高锰酸钾溶液,无明显现象;
③另取①中溶液,并向其中滴入KSCN溶液,溶液变红。
由此得出结论:红色固体为
(4)该实验中,加热5.56gFeSO4•xH2O,充分反应后A中得到红色固体1.60g,经过计算,x=
(5)D中白色沉淀的成分:
(6)根据实验结果,写出FeSO4•xH2O热分解的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】浓硫酸和木炭在加热时发生化学反应。用如图所示各装置设计一个实验,验证浓硫酸与木炭在加热条件下反应产生的各种产物。

(1)写出浓硫酸和木炭在加热时反应的化学方程式:___________ 。
(2)这些装置的连接顺序(按产物气流从左到右的方向)是④___________ (填装置的序号)。
(3)图①中装置C的作用___________ 。
(4)下列关了该实验的说法中不正确的是___________ (多选)。
A.该反应体现了浓硫酸的强氧化性和酸性
B.浓硫酸应该放在图④的分液漏斗中,以便控制反应
C.反应一段时间后,可以用氯化钡溶液检验,装置④中是否有硫酸剩余
D.含0.04 mol溶质的浓硫酸与足量木炭反应,可生成标准状况下气体1344 mL

(1)写出浓硫酸和木炭在加热时反应的化学方程式:
(2)这些装置的连接顺序(按产物气流从左到右的方向)是④
(3)图①中装置C的作用
(4)下列关了该实验的说法中不正确的是
A.该反应体现了浓硫酸的强氧化性和酸性
B.浓硫酸应该放在图④的分液漏斗中,以便控制反应
C.反应一段时间后,可以用氯化钡溶液检验,装置④中是否有硫酸剩余
D.含0.04 mol溶质的浓硫酸与足量木炭反应,可生成标准状况下气体1344 mL
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某研究性学习小组探究碳化铝的性质:发现碳化铝与水在常温下剧烈反应,生成大量气体和白色沉淀,该沉淀既能溶于盐酸也能溶于NaOH溶液,该小组同学为了探究气体产物的组成,设计出如下实验:

(1)利用碳化铝制取气体,下列装置中适合作为气体发生装置的是____ 。
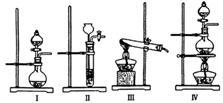
(2)正确选择发生装置后,连接装置进行实验。一段时间后,硬质玻璃管C中黑色粉末变成红色,干燥管D中白色粉末变成蓝色,装置E中澄清石灰水变浑浊,尾气燃烧产生蓝色火焰。
①干燥管D中的试剂可能是__________ ,其作用是___________ 。
②根据实验现象,某同学得出下列推论,其中正确的是_________ 。
a.气体与氧化铜在一定条件下反应,氧化产物只有二氧化碳
b.气体与氧化铜在一定条件下反应,产物一定有水和二氧化碳,可能有一氧化碳
c.气体与氧化铜在一定条件下反应,产物一定有水、二氧化碳和一氧化碳
d.气体具有还原性,氧化产物可能有多种
(3)实验完毕后,要先后熄灭C和F处的酒精灯,应先熄灭的是_____ 处酒精灯,理由是_____________________________ 。(只写出一条即可)
(4)若最后在F处点燃气体与在A处产生的气体相同,实验前系统内的空气已排尽,实验验结束后,C装置减轻12.8 g,D装置增重7.2 g,E装置增重8.8 g(假定D、E吸收气体是完全的),则A、C处发生反应的方程式分别为_____________ 、( ) (5)如图所示,U型透明玻璃管的左端封闭有A处产生气体和氯气的混合气,将该装置放在日光灯下。一段时间后(不考虑水与氯气的反应),下列关于U形管中可能出现的现象的叙述中正确的是( )

a.U形管左侧会有油状液滴出现
b.溶液很快变成蓝色
c.气柱缩小,右端液柱下降
d.气柱膨胀,右端玻璃管中液体溢出

(1)利用碳化铝制取气体,下列装置中适合作为气体发生装置的是

(2)正确选择发生装置后,连接装置进行实验。一段时间后,硬质玻璃管C中黑色粉末变成红色,干燥管D中白色粉末变成蓝色,装置E中澄清石灰水变浑浊,尾气燃烧产生蓝色火焰。
①干燥管D中的试剂可能是
②根据实验现象,某同学得出下列推论,其中正确的是
a.气体与氧化铜在一定条件下反应,氧化产物只有二氧化碳
b.气体与氧化铜在一定条件下反应,产物一定有水和二氧化碳,可能有一氧化碳
c.气体与氧化铜在一定条件下反应,产物一定有水、二氧化碳和一氧化碳
d.气体具有还原性,氧化产物可能有多种
(3)实验完毕后,要先后熄灭C和F处的酒精灯,应先熄灭的是
(4)若最后在F处点燃气体与在A处产生的气体相同,实验前系统内的空气已排尽,实验验结束后,C装置减轻12.8 g,D装置增重7.2 g,E装置增重8.8 g(假定D、E吸收气体是完全的),则A、C处发生反应的方程式分别为

a.U形管左侧会有油状液滴出现
b.溶液很快变成蓝色
c.气柱缩小,右端液柱下降
d.气柱膨胀,右端玻璃管中液体溢出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.乙酸乙酯应用广泛,中学化学实验常用下图装置来制备。回答下列问题:

(1)制备乙酸乙酯的化学方程式为___________ 。
(2)实验时,加入浓硫酸做催化剂和吸水剂,但实际上浓硫酸用量又不能过多,原因是___________ 。
(3)若用此装置制备乙酸乙酯,其缺点有___________ 、___________ 。
Ⅱ.某兴趣小组对乙酸乙酯在NaOH溶液条件下的催化水解进行探究。
已知:①乙酸乙酯的沸点约77℃;②酸和碱均可用作该反应的催化剂。
实验步骤:向试管中加入8molNaOH溶液,再加入2mL乙酸乙酯,量出乙酸乙酯的高度。再把试管放入70℃的水浴中,每隔1min将其取出,振荡,静置,立即测量并记录剩余酯层的高度,再迅速放回水浴中继续加热,如此反复进行。改变NaOH溶液的浓度,重复实验。数据记录:
回答下列问题:
(4)分析上述数据,得到乙酸乙酯水解速率的结论是:
①NaOH溶液浓度越大,水解速率越___________ ;
②___________ 。
(5)结论②的理论解释是___________ 。
(6)该实验必须严格控制NaOH溶液的体积、乙酸乙酯的用量和反应的温度。为了达到实验的目的,有同学建议用___________ 代替NaOH溶液重复试验,对数据进行修正。

(1)制备乙酸乙酯的化学方程式为
(2)实验时,加入浓硫酸做催化剂和吸水剂,但实际上浓硫酸用量又不能过多,原因是
(3)若用此装置制备乙酸乙酯,其缺点有
Ⅱ.某兴趣小组对乙酸乙酯在NaOH溶液条件下的催化水解进行探究。
已知:①乙酸乙酯的沸点约77℃;②酸和碱均可用作该反应的催化剂。
实验步骤:向试管中加入8molNaOH溶液,再加入2mL乙酸乙酯,量出乙酸乙酯的高度。再把试管放入70℃的水浴中,每隔1min将其取出,振荡,静置,立即测量并记录剩余酯层的高度,再迅速放回水浴中继续加热,如此反复进行。改变NaOH溶液的浓度,重复实验。数据记录:
| 组别 | c(NaOH)/mol/L 酯层高度/mm | 时间/min | ||||||||
| 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | ||
| 1 | 0.5 | 10.0 | 9.0 | 8.0 | 7.5 | 7.0 | 6.5 | 6.5 | 6.5 | 6.5 |
| 2 | 1.0 | 10.0 | 8.5 | 7.0 | 6.0 | 5.0 | 4.5 | 4.5 | 4.5 | 4.5 |
| 3 | 2.0 | 10.0 | 8.0 | 6.0 | 4.5 | 3.0 | 2.0 | 1.5 | 1.5 | 1.5 |
(4)分析上述数据,得到乙酸乙酯水解速率的结论是:
①NaOH溶液浓度越大,水解速率越
②
(5)结论②的理论解释是
(6)该实验必须严格控制NaOH溶液的体积、乙酸乙酯的用量和反应的温度。为了达到实验的目的,有同学建议用
您最近一年使用:0次



