回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______ 形象化描述。在基态14C原子中,核外存在_______ 对自旋相反的电子。
(2)N的基态原子核外电子排布式为_______ ;Cu的基态原子最外层有_______ 个电子。
(3)钒(23V)是元素广泛用于催化及钢铁工业。钒在元素周期表中的位置为_______ ,其价层电子的轨道表示式为_______ 。
(4)Na位于元素周期表第_______ 周期第_______ 族;S的基态原子核外有_______ 个未成对电子;Si的基态原子核外电子排布式为_______ 。
(5)Cu+基态核外电子排布式为_______ 。
(6)基态Fe原子有_______ 个未成对电子,Fe3+的电子排布式为_______ 。
(7)31Ga基态原子的核外电子排布式是_______ 。
(8)铝原子核外电子云有_______ 种不同的伸展方向,有_______ 种不同运动状态的电子。
(9)基态Mn2+的核外电子排布式为_______ 。
(10)Se原子序数为_______ ,其核外M层电子的排布式为_______ 。
(11)可正确表示原子轨道的是_______。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)N的基态原子核外电子排布式为
(3)钒(23V)是元素广泛用于催化及钢铁工业。钒在元素周期表中的位置为
(4)Na位于元素周期表第
(5)Cu+基态核外电子排布式为
(6)基态Fe原子有
(7)31Ga基态原子的核外电子排布式是
(8)铝原子核外电子云有
(9)基态Mn2+的核外电子排布式为
(10)Se原子序数为
(11)可正确表示原子轨道的是_______。
| A.2s | B.2d | C.3pz | D.3f |
21-22高二·全国·课时练习 查看更多[2]
(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.1.3 电子云与原子轨道 泡利原理与洪特规则 能量最低原理-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)
更新时间:2021-12-26 22:42:16
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求填空:
(1)基态Si原子中,电子占据的能量最高的电子层符号为_______ ,该电子层具有的原子轨道数为_______ ,具有的电子数为_______
(2)基态N原子中,核外电子占据_______ 个电子层,_______ 个原子轨道,共有_______ 种运动状态;电子占据的能量最高的原子轨道的形状为_______ 。
(1)基态Si原子中,电子占据的能量最高的电子层符号为
(2)基态N原子中,核外电子占据
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式_______ ;
(2)基态Cr原子的核外电子排布式为_______ ;
(3)稳定性:
_______  (填“>”或“<”);
(填“>”或“<”);
(4)基态S原子电子占据最高能级的电子云轮廓图为_______ 形;
(5)镍元素基态原子3d能级上的未成对电子数为_______ 。
(1)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,该原子价层电子的轨道表示式
(2)基态Cr原子的核外电子排布式为
(3)稳定性:

 (填“>”或“<”);
(填“>”或“<”);(4)基态S原子电子占据最高能级的电子云轮廓图为
(5)镍元素基态原子3d能级上的未成对电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:_______________________________ ,核外电子运动状态有_______ 种。
(2)B是原子序数为35的元素,其原子中有___________ 个电子层,有_________ 个能级。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为_________________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应方程式:____________ 。
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:
(2)B是原子序数为35的元素,其原子中有
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)s电子的原子轨道呈___________ 形,每个s能级有___________ 个原子轨道;p电子的原子轨道呈___________ 形,每个p能级有___________ 个原子轨道。
(2) 基态铝原子核外共有___________ 种不同能级的电子,有___________ 种不同运动状态的电子。
(2) 基态铝原子核外共有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是_______ 。
a.最易失去的电子能量最高
b.同一个电子层上的不同能级上的原子轨道,能量大小不同
c.p轨道电子能量一定高于s轨道电子能量
d.在离核最近区域内运动的电子能量最低
(2)比较下列多电子原子的原子轨道的能量高低。
①1s,3d:_______ ;②3s,3p,3d:_______ ;③2p,3p,4p:_______ ;④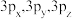 :
:_______ 。
(3)基态铝原子核外电子云有_______ 种不同的伸展方向,共有_______ 种不同能级的电子,有_______ 种不同运动状态的电子。
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是
a.最易失去的电子能量最高
b.同一个电子层上的不同能级上的原子轨道,能量大小不同
c.p轨道电子能量一定高于s轨道电子能量
d.在离核最近区域内运动的电子能量最低
(2)比较下列多电子原子的原子轨道的能量高低。
①1s,3d:
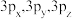 :
:(3)基态铝原子核外电子云有
您最近一年使用:0次
【推荐3】根据有关知识,回答下列问题。
(1)符号 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。
(2)铝原子核外电子云有__________ 种不同的伸展方向,有__________ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是__________ (填元素符号,下同),电负性最大的元素是__________ 。
(4)Be的第一电离能大于B的第一电离能,这是因为__________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:__________ 。
(6)锰元素位于第四周期第ⅦB族,请写出基础 的价层电子排布式
的价层电子排布式__________ 。
(1)符号
 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C. 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)锰元素位于第四周期第ⅦB族,请写出基础
 的价层电子排布式
的价层电子排布式
您最近一年使用:0次
【推荐1】完成下列填空
(1)写出下列基态原子的核外电子排布式。
Li:___________ ;N:___________ ;Ti:___________ ;Cu___________ 。
(2)钒元素在元素周期表中的位置是___________ 。
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是___________ 。
(1)写出下列基态原子的核外电子排布式。
Li:
(2)钒元素在元素周期表中的位置是
(3)X元素位于第三周期,同周期元素中其第一电离能最小,X的元素符号是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】阅读教材P17页内容,总结归纳元素的化合价与核外电子排布的关系。
①除Ⅷ族、ⅠB族的某些元素和0族元素外,元素的最高化合价_____ 它所在族的序数。
②一般来说,非金属元素的最高正化合价和它的最低负化合价的绝对值之和等于_____ (F无正价)。
③稀有气体元素的化合价在通常情况下为_____ 。
④过渡元素的价电子较多且所在轨道的能量相差不大,因此过渡元素具有_____ 价态。
①除Ⅷ族、ⅠB族的某些元素和0族元素外,元素的最高化合价
②一般来说,非金属元素的最高正化合价和它的最低负化合价的绝对值之和等于
③稀有气体元素的化合价在通常情况下为
④过渡元素的价电子较多且所在轨道的能量相差不大,因此过渡元素具有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】以Cu2O、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态O原子的电子排布式_______ ,其中未成对电子有_______ 个。
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______ 。
(1)基态O原子的电子排布式
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是
您最近一年使用:0次
【推荐2】元素铜与镍的第二电离能分别为:ICu=1959kJ•mol﹣1,INi=1753kJ•mol﹣1,ICu>INi的原因是______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】TiO2是一种性能优良的半导体光催化剂,能有效地吸附有机污染物(如甲醛、甲苯等)和含氮化合物(如NH3、CN-等),并能将它们转化为CO2和N2等小分子物质。
(1)基态Ti原子的价电子排布式为____ ,其中最外层电子所占能级的原子轨道呈____ 形。与钛元素同周期且未成对电子数相同的元素有____ (填元素名称)。
(2)甲苯中C原子的杂化类型为____ ,所有原子___ (填“在”或“不在”)同一平面内。
(3)已知CO2在水中溶解度较小,其原因为____ 。
(4)含CN-的污水毒性极大,用NaClO将CN-氧化为无污染的气体时有一中间产物CNO-。CN-中σ键和π键的个数比为____ 。
(5)纳米级TiO2可以用TiCl4来制备,制备时TiCl4加入大量的水中,同时加热促进水解趋于完全。写出该反应的化学方程式:____ 。
(6)二氧化钛纳米材料是一种高效催化剂,可催化如图反应:


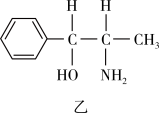
化合物乙中各元素的电负性由小到大的顺序为____ 。
(1)基态Ti原子的价电子排布式为
(2)甲苯中C原子的杂化类型为
(3)已知CO2在水中溶解度较小,其原因为
(4)含CN-的污水毒性极大,用NaClO将CN-氧化为无污染的气体时有一中间产物CNO-。CN-中σ键和π键的个数比为
(5)纳米级TiO2可以用TiCl4来制备,制备时TiCl4加入大量的水中,同时加热促进水解趋于完全。写出该反应的化学方程式:
(6)二氧化钛纳米材料是一种高效催化剂,可催化如图反应:



化合物乙中各元素的电负性由小到大的顺序为
您最近一年使用:0次



