室温下,用0.5mol·L-1Na2CO3溶液浸泡CaSO4粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。已知Ksp(CaSO4)=5×10-5,Ksp(CaCO3)=3×10-9。下列说法正确的是
A.0.5mol·L-1Na2CO3溶液中存在:c(OH-)=c(H+)+c(HCO )+c(H2CO3) )+c(H2CO3) |
B.反应CaSO4+CO  CaCO3+SO CaCO3+SO 正向进行,需满足 正向进行,需满足 > >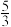 ×104 ×104 |
C.过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤ 且c(Ca2+)≤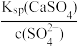 |
| D.滤渣中加入醋酸发生反应的离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O |
2021·江苏·高考真题 查看更多[10]
(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题(已下线)第26讲 难溶电解质的溶解平衡(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题6 Ksp专练(已下线)押江苏卷第13题 水溶液中的离子平衡 -备战2022年高考化学临考题号押题(江苏卷)(已下线)必刷卷05-2022年高考化学考前信息必刷卷(江苏专用)江苏省丹阳高级中学2021-2022学年高二上学期期末考试化学试题2021年新高考江苏化学高考真题
更新时间:2022-01-04 12:01:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式书写正确的是
A.将少量 加入氢氧化钠溶液中: 加入氢氧化钠溶液中: |
B.将少量Ag加入稀硫酸中: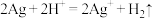 |
C.将少量 通入 通入 溶液中: 溶液中: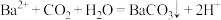 |
D.将少量 加入稀盐酸中: 加入稀盐酸中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】解释下列事实的方程式正确的是
| A.向NaClO溶液中通入少量SO2: 2ClO-+SO2十H2O= SO32- +2HClO |
| B.用醋酸溶液除水垢中的CaCO3: CaCO3+2H+=Ca2++H2O+CO2↑ |
C.向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2 2CO2+2CaSO4 2CO2+2CaSO4 |
| D.碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:CO32-+Ca2+=CaCO3↓ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知某温度下,MnCO3、MnS的溶度积分别为2.0×10-11mol2·L-2、5.0×10-14mol2·L-2。下列推断不正确的是
| A.碳酸锰的溶解度大于硫化锰的溶解度 |
B.碳酸锰转化成硫化锰的离子方程式为 |
| C.碳酸锰转化成硫化锰的平衡常数K=2.5×10-3 |
D.在含相同浓度的 、S2-的溶液中滴加氯化锰溶液,先产生沉淀MnS 、S2-的溶液中滴加氯化锰溶液,先产生沉淀MnS |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】有关 的沉淀溶解平衡,下列说法中错误的是
的沉淀溶解平衡,下列说法中错误的是
 的沉淀溶解平衡,下列说法中错误的是
的沉淀溶解平衡,下列说法中错误的是A. 饱和溶液中 饱和溶液中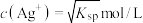 |
B.用 溶液代替蒸馏水洗涤 溶液代替蒸馏水洗涤 沉淀,可以减少沉淀的损失 沉淀,可以减少沉淀的损失 |
C.向 悬浊液中加少量水, 悬浊液中加少量水, 一定减小 一定减小 |
D.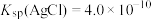 , , ,说明溶解度: ,说明溶解度: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列有关说法中正确的是
A.某温度时的混合溶液中c(H+)=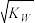 mol·L-1,说明该溶液呈中性(Kw为该温度时水的离子积常数) mol·L-1,说明该溶液呈中性(Kw为该温度时水的离子积常数) |
| B.由水电离出的c(H+)=10-12mol·L-1的溶液中:Na+、Ba2+、HCO3-、Cl-可以大量共存 |
| C.已知Ksp(AgCl)=1.56×10-10, Ksp(Ag2CrO4)=9.0×10-12。向含有Cl-、CrO42-且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,CrO42-先产生沉淀 |
| D.常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下进行下列实验,根据实验操作和现象所得到的结论错误的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中滴加Ba(NO3)2溶液和盐酸,产生白色沉淀 | 不能确定原溶液一定含有 |
| B | 向盛有等物质的量浓度的NaI和NaCl的混合溶液中滴加AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 蔗糖与浓硫酸反应所得刺激性气体使溴水和品红溶液颜色变为无色 | SO2具有还原性和漂白性 |
| D | 用pH计测得浓度均为0.01mol/L的NaX溶液和Na2CO3溶液的pH依次为10.9、11.1 | HX的酸性比碳酸酸性强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】下列设计的实验方案不能达到实验目的的是
| 选项 | 实验现象和操作 | 实验目的 |
| A | 向2mL0.1mol·L-1Na2S溶液中滴加0.1mol·L-1ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1mol·L-1CuSO4溶液,出现黑色沉淀 | 验证Ksp(ZnS)>Ksp(CuS) |
| B | 向含有0.1mol的FeI2溶液中通入0.1molCl2,再加入淀粉溶液,溶液变蓝色 | 还原性:I->Fe2+ |
| C | 以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极保护法 |
| D | 向盛有2mL0.1mol·L-1K2Cr2O7溶液的试管中滴加5~10滴NaOH溶液,再继续滴加5~10滴6mol·L-1H2SO4溶液,观察现象 | 探究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



