已知某温度下,MnCO3、MnS的溶度积分别为2.0×10-11mol2·L-2、5.0×10-14mol2·L-2。下列推断不正确的是
| A.碳酸锰的溶解度大于硫化锰的溶解度 |
B.碳酸锰转化成硫化锰的离子方程式为 |
| C.碳酸锰转化成硫化锰的平衡常数K=2.5×10-3 |
D.在含相同浓度的 、S2-的溶液中滴加氯化锰溶液,先产生沉淀MnS 、S2-的溶液中滴加氯化锰溶液,先产生沉淀MnS |
17-18高二上·黑龙江哈尔滨·期末 查看更多[7]
黑龙江省哈尔滨市第六中学2017-2018学年高二上学期期末考试化学试题河南省西华县第一高级中学2017-2018学年高二上学期期末选拔考试化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时1 沉淀溶解平衡及其应用高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第三章 水溶液中的离子平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)云南省普洱市西盟佤族自治县第一中学2021-2022学年高二上学期12月月考化学试题
更新时间:2020-09-13 17:31:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】根据下列图示所得出的结论不正确的是


| A.由图甲可知,除去CuSO4溶液中的Fe3+可加入适量CuO调节pH至4左右 |
B.图乙是一定温度下三种碳酸盐的沉淀溶解平衡曲线,a点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO ) ) |
C.图丙是室温下AgCl和AgI的饱和溶液中离子浓度的关系曲线,该温度下反应AgCl(s)+I-(aq) AgI(s)+Cl-(aq)的平衡常数K=2.5×106 AgI(s)+Cl-(aq)的平衡常数K=2.5×106 |
| D.图丁是室温下AgCl和Ag2CrO4的沉淀溶解平衡曲线,阴影区域中的点可以同时生成Ag2CrO4沉淀和AgCl沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验目的对应的方案设计、现象和结论都正确的是
选项 | 实验目的 | 方案设计 | 现象和结论 |
A | 比较 | 向 | 白色沉淀转化为红褐色沉淀,证明 |
B | 探究压强对平衡移动的影响 | 密闭容器中盛 | 气体颜色加深,说明平衡向生成 |
C | 比较 | 向等体积饱和 | 得到沉淀 |
D | 比较 | 用 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列由实验现象得出的结论正确的是( )
| 操作及现象 | 结论 | |
| A | 室温下,向1 mL 0.1mol/L AgNO3溶液中加入几滴0.01mol/L NaCl溶液出现白色沉淀,再滴加几滴0.1mol/L NaI溶液,出现黄色沉淀。 | Ksp(AgI)< Ksp(AgCl) |
| B | 在醋酸钠溶液中滴入酚酞试液,加热后红色加深 | 盐类水解是吸热反应 |
| C | 向某溶液中滴加氯水后再加入KSCN溶液,溶液变红 | 溶液中一定含有Fe2+ |
| D | 将FeCl3饱和溶液滴加到NaOH溶液中 | 可以制得Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向50 mL 0.018 mol·L-1的AgNO3溶液中加入50 mL 0.02 mol·L-1的盐酸生成沉淀。已知:Ksp(AgCl)=1.8×10-10,则生成沉淀后的溶液中c(Ag+)与pH分别为
| A.1.8×10-7mol·L-1,2 | B.1.8×10-8mol·L-1,2 |
| C.1.8×10-7mol·L-1,3 | D.1.8×10-8mol·L-1,3 |
您最近一年使用:0次
【推荐2】已知 时,
时, ,其沉淀溶解平衡曲线如图所示(图中R表示
,其沉淀溶解平衡曲线如图所示(图中R表示 或
或 ),下列说法正确的是(已知:
),下列说法正确的是(已知: )
)

 时,
时, ,其沉淀溶解平衡曲线如图所示(图中R表示
,其沉淀溶解平衡曲线如图所示(图中R表示 或
或 ),下列说法正确的是(已知:
),下列说法正确的是(已知: )
)
A.M点对应的溶液中, |
B.与P点相对应的 的分散系是均一稳定的 的分散系是均一稳定的 |
C. 的平衡常数 的平衡常数 |
| D.向N点对应的溶液中加水,可转化成Q点对应的溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】锂电池具有广泛应用。用废铝渣(含金属铝、锂盐等)获得电池级Li2CO3的一种工艺流程如下(部分物质已略去):

下列说法不正确 的是

下列说法
| A.①中加热后有SO2生成 |
B.②生成Al(OH)3的离子方程式:2Al3++3 +3H2O=2Al(OH)3↓+3CO2↑ +3H2O=2Al(OH)3↓+3CO2↑ |
| C.由③推测溶解度:CaCO3>Li2CO3 |
| D.④中不宜通入过多CO2,否则会造成Li2CO3产率降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在25℃,向含c(H+)=0.1 mol•L-1、c(Cu2+ )=c(Fe3+ )=0.01 mol•L-1的200 mL溶液中加入NaOH固体时,c(Cu2+ )、c(Fe3+ )随pH的变化曲线如图所示(忽略加入固体时溶液体积的变化)。下列叙述不正确的是


| A.Ksp[Fe(OH)3 ]<Ksp[Cu(OH)2] |
| B.pH=5时溶液中的阳离子主要为H+和Cu2+ |
| C.Ksp只与难溶电解质的性质和温度有关,而与离子浓度和沉淀的量均无关 |
| D.向含有FeCl3杂质的CuCl2溶液中加入CuO或CuCO3可除去溶液中混有的Fe3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向NaHSO3溶液中滴加足量Ba(OH)2溶液,出现白色沉淀,再加入足量盐酸,沉淀全部溶解 | NaHSO3未被氧化 |
| B | 向3mLFe(NO3)3溶液中滴加几滴HI溶液,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | I-的还原性比Fe2+的强 |
| C | 向MgSO4、CuSO4的混合稀溶液中滴入1滴稀NaOH溶液,有蓝色沉淀生成 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| D | 用精密pH试纸测得:浓度均为0.1mol·L-1的NH4HCO3溶液、HCOONa溶液的pH分别为7.8、10.0 | H2CO3电离出H+的能力比HCOOH的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 和
和 的
的 相对大小
相对大小 的
的 溶液中滴加
溶液中滴加 的
的 溶液,再滴加
溶液,再滴加 溶液
溶液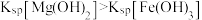
 ,一段时间后反应达平衡,压缩体积至原来的一半
,一段时间后反应达平衡,压缩体积至原来的一半 和
和 的
的 溶液
溶液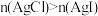 ,则
,则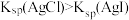
 与
与 的酸性
的酸性 计测定
计测定 溶液②
溶液② 溶液
溶液 和
和 的混合液中滴加
的混合液中滴加 与
与 代表
代表 或
或 ,
, 。下列叙述正确的是
。下列叙述正确的是
 分别代表
分别代表 与
与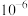

 和
和 共存时:
共存时:


