根据元素性质递变规律,下列判断不正确的是
| A.酸性:H2SiO3 < H3PO4 < H2SO4 | B.电负性:F > Cl > Br > I |
| C.第一电离能:Na < Mg < Al | D.原子半径:N > O > F |
21-22高二上·浙江绍兴·期中 查看更多[3]
浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题(已下线)第1.2.2讲 元素周期律-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)福建省莆田华侨中学2021-2022学年高二下学期期中考试化学试题
更新时间:2021/12/03 09:21:32
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法不正确的是
A.硫离子的结构示意图: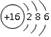 |
| B.铷、氯、锗三种元素中,适合作半导体材料的是锗 |
| C.氧元素位于第2周期VIA族 |
| D.同周期主族元素随着原子序数的递增,原子半径逐渐减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】我国拥有自主知识产权的铷(Rb)原子钟,能3000万年误差仅1秒。Rb是第五周期第IA族元素,下列关于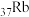 的说法错误的是
的说法错误的是
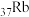 的说法错误的是
的说法错误的是| A.元素的金属性:Cs>Rb |
B.中子数为50的Rb的核素: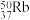 |
C.与同周期元素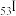 的原子半径比:I<Rb 的原子半径比:I<Rb |
| D.最高价氧化物对应的水化物的碱性:KOH<RbOH |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列有关碱金属元素和卤素的说法中,错误的是
| A.溴单质与H2的反应比碘单质与H2的反应更剧烈 |
| B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C.随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低 |
| D.钾与水的反应比钠与水的反应更剧烈 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列关于元素周期表的叙述中正确的是
| A.卤素单质随原子序数的增大,其氧化性逐渐增强 |
| B.碱金属随原子序数的增大,其熔沸点逐渐降低 |
| C.除0族元素外,族序数都等于该族元素的最外层电子数 |
| D.元素周期表共七个横行代表七个周期,18 个纵列代表18个族 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】离子液体是室温或稍高于室温时呈液态的离子化合物,常见的阴离子如 、
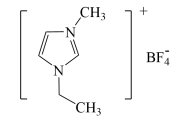
、 等。一种离子液体的结构如下图所示:下列与离子液体有关说法正确的是
等。一种离子液体的结构如下图所示:下列与离子液体有关说法正确的是
 、
、 等。一种离子液体的结构如下图所示:下列与离子液体有关说法正确的是
等。一种离子液体的结构如下图所示:下列与离子液体有关说法正确的是
A.第一电离能: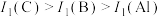 |
B.稳定性: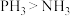 |
C.简单离子的半径: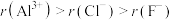 |
| D.离子液体有体积很大的阴、阳离子,故熔点较高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列性质的比较,不正确的是
| A.热稳定性:HCl>HBr>HI | B.酸性:HNO3>H3PO4>H2SiO3 |
| C.第一电离能:Al>Mg>Na | D.电负性:F>O>C |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】2023年诺贝尔化学奖被授予蒙吉·巴文迪、路易斯,布鲁斯和阿列克谢·叶基莫夫三位科学家,以表彰他们“发现和合成了量子点,为纳米技术埋下了重要种子”。钙钛矿量子点是结构与钙钛矿( )相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。
)相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。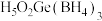 是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
 )相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。
)相似的一种新型纳米材料,应用于量子点显示与照明、太阳能电池等领域。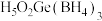 是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是
是钙钛矿型化合物,量子化学计算结果显示其具有良好的光电化学性能。下列说法错误的是A. 中B的杂化方式为 中B的杂化方式为 |
B.H、B、O的电负性大小顺序是 |
| C.基态Ge原子有32种不同运动状态的电子 |
| D.与Ti同周期且含有相同未成对电子数的主族元素有两种 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】光气( )是一种重要的有机中间体。利用反应可
)是一种重要的有机中间体。利用反应可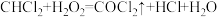 用于制备光气。下列有关叙述正确的是
用于制备光气。下列有关叙述正确的是
 )是一种重要的有机中间体。利用反应可
)是一种重要的有机中间体。利用反应可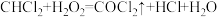 用于制备光气。下列有关叙述正确的是
用于制备光气。下列有关叙述正确的是A. 为非极性分子 为非极性分子 | B. 的电子式为 的电子式为 |
C. 、 、 分子间均能形成氢键 分子间均能形成氢键 | D.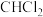 中电负性最小的元素是Cl 中电负性最小的元素是Cl |
您最近一年使用:0次

 微溶于水,
微溶于水, 难溶于水
难溶于水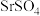 难溶于水(Sr与Ca、Ba同主族)
难溶于水(Sr与Ca、Ba同主族)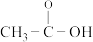 中σ键和π键的数目比为6:1
中σ键和π键的数目比为6:1 所含元素中第一电离能最大的是O
所含元素中第一电离能最大的是O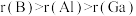
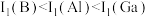
 、
、 均为共价晶体
均为共价晶体

