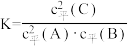SO2既是大气主要污染物之一,又在生产生活中具有广泛应用,如可生产SO3并进而制得硫酸等,其反应原理为:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1。实验室可用铜和浓硫酸制取SO2。对于反应2SO2(g)+O2(g)  2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.该反应在任何条件下都能自发进行 |
| B.反应达平衡后再通入O2,SO3的体积分数一定增加 |
| C.反应在高温、催化剂条件下进行可提高SO2的平衡转化率 |
| D.2 mol SO2(g)和1 mol O2(g)所含键能总和比2 mol SO3(g)所含键能小 |
2022·江苏·一模 查看更多[12]
江苏省南京市、盐城市2021-2022学年高三第一次模拟考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)天津市滨海新区2022届普通高考模拟试卷化学试题天津市高三九校2022届高三第二次模拟考试化学试题湖南省娄底市新化县第一中学2021-2022学年高三下学期模拟考试化学试题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题1-5)天津西青区2022-2023学年高三上学期期末考试化学试题江苏省南京市六校联合体2022-2023学年高二下学期5月期中考试化学试题(已下线)第08讲 化学反应的调控-【暑假自学课】2023年新高二化学暑假精品课(人教版2019选择性必修1)江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题
更新时间:2022-01-11 19:45:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
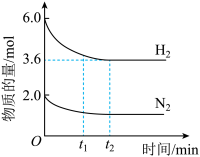
【推荐1】在2.0 L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,加入催化剂发生反应:N2(g)+3H2(g) 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
 2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
2NH3(g),N2、H2的物质的量随时间的变化如下图所示。下列有关说法正确的是
| A.t1 min时,N2的生成速率等于N2的消耗速率 |
| B.使用催化剂可以缩短到达平衡时所需的时间 |
C.0~t2 min内,v(NH3)= mol·L−1·min−1 mol·L−1·min−1 |
| D.反应中通入足量的N2,可使H2完全转化为NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】把2.5molA和2.5molB混合,装入容积为2L的密闭容器里,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述错误的是
| A.x=4 |
| B.达到平衡时容器内气体的压强与起始时的压强比为6:5 |
| C.达到平衡时B的转化率为50% |
| D.通过控制反应条件可以改变该可逆反应的限度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】阿伏加德罗常数的值约为6.02×1023mol-1,下列叙述中正确的是
| A.2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数等于2×6.02×1023 |
| B.电解精炼铜时转移了6.02×1023个电子,阴极析出32 g铜 |
| C.2.9g 2CaSO4·H2O含有的结晶水分子数为0.02×6.02×1023(2CaSO4·H2O式量为290) |
| D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1×6.02×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】活性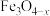 催化反应
催化反应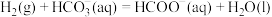 的部分机理如图所示。下列说法正确的是
的部分机理如图所示。下列说法正确的是
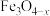 催化反应
催化反应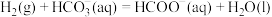 的部分机理如图所示。下列说法正确的是
的部分机理如图所示。下列说法正确的是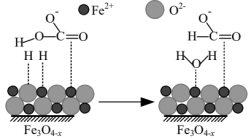
A.该反应的 |
B.该反应平衡常数 |
| C.反应前后碳原子杂化方式没有发生变化 |
D.吸附在 表面的 表面的 与 与 中的羟基结合生成水 中的羟基结合生成水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】以 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.
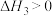
向恒压、密闭容器中通入1mol 和3mol
和3mol 发生上述反应,平衡时
发生上述反应,平衡时 、CO、
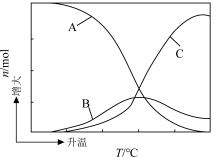
、CO、 的物质的量随温度的变化如图所示。下列说法正确的是
的物质的量随温度的变化如图所示。下列说法正确的是
 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:Ⅰ.


Ⅱ.


Ⅲ.

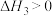
向恒压、密闭容器中通入1mol
 和3mol
和3mol 发生上述反应,平衡时
发生上述反应,平衡时 、CO、
、CO、 的物质的量随温度的变化如图所示。下列说法正确的是
的物质的量随温度的变化如图所示。下列说法正确的是
A.反应Ⅰ平衡常数可表示为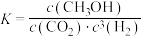 |
| B.图中曲线B表示CO的物质的量随温度的变化 |
C.某时刻 为a mol,CO为b mol,此时 为a mol,CO为b mol,此时 为 为 |
D.为提高 的平衡产率,需要选择低温、低压的反应条件 的平衡产率,需要选择低温、低压的反应条件 |
您最近一年使用:0次

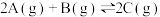 ,下列说法中正确的是
,下列说法中正确的是