用下列实验装置进行相应的实验,操作错误或不能达到实验目的的是
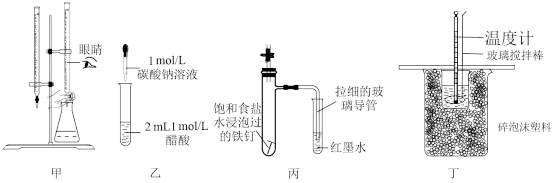

| A.图甲为NaOH标准溶液滴定锥形瓶中的盐酸 |
| B.用图乙装置验证电离平衡常数: Ka (CH3COOH)> Ka1(H2CO3) |
| C.用图丙装置探究铁钉在饱和食盐水中发生的电化学腐蚀类型 |
| D.用图丁可以测定中和反应的反应热 |
更新时间:2022-01-15 17:24:50
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列关于热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol |
| B.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5kJ/mol |
| C.在中和热的测定实验中,环形玻璃搅拌棒可以用铜质搅拌棒代替。 |
| D.需要加热才能发生的反应不一定是吸热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关说法正确的是
| A.陶瓷、水晶、水泥、玻璃都属于硅酸盐产品 |
| B.糖类、油脂、蛋白质都能发生水解反应 |
| C.进行中和热的测定实验时,必须用到两个量筒和两个温度计 |
| D.“血液透析”利用了胶体的渗析原理 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某学生用碱式滴定管量取0.1 mol/L的NaOH溶液,开始时仰视液面读数为1.00 mL,取出部分溶液后,俯视液面,读数为11.00 mL,该同学在操作中实际取出的液体体积为( )


| A.大于10.00 mL | B.小于10.00 mL |
| C.等于10.00 mL | D.等于11.00 mL |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列实验操作正确的是( )
| A.用pH试纸测定溶液的酸碱性时,应先用蒸馏水将其润湿 |
| B.滴定管在检查不漏水后,即可装满标准液进行滴定操作 |
| C.滴定过程中,视线应始终关注锥形瓶内液体颜色的变化 |
| D.滴定过程中,当指示剂颜色发生突变时,应立即进行读数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关实验原理或实验操作正确的是
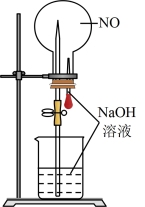
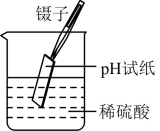
A.用蒸馏水润湿过的 试纸测量出某溶液的 试纸测量出某溶液的 |
B.用 量筒量取 量筒量取 溶液 溶液 |
| C.铁钉镀铜时,铁钉连接直流电源的正极 |
D.盛装 溶液的试剂瓶要使用橡胶塞 溶液的试剂瓶要使用橡胶塞 |
您最近一年使用:0次
【推荐2】下列过程或现象与盐类水解无关的是
| A.热的纯碱溶液去油污能力更强 |
| B.铁在潮湿的环境下生锈 |
| C.明矾可用来净水 |
| D.配制氯化铁溶液时先把氯化铁固体溶于浓盐酸再加水稀释 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在25 ℃时,0.1 mol·L-1的HNO2、HCOOH、HCN、H2CO3的溶液,电离平衡常数分别为5.6×10-4、1.8×10-4、6.2×10-10、 (H2CO3)=4.5×10-7和
(H2CO3)=4.5×10-7和 (H2CO3)=4.7×10-11,其中氢离子浓度最大的是
(H2CO3)=4.7×10-11,其中氢离子浓度最大的是
 (H2CO3)=4.5×10-7和
(H2CO3)=4.5×10-7和 (H2CO3)=4.7×10-11,其中氢离子浓度最大的是
(H2CO3)=4.7×10-11,其中氢离子浓度最大的是| A.HNO2 | B.HCOOH |
| C.HCN | D.H2CO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某温度下,CO2饱和溶液的浓度是0.03mol·L-1,其中 的CO2转变为H2CO3,而H2CO3仅有0.1%发生电离:H2CO3⇌H++
的CO2转变为H2CO3,而H2CO3仅有0.1%发生电离:H2CO3⇌H++ (忽略碳酸的第二步电离和水的电离),则溶液的pH约为
(忽略碳酸的第二步电离和水的电离),则溶液的pH约为
 的CO2转变为H2CO3,而H2CO3仅有0.1%发生电离:H2CO3⇌H++
的CO2转变为H2CO3,而H2CO3仅有0.1%发生电离:H2CO3⇌H++ (忽略碳酸的第二步电离和水的电离),则溶液的pH约为
(忽略碳酸的第二步电离和水的电离),则溶液的pH约为| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次



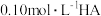 溶液中有1%的
溶液中有1%的 电离,则
电离,则 为
为





