前3周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,基态时Y最外层电子数是次外层的四分之一,基态Z原子3p轨道上只有1个电子,W与X位于同一主族。下列说法正确的是
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.第一电离能:I1(X)>I1(Y)>I1(Z) |
| C.X的简单气态氢化物分子的空间构型为平面三角形 |
| D.最高价氧化物对应水化物的碱性:Z>Y |
21-22高三上·江苏南通·阶段练习 查看更多[7]
广东省广州市白云中学2023-2024学年高三上学期9月月考化学试题(已下线)2023年广东卷高考真题变式题(选择题11-16)江苏省海安高级中学2022-2023学年高三下学期第五次阶段考试化学试题江苏省南京、镇江市部分名校2021-2022学年高二下学期期中学情调查考试化学试题江苏省镇江市第一中学2021~2022学年高二年级下学期期中考试化学试题辽宁省名校联盟2021-2022学年高二下学期4月联考化学试题(已下线)江苏省如皋市2021-2022学年高三上学期教学质量调研(三)化学试题
更新时间:2022-01-17 17:32:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】由原子序数依次增大的四种短周期主族元素X、Y、Z、W组成的化合物 是一种食品品质改良剂。已知X、Y、Z、W分属三个周期,X、W元素的原子序数之和是Y元素原子序数的2倍,且X、W元素原子的最外层电子数之和与Y元素原子最外层电子数相等,Z是短周期金属性最强的元素。下列说法正确的是
是一种食品品质改良剂。已知X、Y、Z、W分属三个周期,X、W元素的原子序数之和是Y元素原子序数的2倍,且X、W元素原子的最外层电子数之和与Y元素原子最外层电子数相等,Z是短周期金属性最强的元素。下列说法正确的是
 是一种食品品质改良剂。已知X、Y、Z、W分属三个周期,X、W元素的原子序数之和是Y元素原子序数的2倍,且X、W元素原子的最外层电子数之和与Y元素原子最外层电子数相等,Z是短周期金属性最强的元素。下列说法正确的是
是一种食品品质改良剂。已知X、Y、Z、W分属三个周期,X、W元素的原子序数之和是Y元素原子序数的2倍,且X、W元素原子的最外层电子数之和与Y元素原子最外层电子数相等,Z是短周期金属性最强的元素。下列说法正确的是A.原子半径: |
| B.W的最高价氧化物对应的水化物为强酸 |
C. 具有强还原性 具有强还原性 |
D. 不属于电解质 不属于电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】V、W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X、X与Z在周期表中位置分别相邻,化合物甲可表示为WV4Y(ZX4)2,其中除含有Y3+外,另外两种离子的结构如图所示,下列判断错误的是
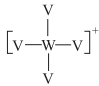
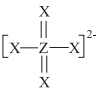
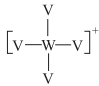
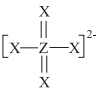
| A.化合物甲的水溶液可用于净水 |
| B.W的单质很稳定,常用于保存粮食 |
| C.简单氢化物的沸点:X>W>Z |
| D.简单离子半径:Y>Z>X |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W为短周期主族元素,其原子序数依次增大,Y、Z、W位于同一周期,W原子的最外层电子数与Y原子的电子总数相同,它们形成的某阴离子的结构如图所示。下列说法正确的是
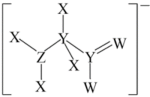

| A.X与钠元素形成的化合物具有强氧化性 |
B.化合物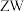 可用向上排空气法收集 可用向上排空气法收集 |
| C.Y的氢化物的沸点一定小于W的氢化物的沸点 |
D.最高价氧化物对应水化物的酸性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次减小,其中只有Z为金属元素,X、Y、Z同周期且位于不同奇数族,Z、W同主族,Y、Z的原子序数相差4。下列说法正确的是( )
| A.W的简单阴离子半径一定大于Z的简单阳离子半径 |
| B.非金属性:X>Y,所以X和Y分别对应含氧酸的酸性:X一定强于Y |
| C.X、 Y形成的单质一定都是双原子分子 |
D.Z、W形成化合物的电子式为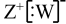 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某离子液体结构如图所示,其中X、Y、Z、M、W均为短周期元素且原子序数依次增大,X是宇宙中最丰富的元素,Z与W同主族,下列说法错误的是


A.氢化物沸点可能 |
B.第一电离能和电负性均有 |
| C.该离子液体中存在配位键和氢键 |
| D.相较于易挥发且有毒的有机溶剂,其更适合做有机合成溶剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面。下列说法不正确的是

| A.酞菁中,元素的第一电离能由大到小的顺序为N>H>C |
| B.酞菁中,标注③的N原子p轨道能提供1个电子 |
| C.酞菁钴中,钴离子的化合价为+2 |
| D.酞菁钴中,钴离子的配位数为4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中正确的是
| A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构 |
| B.P4和CH4都是正四面体分子且键角都为109o28ˊ |
| C.NaCl晶体中与每个Na+距离相等且最近的Na+共有8个 |
| D.单质的晶体中一定不存在的微粒是阴离子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列化学用语表示正确的是
A.中子数为16的磷原子: |
B. 分子的VSEPR模型: 分子的VSEPR模型: |
C. 的电子式: 的电子式: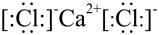 |
D.顺-2-丁烯的结构简式: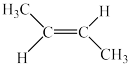 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】硫的化合物种类繁多。利用H2S废气制取单质硫的常见途径有:①用O2将部分H2S氧化为SO2,SO2与剩余H2S反应得到硫单质,总反应为2H2S(g)+O2(g)=2S(s)+2H2O(g) △H<0;②用ZnO与H2S反应生成ZnS,再用Fe2(SO4)3溶液浸取ZnS得到单质硫。下列有关H2S、SO2、SO 、SO
、SO 的说法正确的是
的说法正确的是
 、SO
、SO 的说法正确的是
的说法正确的是| A.H2S的稳定性比H2O的强 | B.SO2与H2S反应体现SO2的还原性 |
C.SO 的空间构型为平面三角形 的空间构型为平面三角形 | D.SO 中S原子轨道杂化类型为sp3 中S原子轨道杂化类型为sp3 |
您最近一年使用:0次




