 在
在 催化剂表面脱氢的反应机理,反应历程与能量的关系如图所示:
催化剂表面脱氢的反应机理,反应历程与能量的关系如图所示:
下列说法错误的是
A.在历程Ⅰ~Ⅴ中,涉及了 、 、 、 、 的断裂 的断裂 |
B.在历程Ⅰ~Ⅴ中,生成V的反应决定了 脱氢反应的速率 脱氢反应的速率 |
C.若用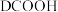 或 或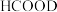 代替 代替 ,得到的产物都有 ,得到的产物都有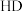 和 和 |
D.在 催化剂表面 催化剂表面 脱氢反应的 脱氢反应的 |
21-22高二上·湖南·期末 查看更多[5]
湖南省湖湘名校联盟2021-2022学年高二上学期期末考试化学试题湖南省湘潭县2021-2022学年高二上学期期末考试化学试题四川省成都外国语学校2022-2023学年高二上学期12月月考化学试题(已下线)上海市静安区2022-2023学年高三下学期二模变式题(选择题16-20)新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题
更新时间:2022-01-20 19:21:18
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】在一定条件下A与B反应可生成C和D,其能量变化如下图,下列有关反应的说法正确的是


| A.反应前后原子的种类和数目一定不变 |
| B.反应前后分子的种类和数目一定改变 |
| C.反应物的总能量E1与生成物的总能量E2一定相等 |
| D.此反应一定是吸热反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
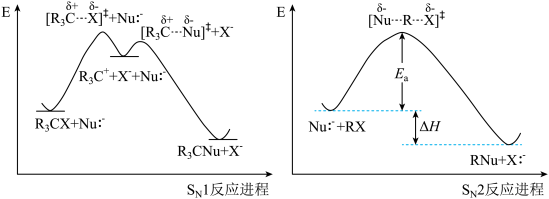
【推荐2】丙烷的一溴代反应产物有两种: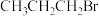 和
和 ,部分反应过程的能量变化如图所示(
,部分反应过程的能量变化如图所示( 表示活化能)。
表示活化能)。
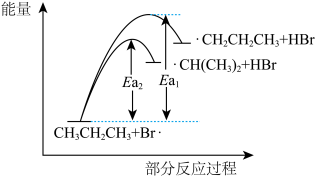
下列说法不正确的是
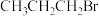 和
和 ,部分反应过程的能量变化如图所示(
,部分反应过程的能量变化如图所示( 表示活化能)。
表示活化能)。
下列说法不正确的是
A.稳定性: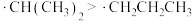 |
B. 与 与 的反应涉及极性键和非极性键的断裂 的反应涉及极性键和非极性键的断裂 |
C.  |
D.比较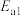 和 和 推测生成速率: 推测生成速率: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究人员发现,一定条件下,Pt 单原子催化剂有着高达 90.3%的甲醇选择性。反应历程如图,其中吸附在催化剂表面上的物种用*表示,TS 表示过渡态。
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究人员发现,一定条件下,Pt 单原子催化剂有着高达 90.3%的甲醇选择性。反应历程如图,其中吸附在催化剂表面上的物种用*表示,TS 表示过渡态。
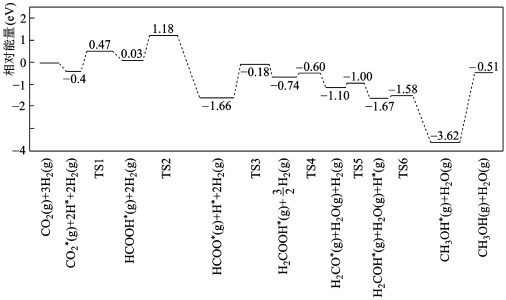
下列说法正确的是
 CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究人员发现,一定条件下,Pt 单原子催化剂有着高达 90.3%的甲醇选择性。反应历程如图,其中吸附在催化剂表面上的物种用*表示,TS 表示过渡态。
CH3OH(g)+H2O(g)使用不同催化剂的调控中,研究人员发现,一定条件下,Pt 单原子催化剂有着高达 90.3%的甲醇选择性。反应历程如图,其中吸附在催化剂表面上的物种用*表示,TS 表示过渡态。
下列说法正确的是
| A.该反应的△H>0 |
| B.经历 TS1,CO2共价键发生断裂,且生成羧基 |
C.能垒(活化能)为 1.48ev 的反应为 HCOOH*(g)+2H2(g)=H2COOH*(g)+ H2(g) H2(g) |
| D.如果换用铜系催化剂,所得反应历程与上图相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列形式表示的反应为放热反应的是( )
A.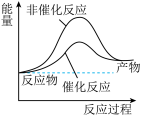 | ||||||||
B.
| ||||||||
C.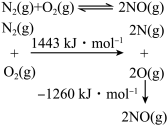 | ||||||||
D.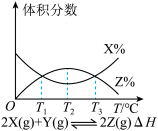 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某杂志曾报道过某课题组利用磁性纳米Fe3O4颗粒除去水体中草甘膦污染物的方法,其原理如图所示(Fe3O4颗粒在水中表面会带-OH)。下列说法不正确的是


| A.草甘膦能与氢氧化钠溶液反应 |
| B.Fe3O4纳米颗粒除去草甘膦的过程有化学键的形成和断裂 |
| C.溶液中c(H+)越大,Fe3O4纳米颗粒除污效果越好 |
| D.处理完成后,Fe3O4纳米颗粒可用磁铁回收,经加热活化重复使用 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】XH和 反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和
反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和 ,
, 时测得
时测得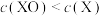 ,下列有关说法不正确的是
,下列有关说法不正确的是

 反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和
反应生成X或XO的能量-历程变化如图。在恒温恒容的密闭容器中加入一定量的XH和 ,
, 时测得
时测得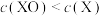 ,下列有关说法不正确的是
,下列有关说法不正确的是
A.热化学方程式可表示为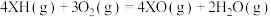 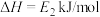 |
B.由图可知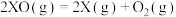 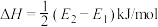 |
C.只改变反应温度, 时可能出现 时可能出现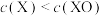 |
D. 时容器内的压强比初始状态更大 时容器内的压强比初始状态更大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在催化剂表面,丙烷催化氧化脱氢反应历程如图。下列说法正确的是
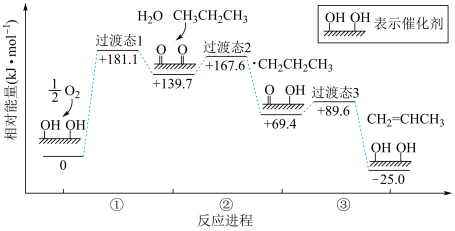
| A.①中,催化剂被还原 | B.②中,丙烷分子中的亚甲基先失去氢原子 |
| C.③中,仅涉及极性键的断裂与形成 | D.①决定总反应的速率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中图像和实验结论表达均正确的是
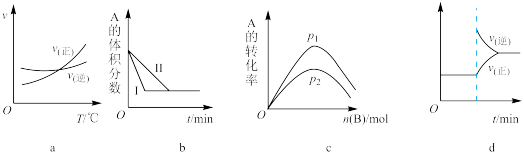

A.a是其他条件一定时A(g)+3B(g) 2C(g),反应速率随温度变化的图像,正反应ΔH<0 2C(g),反应速率随温度变化的图像,正反应ΔH<0 |
B.b反应A(g)+3B(g) 2C(g)建立的平衡过程中,曲线I比曲线II反应时活化能低 2C(g)建立的平衡过程中,曲线I比曲线II反应时活化能低 |
C.c反应A(g)+B(g) 2C(g)是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强P1>P2 2C(g)是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强P1>P2 |
D.d反应FeCl3+3KSCN Fe(SCN)3+3KCl是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像 Fe(SCN)3+3KCl是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】金(Au)表面发生分解反应: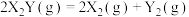 ,其速率方程为
,其速率方程为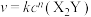 。已知部分信息如下:
。已知部分信息如下:
①k为速率常数,只与催化剂、温度、固体接触面积有关,与浓度、压强无关;
②n为反应级数,可以取整数、分数,如0、1、2、 等;
等;
③化学上,将物质消耗一半所用时间称为半衰期。
在某温度下,实验测得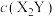 与时间变化的关系如下表所示:
与时间变化的关系如下表所示:
下列叙述正确的是
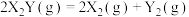 ,其速率方程为
,其速率方程为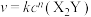 。已知部分信息如下:
。已知部分信息如下:①k为速率常数,只与催化剂、温度、固体接触面积有关,与浓度、压强无关;
②n为反应级数,可以取整数、分数,如0、1、2、
 等;
等;③化学上,将物质消耗一半所用时间称为半衰期。
在某温度下,实验测得
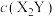 与时间变化的关系如下表所示:
与时间变化的关系如下表所示:| t/min | 0 | 20 | 40 | 60 | 80 | 100 |
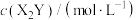 | 0.100 | 0.080 | 0.060 | 0.040 | 0.020 | 0 |
A.速率常数k等于 反应速率即为 反应速率即为 |
| B.该反应属于2级反应,不同催化剂可能会改变反应级数 |
C.升温或增大催化剂表面积,反应10min时 浓度净减小于 浓度净减小于 |
D.其他条件不变,若 起始浓度为 起始浓度为 ,则半衰期为500cmin ,则半衰期为500cmin |
您最近一年使用:0次

 ②
② 。述反应过程中的能量变化如图所示。下列说法正确的是
。述反应过程中的能量变化如图所示。下列说法正确的是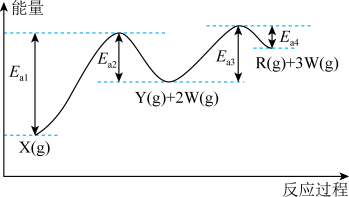
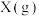 的能量低于1mol
的能量低于1mol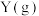 的能量
的能量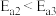 ,反应①的速率大于反应②的速率
,反应①的速率大于反应②的速率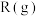 和3mol
和3mol 中的化学键所放出的能量
中的化学键所放出的能量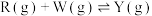
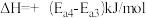
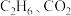 为原料合成
为原料合成 ,主要反应有:
,主要反应有: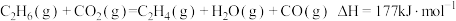
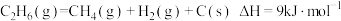
 的
的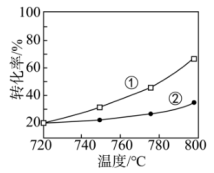

 转化率随温度的变化
转化率随温度的变化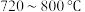 范围内,随温度的升高,
范围内,随温度的升高, 的量均增大
的量均增大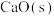 或选用高效催化剂,均能提高平衡时
或选用高效催化剂,均能提高平衡时

