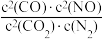下列说法正确的是
| A.CaCO3(s)=CaO(s)+CO2(g) △H=+178.5kJ·mol-1,该反应低温才能自发 |
| B.需要加热才能发生的反应一定是吸热反应 |
| C.在任何条件下,化学反应的焓变都等于化学反应的反应热 |
| D.常温下,反应A(s)+B(g)=2X(g)不能自发进行,则该反应的ΔH>0 |
更新时间:2021-12-29 14:19:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】两种制备硫酸的途径(反应条件略)如图。下列说法正确的是
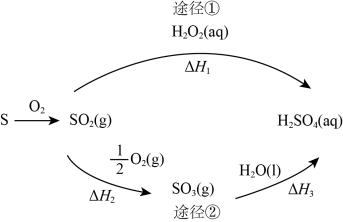

| A.S和过量O2反应可直接生成SO3 |
| B.SO2能使紫色石蕊试液先变红后褪色 |
C.若△H1<△H2+△H3,则 为放热反应 为放热反应 |
| D.含0.5 mol H2SO4的稀溶液与足量Ba(OH)2溶液反应,放出的热量即为中和热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】化学反应一定伴随旧化学键的断裂和新化学键的形成。根据下表数据,有关反应 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是| 化学键 | H-H | Cl-Cl | H-Cl |
| 断开1mol化学键需要的能量/kJ | 436 | 243 | 431 |
A. 和 和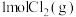 的总能量比 的总能量比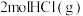 的总能量低 的总能量低 |
| B.相同条件下,氢气分子具有的能量高于氯气分子具有的能量 |
| C.该反应需要点燃或强光照射,属于吸热反应 |
| D.每生成1molHCl气体,该反应将放出91.5kJ能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知:①4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol—1
4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol—1
②N2(g)+O2(g) 2NO(g)△H2
2NO(g)△H2
一定条件下,NO可以与NH3反应转化为无害的物质,反应如下
③NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2Og) ΔH3=—1625.5 kJ·mol—1
4N2(g)+6H2Og) ΔH3=—1625.5 kJ·mol—1
下列说法不正确的是
 4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol—1
4NO(g)+6H2O(g) ΔH1=-905.5kJ·mol—1②N2(g)+O2(g)
 2NO(g)△H2
2NO(g)△H2一定条件下,NO可以与NH3反应转化为无害的物质,反应如下
③NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2Og) ΔH3=—1625.5 kJ·mol—1
4N2(g)+6H2Og) ΔH3=—1625.5 kJ·mol—1下列说法不正确的是
| A.反应③一定能自发进行 |
| B.反应②生成物总能量高于反应物总能量 |
| C.反应①使用催化剂,反应速率加快,△H1减小 |
D.反应③达到平衡后改变条件,v(正)、v(逆)的变化如图所示,则该条件可能是升高温度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】乙烯与氯化氢气体催化加成反应的能量与反应历程的关系如图所示,下列说法正确的是
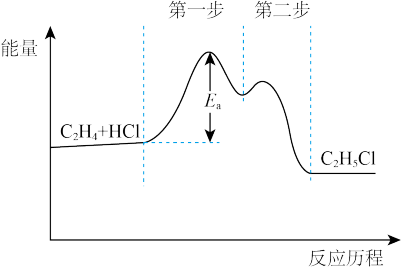

| A.第一步反应比第二步的快 |
| B.两步反应的H均小于0 |
| C.第一步的逆反应活化能比第二步的小 |
| D.催化剂可以使该反应的速率和焓变增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】研究表明,利用 可消除大气污染物
可消除大气污染物 和
和 ,反应过程中相对能量变化如图所示。下列说法错误的是( )
,反应过程中相对能量变化如图所示。下列说法错误的是( )
 可消除大气污染物
可消除大气污染物 和
和 ,反应过程中相对能量变化如图所示。下列说法错误的是( )
,反应过程中相对能量变化如图所示。下列说法错误的是( )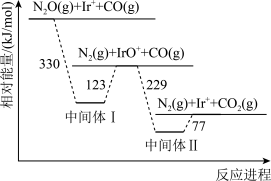
A. 为放热反应 为放热反应 |
| B.中间体I的相对能量比中间体Ⅱ高 |
C.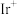 在整个过程都未参与反应 在整个过程都未参与反应 |
| D.反应过程中有极性键形成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 催化重整能够获得氢能,同时消除温室气体,催化重整过程中主要发生反应的热化学方程式如下:
催化重整能够获得氢能,同时消除温室气体,催化重整过程中主要发生反应的热化学方程式如下:
反应①

反应②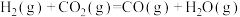

反应③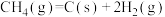
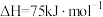
常压下,将 的混合气体置于密闭容器中,在不同温度下的重整体系中,平衡时各组分的物质的量分数如图所示。下列说法
的混合气体置于密闭容器中,在不同温度下的重整体系中,平衡时各组分的物质的量分数如图所示。下列说法不正确 的是

 催化重整能够获得氢能,同时消除温室气体,催化重整过程中主要发生反应的热化学方程式如下:
催化重整能够获得氢能,同时消除温室气体,催化重整过程中主要发生反应的热化学方程式如下:反应①


反应②
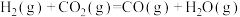

反应③
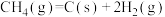
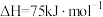
常压下,将
 的混合气体置于密闭容器中,在不同温度下的重整体系中,平衡时各组分的物质的量分数如图所示。下列说法
的混合气体置于密闭容器中,在不同温度下的重整体系中,平衡时各组分的物质的量分数如图所示。下列说法
| A.反应①是催化重整的主反应 |
B.反应②的 |
| C.450-800℃间,反应②的进行程度大于反应③ |
D.为提高平衡时 的产率,应研发更合适的催化剂 的产率,应研发更合适的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】含硫矿物是多种化工生产的原料,主要有硫磺、黄铁矿( )、辉铜矿(
)、辉铜矿( )、明矾
)、明矾 、绿矾(
、绿矾( )、胆矾(
)、胆矾( )、重晶石(
)、重晶石( )等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应:
)等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化,或用石灰乳、
直接排放会造成环境污染,可将其转化,或用石灰乳、 等物质进行回收再利用。对于反应
等物质进行回收再利用。对于反应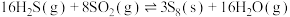
 ,下列说法正确的是
,下列说法正确的是
 )、辉铜矿(
)、辉铜矿( )、明矾
)、明矾 、绿矾(
、绿矾( )、胆矾(
)、胆矾( )、重晶石(
)、重晶石( )等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应:
)等。硫磺、黄铁矿可作为工业制硫酸的原料,辉铜矿煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化,或用石灰乳、
直接排放会造成环境污染,可将其转化,或用石灰乳、 等物质进行回收再利用。对于反应
等物质进行回收再利用。对于反应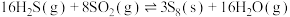
 ,下列说法正确的是
,下列说法正确的是A.该反应 |
B.反应平衡常数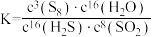 |
| C.其他条件一定,增大体系的压强可以增大反应的平衡转化率 |
| D.其他条件一定,升高温度可以增大反应的平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应
 可实现
可实现 的资源化,下列说法正确的是
的资源化,下列说法正确的是

 可实现
可实现 的资源化,下列说法正确的是
的资源化,下列说法正确的是| A.上述反应在任何温度下均可自发进行 |
B.上述反应每消耗1mol  同时形成7mol σ键 同时形成7mol σ键 |
C.上述反应平衡常数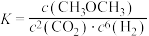 |
| D.催化剂可以降低上述反应的焓变,提高化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的方向和限度的说法中正确的是
A.mA(g)+nB(g) pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p |
B.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据 2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据 |
| C.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0 |
D.对于反应A(g)+B(g) 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变 |
您最近一年使用:0次