化学反应进行的方向和限度是化学反应原理所要研究的两个重要问题,下列有关化学反应进行的方向和限度的说法中正确的是
A.mA(g)+nB(g) pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p pC(g),平衡时A的浓度等于0.5mol/L,将容器体积扩大一倍,达到新的平衡后A的浓度变为0.3mol/L,则计量数m+n < p |
B.将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据 2NH3(g)+CO2(g),则CO2的体积分数不变可以作为平衡判断的依据 |
| C.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的ΔH>0 |
D.对于反应A(g)+B(g) 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分数为n%,此时若给体系加压则A的体积分数不变 |
17-18高二下·福建泉州·期末 查看更多[12]
福建省晋江市季延中学2017-2018学年高二下学期期末考试化学试题河北省隆化县存瑞中学2019届高三上学期期中考试化学试题甘肃省兰州第一中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】福建省厦门市外国语学校2018-2019学年高二下学期期中考试化学试题贵州省遵义航天高级中学2019-2020学年高二上学期期中考试化学(理)试题【懂做原理题】2020届高三化学选修4二轮专题练——化学平衡移动及其影响因素【精编25题】湖南省常德市石门县第六中学2019-2020学年高二下学期期末考试化学试题陕西省西安中学2021-2022学年高二上学期期中考试化学试题陕西省渭南高级中学2021-2022学年高一下学期第三阶段考试化学试题宁夏吴忠中学2022-2023学年高二上学期期中考试化学试题福建省福州第三中学2022-2023学年高二上学期半期考试化学试题福建省漳州市正兴学校2023-2024学年高二上学期10月月考化学试卷
更新时间:2019-05-09 20:38:23
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2L的恒容密闭容器中发生反应: 2SO2(g)+O2(g) 2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:
下列说法正确的是
 2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A.该反应进行到第3分钟时,逆反应速率大于正反应速率 |
| B.若要提高SO2的转化率,可用空气代替纯氧气并鼓入过量空气 |
| C.从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L·min) |
| D.容器内达到平衡状态时的压强与起始时的压强之比为5∶4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
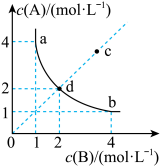
【推荐2】t ℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g) C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
 C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s) ΔH<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
| A.t ℃时,该反应的平衡常数值为0.35 |
| B.c点没有达到平衡,此时反应向逆向进行 |
| C.若c为平衡点,则此时容器内的温度高于t ℃ |
| D.t ℃时,直线cd上的点均为平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应 是放热反应。下列有关说法正确的是
是放热反应。下列有关说法正确的是
 是放热反应。下列有关说法正确的是
是放热反应。下列有关说法正确的是A.使用合适的高效催化剂,可以实现 的完全转化 的完全转化 |
B.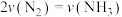 时,反应达到平衡状态 时,反应达到平衡状态 |
C.1 mol 和3 mol 和3 mol  的总能量大于2 mol 的总能量大于2 mol 的能量 的能量 |
D.断开1 mol 和3 mol 和3 mol  中共价键吸收的总能量大于形成2 mol 中共价键吸收的总能量大于形成2 mol 中共价键放出的能量 中共价键放出的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对可逆反应:4NH3(g)+5O2(g)  4NO(g)+6H2O(g),则下列叙述中正确的是
4NO(g)+6H2O(g),则下列叙述中正确的是
 4NO(g)+6H2O(g),则下列叙述中正确的是
4NO(g)+6H2O(g),则下列叙述中正确的是| A.达到化学平衡时,5v正(O2)=4v逆(NO) |
| B.若单位时间内生成nmolNO的同时,生成nmolNH3,则反应达到平衡状态 |
| C.若NH3、O2、NO、H2O的分子数之比为4∶5∶4∶6时,反应达到化学平衡状态 |
| D.化学反应速率关系是:2v正(NH3)=3v正(H2O) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于热化学反应的描述中正确的是
A.在一定的条件下将1molSO2和0.5molO2置于密闭容器中充分反应,放出热量79.2kJ,则反应的热化学方程式为2SO2(g)+O2(g) 2SO3(g) △H=-158.4kJ/mol 2SO3(g) △H=-158.4kJ/mol |
| B.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=-114.6kJ/mol |
| C.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+283.0kJ/mol |
| D.常温下,MgO(s)+C(s)=Mg(s)+CO(g)不能自发进行,则其△H>0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是
| A.一定条件下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)⇌2NH3(g) ΔH=-38.6kJ·mol-1 |
| B.2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)在低温下能自发进行,则该反应△H>0 |
| C.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则1mol硫酸与足量氨水反应放热为114.6kJ |
| D.H2(g)的燃烧热是285.8kJ·mol-1,则2H2O(l)=2H2(g)+O2(g)反应的ΔH=+571.6kJ·mol-1 |
您最近一年使用:0次



