C、Si和P元素的前四级电离能变化趋势如图所示。下列说法不正确的是
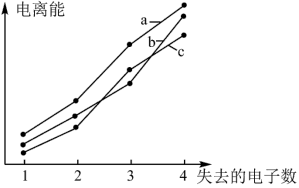

| A.c为Si元素 | B.最简单气态氢化物的热稳定性:c>a>b |
| C.元素的电负性:a>c>b | D.第五电离能:a>c>b |
更新时间:2022-01-05 18:08:20
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】依据元素周期律,下列判断错误 的是
A.第一电离能: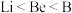 | B.原子半径: |
C.电负性: | D.酸性: |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】C、N、O、Si、P、Ge、As及其化合物在科研和生产中有许多重要用途。下列相关叙述正确的是


| A.基态氮原子核外电子占据的原子轨道数目为5 |
B.图1表示碳、硅和磷三种元素的四级电离能变化趋势,其中表示磷的曲线是 |
C. 的分子结构如图2所示,则在该化合物中 的分子结构如图2所示,则在该化合物中 的杂化方式是 的杂化方式是 |
D. 的稳定性比 的稳定性比 高,原因是 高,原因是 键能大于 键能大于 键能 键能 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】对于基态Cr原子,下列叙述正确的是
| A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1 |
| B.4s电子能量较高,总是在比3d电子离核更远的地方运动 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】化合物A (结构如下图)由原子序数依次增大的X、Y、Z、W短周期元素组成,常用来做金属矿物的浮选剂。已知Z与W位于不同周期。下列说法正确的是


| A.四种元素中X的电负性最小 |
| B.最简单气态氢化物的稳定性:Z<Y |
| C.W位于周期表的第二周期VIA族 |
| D.四种元素可组成既含离子键又含共价键的化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】M、X、Y、Z四种短周期主族元素,M为金属元素,X、Y和Z为非金属元素,原子序数Z<X<M<Y。M在常压下可生成 :
: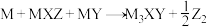 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下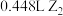 ,
, 可表示成
可表示成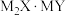 形式。下列说法正确的是
形式。下列说法正确的是
 :
: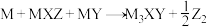 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下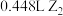 ,
, 可表示成
可表示成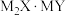 形式。下列说法正确的是
形式。下列说法正确的是| A.基态M原子核外电子空间运动状态有6种 |
| B.电负性:X<Y |
C.Z与X能组合成非极性分子 |
D. 与水反应能得到含有离子键和极性共价键的产物 与水反应能得到含有离子键和极性共价键的产物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】前四周期元素V、W、X、Y、Z(不含过渡元素)原子序数依次增大,V的基态原子有2个未成对电子, 是VX的等电子体,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,Z的价电子数是Y的3倍。下列说法错误的是
是VX的等电子体,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,Z的价电子数是Y的3倍。下列说法错误的是
 是VX的等电子体,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,Z的价电子数是Y的3倍。下列说法错误的是
是VX的等电子体,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,Z的价电子数是Y的3倍。下列说法错误的是| A.Y与X可形成含非极性共价键的化合物 |
| B.同周期中比元素W第一电离能大的元素有3种 |
| C.氢化物的沸点:X<W<V |
| D.Z的最高价氧化物的水化物可能具有两性 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】某盐{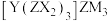 }由原子序数依次增大的短周期主族元素X、Y、Z、M组成,X原子的核内质子数为1,基态原子M的价层电子排布为
}由原子序数依次增大的短周期主族元素X、Y、Z、M组成,X原子的核内质子数为1,基态原子M的价层电子排布为 ,基态原子的第一电离能排序为:Z>M>Y,下列说法
,基态原子的第一电离能排序为:Z>M>Y,下列说法不正确 的是
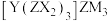 }由原子序数依次增大的短周期主族元素X、Y、Z、M组成,X原子的核内质子数为1,基态原子M的价层电子排布为
}由原子序数依次增大的短周期主族元素X、Y、Z、M组成,X原子的核内质子数为1,基态原子M的价层电子排布为 ,基态原子的第一电离能排序为:Z>M>Y,下列说法
,基态原子的第一电离能排序为:Z>M>Y,下列说法| A.Y的最简单氢化物的二氯取代产物有2种 |
B.化合物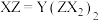 具有较强的碱性 具有较强的碱性 |
C.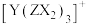 离子中Y发生 离子中Y发生 杂化 杂化 |
| D.简单氢化物的沸点:Z>M |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列各项叙述中,正确的是
| A.电负性:S>As>Se | B.键角:H2O<NH3<CH4 |
| C.沸点:HF>HCl>HBr>HI | D.离子还原性:S2->I->Br->Cl- |
您最近一年使用:0次
【推荐2】下列事实能证明氮元素的非金属性强于磷元素的是
| A.沸点:NH3>PH3 |
| B.酸性:HNO3>H3PO4 |
| C.P4与浓硝酸反应生成H3PO4与NO2 |
D. 中N—P共用电子对偏向N 中N—P共用电子对偏向N |
您最近一年使用:0次

 能反映钠原子轨道的能级差别和电子的自旋状态
能反映钠原子轨道的能级差别和电子的自旋状态 基态原子的核外电子排布式为:
基态原子的核外电子排布式为: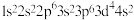
 、
、 ……表示,单位为
……表示,单位为 )。
)。




