C、N、O、Si、P、Ge、As及其化合物在科研和生产中有许多重要用途。下列相关叙述正确的是


| A.基态氮原子核外电子占据的原子轨道数目为5 |
B.图1表示碳、硅和磷三种元素的四级电离能变化趋势,其中表示磷的曲线是 |
C. 的分子结构如图2所示,则在该化合物中 的分子结构如图2所示,则在该化合物中 的杂化方式是 的杂化方式是 |
D. 的稳定性比 的稳定性比 高,原因是 高,原因是 键能大于 键能大于 键能 键能 |
更新时间:2023-08-05 10:54:48
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】下列有关物质结构与性质说法正确的是
A.2022年诺贝尔化学奖授予三位在“点击化学和生物正交化学”方面做出突出贡献的科学家。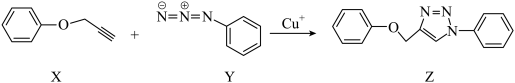 ,其中Z分子中含有1个手性碳原子 ,其中Z分子中含有1个手性碳原子 |
B.氟的电负性大于氯,所以三氟乙酸的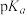 比三氯乙酸小 比三氯乙酸小 |
| C.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关 |
| D.基态铝原子有7种伸展方向,核外电子的空间运动状态有13种 |
您最近一年使用:0次
【推荐2】“嫦娥石”是中国首次在月球上发现的新矿物,其主要由Ca、Fe、P、O和Y(钇,原子序数比Fe大13)组成,下列说法正确的是
| A.Y位于元素周期表的第ⅢB族 |
| B.基态Ca原子的核外电子填充在6个轨道中 |
| C.Fe2+和 Fe3+中未成对电子个数之比为4:5 |
| D.5种元素中,电负性最大的是P |
您最近一年使用:0次
【推荐1】以下有关元素性质的说法不正确的是
| A.①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是④ |
| B.某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,该元素可能在第3周期第IIA族 |
| C.下列原子中,①1s22s22p63s23pl②1s22s22p63s23p2③1s22s22p63s23p3④1s22s22p63s23p4,对应的第一电离能最大的是④ |
| D.①Na、K、Rb,②N、P、As,③O、S,Se,④Na、P、O元素的电负性随原子序数增大而递增的是④ |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】某种化学品的结构如图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周期,Z、M同处另一周期,M原子的最外层电子数等于其电子层数,则下列说法中正确的是
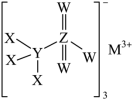

A.元素对应简单离子半径大小关系为: |
| B.与W的同周期元素中,第一电离能比W大的元素有3种 |
| C.Z、W形成的简单氢化物,分子空间构型相同,分子中化学键的键角不相等 |
| D.在该化合物中Y和Z的杂化类型不同 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E为20号以前的元素,原子序数逐渐增大,A元素的原子最外层电子排布式为 ;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高能级的电子对数等于其最高能层的电子层数,下列说法正确的是
;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高能级的电子对数等于其最高能层的电子层数,下列说法正确的是
 ;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高能级的电子对数等于其最高能层的电子层数,下列说法正确的是
;A与C同一周期,基态C原子的s轨道与p轨道电子数相等;D、E元素的基态原子都只有一个未成对电子,它们相互作用形成的离子的电子层结构相同,并且离子最高能级的电子对数等于其最高能层的电子层数,下列说法正确的是| A.A→B→C得电子能力越来越强,其最简单氢化物的稳定性:A>B>C |
| B.同周期元素第一电离能小于C的有4种 |
| C.氧化物对应水化物的酸性:D>B>A |
| D.A、D和C、E形成的化合物中可能均含有非极性共价键 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】Beckmann反应是肟指在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子的氢原子上,具体反应历程如图所示。
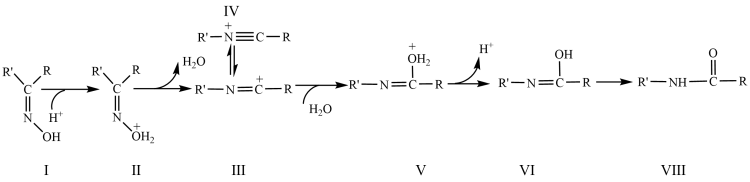
已知:R、R′代表烷基。
下列说法错误的是

已知:R、R′代表烷基。
下列说法错误的是
| A.H+在该反应过程中作催化剂 | B.N—O—H键角:物质Ⅰ>物质Ⅱ |
| C.物质Ⅲ→物质Ⅳ有配位键的形成 | D. 发生上述反应生成 发生上述反应生成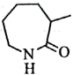 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】氯元素有多种化合价,可形成Cl—、ClO—、ClO 、ClO
、ClO 、ClO
、ClO 等离子,下列说法错误的是
等离子,下列说法错误的是
 、ClO
、ClO 、ClO
、ClO 等离子,下列说法错误的是
等离子,下列说法错误的是| A.基态氯原子的核外电子有17种空间运动状态 |
B.键角:ClO >ClO >ClO >ClO >ClO |
| C.Cl、O均属于元素周期表中p区元素 |
D.ClO 、ClO 、ClO 、ClO 、ClO 的中心原子上的价层中子对数相等 的中心原子上的价层中子对数相等 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】六氟磷酸盐离子液体(M)可用于有机合成的溶剂和催化剂。 由有机阳离子
由有机阳离子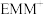 (
(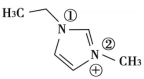 )和阴离子
)和阴离子 构成,
构成,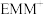 中环上所有原子共平面。下列说法错误的是
中环上所有原子共平面。下列说法错误的是
A.1个阳离子中 键数目为16 键数目为16 |
| B.阳离子中存在配位键 |
C.②号 原子为 原子为 杂化 杂化 |
D.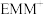 与 与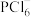 形成的离子液体熔点低于 形成的离子液体熔点低于 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】CH4、H2O、H2S、NaH均为在生产生活中有重要应用的氢化物,其中NaH具有NaCl型结构。几种氢化物的熔点如下表所示。
下列说法正确的是
| 氢化物 | CH4 | H2S | H2O | NaH |
| 熔点/℃ | -182.5 | -85.5 | 0 | 800 |
| A.键角:H2S<CH4 |
| B.CH4、H2S、H2O的熔点差异的主要原因是化学键键能不同 |
C.若NaH的晶胞参数为a pm,则其密度为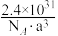 g·cm-3 g·cm-3 |
| D.NaH晶体中,Na+填充在H-围成的正八面体中心 |
您最近一年使用:0次

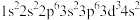
 )是具有层状结构的晶体,硼酸层内的分子通过氢键相连(如图所示),硼酸溶解度随温度升高而增大,并能随水蒸气挥发。下列说法正确的是
)是具有层状结构的晶体,硼酸层内的分子通过氢键相连(如图所示),硼酸溶解度随温度升高而增大,并能随水蒸气挥发。下列说法正确的是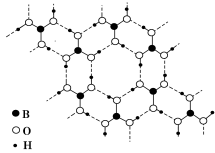
 键
键

