材料既是人类生活和生产的物质基础,又是人类认识自然和改造自然的工具。
(1)2020年11月,我国载人潜水器“奋斗者”号在马里亚纳海沟完成万米深潜。
①轻且坚固的球形载人舱由国产新型钛合金材料(Ti—6Al—3V)制造。高温条件下,可用Na和TiCl4反应制取Ti,其化学方程式为____ 。
②返航利器——固体浮力材料由纳米级大小的空心玻璃制造。玻璃中含有硅元素,硅在元素周期表中的位置为____ 。
(2)中国第一艘国产航母被命名为“中国人民解放军海军山东舰”。
①航母升降机可用铝镁合金制造。合金焊接前需用碱洗,即用NaOH溶液除去铝镁合金表面的自然氧化膜,碱洗时常有气泡冒出,其原因是____ (用离子方程式表示)。
②航母螺旋桨可用铜铝合金制造。80.0g铜铝合金用盐酸完全溶解后过滤,向滤液中加入适量NaOH溶液使沉淀量达到最大值,过滤得到白色沉淀39.0g,生成白色沉淀的离子方程式为____ ;合金中铝元素的质量分数为____ %(保留小数点后一位)。
(1)2020年11月,我国载人潜水器“奋斗者”号在马里亚纳海沟完成万米深潜。
①轻且坚固的球形载人舱由国产新型钛合金材料(Ti—6Al—3V)制造。高温条件下,可用Na和TiCl4反应制取Ti,其化学方程式为
②返航利器——固体浮力材料由纳米级大小的空心玻璃制造。玻璃中含有硅元素,硅在元素周期表中的位置为
(2)中国第一艘国产航母被命名为“中国人民解放军海军山东舰”。
①航母升降机可用铝镁合金制造。合金焊接前需用碱洗,即用NaOH溶液除去铝镁合金表面的自然氧化膜,碱洗时常有气泡冒出,其原因是
②航母螺旋桨可用铜铝合金制造。80.0g铜铝合金用盐酸完全溶解后过滤,向滤液中加入适量NaOH溶液使沉淀量达到最大值,过滤得到白色沉淀39.0g,生成白色沉淀的离子方程式为
更新时间:2022-03-02 10:15:45
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请回答:
(1)NH4Cl的电子式:___________ 。
(2)HClO的结构式:___________ 。
(3)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是___________ 。
(4)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为___________ 。
(5)金属铝和氢氧化钠溶液反应的化学方程式为___________ 。
(1)NH4Cl的电子式:
(2)HClO的结构式:
(3)已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w克R2-所含有电子的物质的量是
(4)二氧化硫可以用氯化铁溶液吸收,生成氯化亚铁和两种强酸,该反应的离子方程式为
(5)金属铝和氢氧化钠溶液反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】钠、铝和铁是三种重要的金属,回答问题:
(1)三种金属中,既能与盐酸反应又能与 溶液反应
溶液反应_________ (填化学式),写出它与 溶液反应的离子方程式
溶液反应的离子方程式_________________ 。
(2)三种金属在一定条件下均能与水发生反应。写出铁与水蒸气反应的化学方程式__________ 。取一小块金属钠放入滴有酚酞的水中,可观察到的实验现象是_______________ 。(填字母序号)。
①钠浮在水面迅速反应
②钠沉在水底迅速反应
③钠熔成小球并迅速游动
④反应中可以听到嘶嘶的响声
⑤反应后的溶液变为红色
A.①④⑤ B.②③④⑤ C.①③④⑤
(1)三种金属中,既能与盐酸反应又能与
 溶液反应
溶液反应 溶液反应的离子方程式
溶液反应的离子方程式(2)三种金属在一定条件下均能与水发生反应。写出铁与水蒸气反应的化学方程式
①钠浮在水面迅速反应
②钠沉在水底迅速反应
③钠熔成小球并迅速游动
④反应中可以听到嘶嘶的响声
⑤反应后的溶液变为红色
A.①④⑤ B.②③④⑤ C.①③④⑤
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据物质及其化合物的性质填空
Ⅰ为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末____ (填试剂化学式),
若观察到____________ 现象,就说明煤油中掺有水;也可向煤油样品中加入一小块金属钠,若观察到________ 现象,就可说明煤油中掺有水,反应的化学方程式是____________________ 。
Ⅱ镁着火不能用二氧化碳来灭火,理由是___________________________ (用化学方程式表示);
Ⅲ铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝离子的结构示意图是____________ 。
(2)铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的化学方程式:________ 。
(3)将7.8g过氧化钠投入500ml 1 mol·L-1氯化铝溶液中,可观察到的现象是________ 。
Ⅰ为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末
若观察到
Ⅱ镁着火不能用二氧化碳来灭火,理由是
Ⅲ铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝离子的结构示意图是
(2)铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的化学方程式:
(3)将7.8g过氧化钠投入500ml 1 mol·L-1氯化铝溶液中,可观察到的现象是
| A.放出无色无味的气体,生成大量白色沉淀 |
| B.放出无色无味的气体,生成白色沉淀后恰好溶解 |
| C.放出无色无味的气体,生成白色沉淀后部分溶解 |
| D.无任何现象 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】镁和铝的碱式碳酸盐是中和胃酸药物的主要成分。欲测定某种镁和铝的碱式碳酸盐的成分进行了以下实验,根据以下实验记录,回答下列问题:
(1)称取6.02g该碱式碳酸盐,加入4.0mol/L盐酸使其溶解,当加入42.5mL时开始产生CO2 ,当加入盐酸至45.0mL时恰好完全溶解,该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=________ ;
(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,试计算确定该碱式碳酸盐的化学式________ 。
(1)称取6.02g该碱式碳酸盐,加入4.0mol/L盐酸使其溶解,当加入42.5mL时开始产生CO2 ,当加入盐酸至45.0mL时恰好完全溶解,该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=
(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,试计算确定该碱式碳酸盐的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】无水AlCl3易升华,可用作有机合成的催化剂等,工业上由铝土矿(主要成分是Al2O3和Fe2O3,还含有少量的SiO2 )和石油焦(主要成分是C)为原料制备无水AlCl3:2Al2O3+6Cl2=4AlCl3+3O2
回答以下问题:
(1)加入焦炭后的化学反应可表示为Al2O3+C+Cl2 AlCl3+X↑,设计实验确定气体X的成分:
AlCl3+X↑,设计实验确定气体X的成分:__________ 。
(2)在提纯AlCl3粗产品时,需加入少量铝粉,可使熔点较低的FeCl3转化为熔点较高的FeCl2,从而避免在AlCl3中混入铁的氯化物。该反应的化学方程式为____________________ 。
(3)为测定制得的无水AlCl3产品(含FeCl3杂质)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①过程涉及的离子方程式___________________ 、_______________ 。
②AlCl3产品的纯度为__________________________________ 。
回答以下问题:
(1)加入焦炭后的化学反应可表示为Al2O3+C+Cl2
 AlCl3+X↑,设计实验确定气体X的成分:
AlCl3+X↑,设计实验确定气体X的成分:(2)在提纯AlCl3粗产品时,需加入少量铝粉,可使熔点较低的FeCl3转化为熔点较高的FeCl2,从而避免在AlCl3中混入铁的氯化物。该反应的化学方程式为
(3)为测定制得的无水AlCl3产品(含FeCl3杂质)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
①过程涉及的离子方程式
②AlCl3产品的纯度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】写出下列反应的离子方程式。
(1)足量二氧化碳通入氢氧化钠溶液反应_________________________________ 。
(2)AlCl3溶液和过量NaOH溶液反应____________________________________ 。
(3)Na[Al(OH)4]与少量盐酸反应___________________________________________ 。
(4)NH4HCO3溶液与少量NaOH溶液反应____________________________________ 。
(5)足量Fe与稀硝酸反应_________________________________ 。
(6)Fe(OH)3与HI溶液反应________________________________________________ 。
(7)Ca(OH)2溶液与足量NaHCO3溶液反应___________________________________ 。
(8)NaHSO4溶液与Ba(OH)2溶液反应:
①加Ba(OH)2溶液至 恰好沉淀完全
恰好沉淀完全______________________________________ 。
②加Ba(OH)2溶液至溶液呈中性_____________________________________________ 。
(9)KAl(SO4)2溶液与少量Ba(OH)2溶液反应___________________________________ 。
(10)FeBr2溶液与Cl2反应,n(FeBr2)∶n(Cl2)=1∶1:___________________________ 。
(1)足量二氧化碳通入氢氧化钠溶液反应
(2)AlCl3溶液和过量NaOH溶液反应
(3)Na[Al(OH)4]与少量盐酸反应
(4)NH4HCO3溶液与少量NaOH溶液反应
(5)足量Fe与稀硝酸反应
(6)Fe(OH)3与HI溶液反应
(7)Ca(OH)2溶液与足量NaHCO3溶液反应
(8)NaHSO4溶液与Ba(OH)2溶液反应:
①加Ba(OH)2溶液至
 恰好沉淀完全
恰好沉淀完全②加Ba(OH)2溶液至溶液呈中性
(9)KAl(SO4)2溶液与少量Ba(OH)2溶液反应
(10)FeBr2溶液与Cl2反应,n(FeBr2)∶n(Cl2)=1∶1:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】元素周期表和元素周期律是学习化学的重要工具,可以帮助我们推测元素及其化合物的结构和性质,对工农业生产具有一定的指导意义。下表是元素周期表的部分片段(2、3周期)
(1)9种元素中,原子半径最小的是______ ,化学性质最不活泼的是____ 。
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是_______ 。
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:______ 和______ 。
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式_______________ 。
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
请你根据上表得出实验结论:_________ ;若比较⑥与⑧的单质的活泼性,请写出实验方案___________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑤ | ⑦ | |||||
| 3 | ① | ② | ③ | ⑥ | ⑧ | ⑨ |
(1)9种元素中,原子半径最小的是
(2)⑥、⑧的最高价氧化物对应的水化物的酸性较强的是
(3)④元素形成的多种同素异形体,有广泛的用途。请写出其中任意两种同素异形体的名称:
(4)写出③的最高价氧化物对应的水化物分别与①、⑤的最高价氧化物对应的水化物反应的化学方程式
(5)某同学做同周期元素金属性递变规律实验时,设什了如下实验并记录了有关实验现象。
| 实验步骤 | 实验现象 |
| A、将一小块单质①放入滴有酚酞溶液的冷水中 | 剧烈反应,①浮于水面上,熔成小球,四处游动,发出“嘶嘶”声.随之消失,溶液变成红色 |
| B、将单质②投入冷水中,观察现象,再将水加热 | 开始无现象,加热后有气体产生 |
| C.将单质②投入稀盐酸中 | 迅速产生大量无色气体 |
| D.将单质③投入稀盐酸中 | 反应不十分剧烈,产生无色气体 |
请你根据上表得出实验结论:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,回答下列问题:
(1)①④⑥三种元素构成的化合物的电子式:__ ;⑨的最高价氧化物对应水化物的化学式:__ 。
(2)⑤、⑦、⑧的简单离子半径由大到小的顺序:__ (用离子符号填写)。
(3)用一个化学方程式表示④、⑤二种元素非金属性的强弱__ 。
(4)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的离子方程式为__ 。
(5)元素①、元素④以原子个数比为1∶1形成化合物Q,元素①、元素③形成化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终产物对空气没有污染,写出该反应的化学方程式:__ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)①④⑥三种元素构成的化合物的电子式:
(2)⑤、⑦、⑧的简单离子半径由大到小的顺序:
(3)用一个化学方程式表示④、⑤二种元素非金属性的强弱
(4)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的离子方程式为
(5)元素①、元素④以原子个数比为1∶1形成化合物Q,元素①、元素③形成化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终产物对空气没有污染,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】部分短周期元素的原子半径与元素的最高价及最低价的关系如图所示。
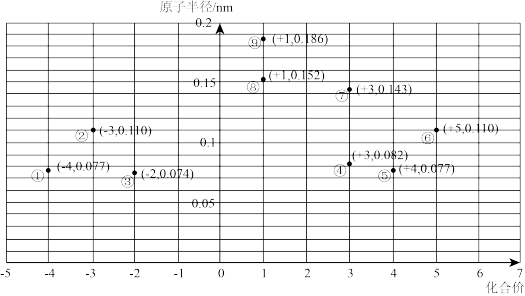
请填写下列空白:
(1)图中涉及________ 种元素,其中元素________ (用化学用语表示,下同 )的金属性最强。
(2)元素①的最简单氢化物的电子式为________ ;元素②的原子结构示意图为________ 。
(3)元素③和⑨对应的单质加热条件下反应的方程式为________________ 。
(4)元素④在周期表中的位置是________________ ;元素⑤、⑥对应的最高价氧化物的水化物酸性强弱关系为________ ;元素⑦和元素⑧两者核电荷数之差是________ 。

请填写下列空白:
(1)图中涉及
(2)元素①的最简单氢化物的电子式为
(3)元素③和⑨对应的单质加热条件下反应的方程式为
(4)元素④在周期表中的位置是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】FeCl3 具有净水作用,而高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,处理污水比FeCl3 高效。请回答下列问题:(已知25℃,Ksp[Fe(OH)3]=4.0×10-38,lg2=0.3)
(1)FeCl3净水的原理是________________ (用离子方程式表示),Fe3+水解生成的Fe(OH)3 胶体粒子能吸附水中的悬浮杂质,常温下此水解反应的平衡常数为_____________ (填写数值)。
(2)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入____________ ,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=________ 。
(3)工业上由CuCl2·2H2O晶体制备无水CuCl2的合理方法是在HCl气氛中加热,若在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是_________________________ (用化学方程式表示)。
(4)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下①取0.36 g试样溶于水,加入过量KI固体,发生反应2Cu2++4I-===2CuI↓+I2,生成白色沉淀。②用0.100 0 mol·L-1Na2S2O3标准溶液滴定生成的I2,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。(已知:I2+2S2O32-===S4O62-+2I-)
①滴定过程可选用________ 作指示剂,滴定终点时的现象是_______________________ 。
②该试样中CuCl2·2H2O的质量分数为________ 。
(1)FeCl3净水的原理是
(2)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入
(3)工业上由CuCl2·2H2O晶体制备无水CuCl2的合理方法是在HCl气氛中加热,若在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是
(4)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下①取0.36 g试样溶于水,加入过量KI固体,发生反应2Cu2++4I-===2CuI↓+I2,生成白色沉淀。②用0.100 0 mol·L-1Na2S2O3标准溶液滴定生成的I2,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。(已知:I2+2S2O32-===S4O62-+2I-)
①滴定过程可选用
②该试样中CuCl2·2H2O的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】胆矾( ,相对分子质量为250)广泛应用于生产生活中。
,相对分子质量为250)广泛应用于生产生活中。
(1)农药波尔多液由胆矾和石灰乳等配制而成。不能用铁桶来配制波尔多液,其原因是_______ 。
(2)将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。
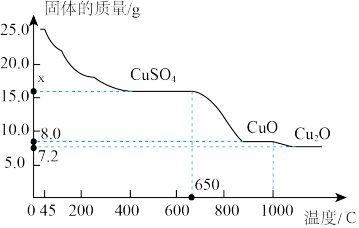
①加热至_______ ℃时, 开始分解。
开始分解。
②加热至1000℃时,CuO开始分解,生成 与一种能使带火星的木条复燃的气体,该气体为
与一种能使带火星的木条复燃的气体,该气体为_______ 。CuO完全分解时产生该气体的质量为_______ g(写出计算过程)
③计算图中x的值(写出计算过程)_______
④等质量下列炼铜原料。理论上,冶炼后得到铜最多的是_______ (填字母序号)。
A. B.
B. C.
C. D.
D.
 ,相对分子质量为250)广泛应用于生产生活中。
,相对分子质量为250)广泛应用于生产生活中。(1)农药波尔多液由胆矾和石灰乳等配制而成。不能用铁桶来配制波尔多液,其原因是
(2)将25.0g胆矾放在坩埚内加热,固体质量与成分随温度变化的曲线如图。

①加热至
 开始分解。
开始分解。②加热至1000℃时,CuO开始分解,生成
 与一种能使带火星的木条复燃的气体,该气体为
与一种能使带火星的木条复燃的气体,该气体为③计算图中x的值(写出计算过程)
④等质量下列炼铜原料。理论上,冶炼后得到铜最多的是
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次



