除了用手触摸和温度计测量外还可以借助其他方法感知温度的变化,如在探究化学反应过程中有热量变化时,某兴趣小组设计了如下三套装置:
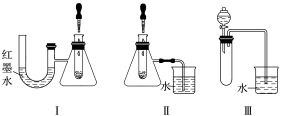
(1)该小组选择装置Ⅰ探究Na2O2和H2O反应为放热反应,将水滴入盛有过氧化钠的试管中,现象为___________ ,化学方程式:___________ 。
(2)该小组采用装置Ⅱ,探究硝酸铵溶于水的能量变化,当向盛有硝酸铵固体的试管中滴入少量水,发现导管中形成一段水柱,则该变化___________ (填“是”或“不是”)吸热反应,原因为___________ 。
(3)该小组在探究镁和盐酸反应热量变化时,选择了装置Ⅲ,发现反应过程中,导管口有气泡冒出该装置___________ (填“能”或“不能”)证明镁和盐酸反应为放热反应,原因为___________ 。

(1)该小组选择装置Ⅰ探究Na2O2和H2O反应为放热反应,将水滴入盛有过氧化钠的试管中,现象为
(2)该小组采用装置Ⅱ,探究硝酸铵溶于水的能量变化,当向盛有硝酸铵固体的试管中滴入少量水,发现导管中形成一段水柱,则该变化
(3)该小组在探究镁和盐酸反应热量变化时,选择了装置Ⅲ,发现反应过程中,导管口有气泡冒出该装置
更新时间:2022-03-02 20:09:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】过氧化钠在呼吸面具或潜水艇中作为__________ 的来源,其化学反应方程式为________________ ;红热的铁跟水蒸气反应,反应的化学方程式为_______________ .
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制钠的工业方法,其反应原理是:2NaCl(熔融) 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:
(1)下列各项中属于保存金属钠的正确方法是_______。
(2)钠长时间放在空气中,最后的产物主要成分是_______。
(3)将一小块钠放在水平放置的试管中部,用酒精灯加热充分反应,产物的颜色为_______ 。将该试管冷却后直立,滴加几滴水,发生反应的离子方程式为_______ ,检验该反应产生的气体的方法是_______ 。
 2Na+Cl2↑。回答下列有关单质钠的问题:
2Na+Cl2↑。回答下列有关单质钠的问题:(1)下列各项中属于保存金属钠的正确方法是_______。
| A.放在棕色瓶中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
| A.Na2O | B.Na2O2 | C.NaOH | D.Na2CO3 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】A、B、C、D、E五种物质的焰色反应都呈黄色,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,B与水反应放出的气体具有氧化性,同时都生成溶液C,C与适量的CO2反应生成D,与过量的CO2反应生成E,E加热能生成D。试推断:
A__________ ,B__________ ,C__________ ,D__________ ,E__________ (写化学式),并写出有关反应的化学方程式:
A和水:____________________________________
B和水:_____________________________________
C和少量的CO2:______________________________
C和过量的CO2:______________________________
E受热分解:__________________________________
A
A和水:
B和水:
C和少量的CO2:
C和过量的CO2:
E受热分解:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在一个小烧杯里加入 20 g Ba(OH)2·8H2O晶体,将小烧杯放在事先已滴有3~4滴水的玻璃片上。然后加入10 g NH4Cl晶体,并用玻璃棒迅速搅拌。
(1)实验中观察到的现象有_______ 、_______ 和反应混合物呈糊状。反应呈糊状的原因是_______ 。
(2)通过_______ 现象,说明该反应为_______ (填“吸”或“放”)热反应,这是由于反应物的总能量_______ (填“高”或“低”)于生成物的总能量。
(3)写出这个反应的化学方程式_______
(1)实验中观察到的现象有
(2)通过
(3)写出这个反应的化学方程式
您最近一年使用:0次
【推荐2】化学反应存在能量变化的原因
从微观讲,旧化学键断裂,需要_______ 能量,新化学键的形成,需要_______ 能量(主要原因)。从宏观讲,生成物的总能量和反应物的能量_______ 同,如果生成物的总能量低于反应物的总能量,反应需要向外界_______ 热,反之,需要_______ 热。即①放热反应可以看成是反应物所具有的_______ 能转化为_______ 能释放出来。②吸热反应可以看成是_______ 能转化为_______ 能被生成物所“储存”。
从微观讲,旧化学键断裂,需要
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】热力学温度,又称开尔文温标,简称开氏温标,是国际单位制七个基本物理量之一。开尔文(LordKelvin)被称为热力学之父,他将第一和第二热力学定律公式化。
(1)下列关于反应ΔU的说法中,正确的是_____。
(2)下列关于内能和内能变化的叙述正确的是_____。
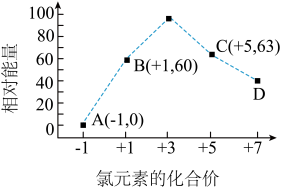
(3)一定条件,在水溶液中1molCl-、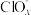 (x=1,2,3,4)的能量(KJ)相对大小如图所示,则D是
(x=1,2,3,4)的能量(KJ)相对大小如图所示,则D是_____ (填离子符号)。B=A+C反应的热化学方程式为(用离子方程表示):_____ 。
(1)下列关于反应ΔU的说法中,正确的是_____。
| A.ΔU>0时,反应放出能量 |
| B.ΔU<0时,反应放出能量 |
| C.ΔU=Q |
| D.ΔU=ΔH |
| A.内能是体系内物质所含的能量总和 |
| B.内能只与物质的种类、数量以及聚集状态有关 |
| C.系统的内能可以通过实验测得 |
| D.内能变化就是反应热 |
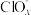 (x=1,2,3,4)的能量(KJ)相对大小如图所示,则D是
(x=1,2,3,4)的能量(KJ)相对大小如图所示,则D是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氮氧化物(NOx)是硝酸工业和汽车尾气产生的主要污染物之一,通过气体传感器可以测定其含量。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g) N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是_________ (填“放热反应”或“吸热反应”),反应中断开反应物中化学键吸收的总能量_________ (填“大于”或“小于”)形成生成物中化学键放出的总能量。

(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=_________ 。
②该条件下,NO的平衡转化率为_________ 。
③下列有关上述反应的说法正确的是_________ (填字母)。
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。
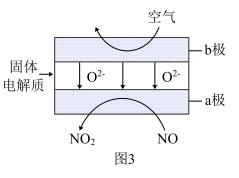
①a极是_________ (填“负极”或“正极”),发生的是_________ 反应(填“氧化”或“还原”)。
②工作时,a极的电极反应式是_________ 。
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是_________ 。
(1)利用催化技术可将汽车尾气中的NO、CO转化为无污染的CO2和N2,反应的化学方程催化剂式为2NO(g)+2CO(g)
 N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
N2(g)+2CO2(g)。该反应过程中的能量变化如图1所示,则该反应是
(2)为了测定汽车尾气催化转化反应的反应速率,某温度下在恒容密闭容器中用气体传感器测得不同时间时NO浓度的变化如图2所示。

①0~2s内的平均反应速率v(CO2)=
②该条件下,NO的平衡转化率为
③下列有关上述反应的说法正确的是
A.断裂N≡N键与形成C=O键数目之比为1∶2时,该反应达到平衡
B.消耗2molNO(g)的同时生成2molCO(g)时,该反应达到平衡
C.其他条件不变,缩小容器的体积,反应速率加快
(3)通过NO传感器可监测NO的含量,其工作原理如图3所示。

①a极是
②工作时,a极的电极反应式是
③每消耗标准状况下4.48LNO,理论上外电路中通过电子的物质的量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】一定条件下,1mol气态H2与1mol气态Br2断键时分别需要吸收436kJ和193kJ的热量,而1mol气态HBr成键时会放出366kJ的热量。据此推算,当1mol气态H2发生如下反应:H2(g)+Br2(g)=2HBr(g),_______ (填“放出”或“吸收”)_______ kJ的热量。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】化学反应中伴随着能量的变化。
(1)下列变化中属于吸热反应的是____ (填字母)。
①液态水汽化 ②Ba(OH)2•8H2O与NH4Cl两固体混合 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
a.①② b.②④ c.③ d.①⑥
(2)工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。已知拆开1mol化学键所需要的能量叫键能。相关键能数据如表:
结合表中所给信息,计算生成2molNH3时___ (填“吸收”或“放出”)的热量是___ kJ。
(3)潜艇中使用的液氨液氧燃料电池工作原理如图所示:
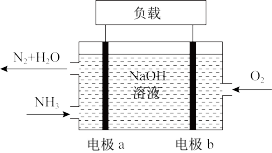
电极a名称是____ (填“正极”或“负极”),其电极反应为___ ,电解质溶液中OH-离子向____ 移动(填“电极a”或“电极b”)。
(1)下列变化中属于吸热反应的是
①液态水汽化 ②Ba(OH)2•8H2O与NH4Cl两固体混合 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华
a.①② b.②④ c.③ d.①⑥
(2)工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。已知拆开1mol化学键所需要的能量叫键能。相关键能数据如表:
| 共价键 | H—H | N≡N | N—H |
| 键能(kJ/mol) | 436 | 945 | 391 |
结合表中所给信息,计算生成2molNH3时
(3)潜艇中使用的液氨液氧燃料电池工作原理如图所示:

电极a名称是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铜是生命必要的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。在化学反应中,铜元素可表现为0、+1、+2。
(1)在西汉古籍中曾有记载:曾青得铁则化为铜〔即曾青(CuSO4 )跟铁反应生成铜〕,试写出该反应的离子方程式:________________ 。
(2)尽管铜比铁较为稳定,但铜器表面经常会生成铜锈[即:铜绿,化学式Cu2(OH)2CO3 ],其中生成铜绿的反应物除铜外还有O2 、CO2 和H2O。试写出保护铜制品的方法:________________________ 。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1183.4 ℃,铁的熔点是1534.8 ℃,________________________________ 。
(1)在西汉古籍中曾有记载:曾青得铁则化为铜〔即曾青(CuSO4 )跟铁反应生成铜〕,试写出该反应的离子方程式:
(2)尽管铜比铁较为稳定,但铜器表面经常会生成铜锈[即:铜绿,化学式Cu2(OH)2CO3 ],其中生成铜绿的反应物除铜外还有O2 、CO2 和H2O。试写出保护铜制品的方法:
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1183.4 ℃,铁的熔点是1534.8 ℃,
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某课外活动小组为了研究“干燥的CO2不能与Na2O2反应”和“CO2在有水存在时才能与Na2O2反应”,设计了如下实验装置:

(1)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,加热铜丝,目的是_________ ,X是_________ 。实验观察到铜丝未变化,则得出结论_________ 。
(2)若打开K2,关闭K1,出现_________ 现象可证明有水时CO2与Na2O2反应产生了O2。
(3)根据以上的实验结论,写出生成O2及O2与Cu反应的化学方程式:_________ ,_________ 。

(1)如图装置,在干燥管中装入Na2O2后,打开活塞加入稀硫酸,生成CO2。打开K1,关闭K2,加热铜丝,目的是
(2)若打开K2,关闭K1,出现
(3)根据以上的实验结论,写出生成O2及O2与Cu反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】(1)一种变色眼镜的镜片和普通照相感光胶片中含有卤化银.镜片变化是因 为卤化银在光的作用下发生化学反应,其反应式是_______ ,照相感光胶片曝光的化学反应是_______ .
(2)在我国干旱严重的华北地区,近年来利用飞机、高炮或火箭等运载工具向过冷支层中播撒碘化银(AgI)或干冰,实现人工增雨(或人工增雪),达到减灾的目的.下列有关人工增雨的评述中,你认为不甚理智的是_______ .
A.它对农业生产条件和大气环境的改善有一定的效益
B.它使用的碘化银中的重金属元素对土壤造成污染
C.它使用的 AgI 如换成干冰,可避免重金属元素对土壤的污染
D.它是人类彻底战胜自然的表现,体现了人类的力量是无穷的.
(2)在我国干旱严重的华北地区,近年来利用飞机、高炮或火箭等运载工具向过冷支层中播撒碘化银(AgI)或干冰,实现人工增雨(或人工增雪),达到减灾的目的.下列有关人工增雨的评述中,你认为不甚理智的是
A.它对农业生产条件和大气环境的改善有一定的效益
B.它使用的碘化银中的重金属元素对土壤造成污染
C.它使用的 AgI 如换成干冰,可避免重金属元素对土壤的污染
D.它是人类彻底战胜自然的表现,体现了人类的力量是无穷的.
您最近一年使用:0次



