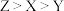下列叙述正确的是
| A.第一电离能:Li<Na<K |
B. 、 、 、 、 均为酸性氧化物 均为酸性氧化物 |
C.通过比较酸性 ,判断硫与碳的非金属性强弱 ,判断硫与碳的非金属性强弱 |
| D.第三周期主族元素,离子半径随原子序数的增大而减小 |
更新时间:2022-03-04 11:33:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知对角线规则为:沿周期表中金属与非金属分界线方向对角的两主族元素性质相似,如Li与Mg,Be与Al,B和Si相似,则下列叙述中不正确的是
| A.BeO为两性氧化物 | B.Li在空气中的燃烧产物为Li2O |
| C.H3BO3是一种强酸 | D.Be能和强碱溶液反应产生H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
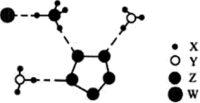
【推荐2】如图所示X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示。若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是


| A.X 、Y对应的氧化物都是酸性氧化物 |
| B.X的氧化物不能与Mg发生化学反应 |
| C.Z比Y更容易与氢气化合 |
| D.W与X形成的化合物中化学键类型为共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对Na、Mg、Al的有关性质的叙述正确的是
| A.碱性:NaOH<Mg(OH)2<Al(OH)3 | B.半径:Na>Mg>Al |
| C.电负性:Na>Mg>Al | D.第一电离能:Na<Mg<Al |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列物质性质递变规律正确的是
| A.Na、K、Cs的熔点依次升高 |
| B.HCl、H2S、PH3的稳定性依次减弱 |
| C.H2CO3、H2SiO3、H2SO4的酸性依次增强 |
| D.单晶硅、CsCl、干冰的熔点依次升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其电子层数的2倍,Y的原子半径是所在周期中除稀有气体外最大的,Z是地壳中含量最高的金属元素,W的最高正价和最低负价的代数和为6。下列说法正确的是
| A.原子半径的大小顺序:r(W)>r(Z)>r(X) |
| B.X位于周期表的第3周期,ⅥA族 |
| C.Y的最高价氧化物对应水化物的碱性比Z的强 |
| D.W的氧化物对应水化物一定为强酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期主族元素X、Y、Z和W的原子序数依次增大,X、Y、W位于不同周期,Y、Z、W的原子最外层电子数之和为14,Z的原子半径在短周期主族元素中最大。下列说法错误的是
| A.简单离子半径:W>Z>X |
| B.Y、W均能与X形成共价化合物 |
| C.W的最高价氧化物的水化物一定为强酸 |
| D.Y与Z形成的化合物溶于水一定得到强碱溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
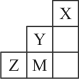
【推荐1】元素周期表前四周期元素的一部分如图所示,X、Y、Z、M均为主族元素,其中M元素原子的最外层电子数为其次外层电子数的 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
A.第一电离能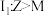 |
B.电负性: |
C.离子半径: |
D.M元素基态原子的简化电子排布式: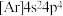 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知前四周期元素X、Y、Q、R、Z和W在周期表中的位置如图所示,其中Z位于ds区,基态W原子的价电子中在不同形状的原子轨道中运动的电子数相等。下列说法正确的是
| X | Y | |||
| Q | R | |||
| Z | W |
| A.最高正化合价:X=Q<Y=R |
| B.基态Z原子的价电子排布为3d104s1 |
| C.X和Q的第一电离能都高于同周期相邻元素 |
| D.R最高价氧化物的水化物不能与其最低价氢化物反应 |
您最近一年使用:0次




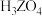
 溶液对应的pH(25℃)
溶液对应的pH(25℃)