甲酸铜[(HCOO)2Cu]在工业生产中有广泛的用途,某工业甲酸铜纯度测定如下:
Ⅰ.准确称取0.1540g样品于锥形瓶中,加入10mL蒸馏水溶解,滴加1mol·L-1H2SO4,配制成pH≤3的溶液;
Ⅱ.加5mL20%碘化钾溶液(过量),用浓度为0.1932mol·L-1的Na2S2O3标准溶液滴定至溶液呈浅黄色,再加入2mL0.5%淀粉溶液;
Ⅲ.继续滴定到溶液变成浅蓝色,加入5mL10%KSCN溶液,振荡,溶液蓝色加深;
Ⅳ.继续滴定至终点,共消耗5.00mL标准溶液。
已知:①Cu2++I-→CuI↓+I2;I2+S2O →I-+S4O
→I-+S4O ,I2+I-
,I2+I- I
I (方程式未配平);
(方程式未配平);
②CuI可吸附I ,[Ksp(CuI)=1.1×10-10,Ksp(CuSCN)=1.1×10-14];
,[Ksp(CuI)=1.1×10-10,Ksp(CuSCN)=1.1×10-14];
③样品中的杂质不参与任何反应。
回答下列问题:
(1)准确称取0.1540g样品应选用____ (填序号)。
A.托盘天平 B.分析天平(精确度:0.01g) C.分析天平(精确度:0.0001g)
(2)滴定时用____ (填“酸式”或“碱式”)滴定管装标准溶液。
(3)步骤Ⅰ加硫酸调节溶液pH≤3的目的是____ 。
(4)滴定终点的实验现象是____ 。
(5)步骤Ⅲ中加入5mL10%KSCN溶液的目的是____ 。
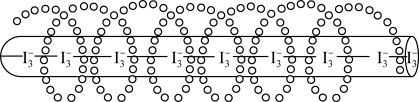
(6)淀粉溶液和碘单质显色原理:I 钻入淀粉螺旋隧道中(如图)。若实验一开始就加入淀粉溶液会使滴定终点滞后,导致实验结果
钻入淀粉螺旋隧道中(如图)。若实验一开始就加入淀粉溶液会使滴定终点滞后,导致实验结果____ (填“偏大”“偏小”或“无影响”)。
(7)样品的纯度为____ %。
(8)在上述方案基础上,下列措施能进一步提高准确度的有____ (填序号)。
Ⅰ.准确称取0.1540g样品于锥形瓶中,加入10mL蒸馏水溶解,滴加1mol·L-1H2SO4,配制成pH≤3的溶液;
Ⅱ.加5mL20%碘化钾溶液(过量),用浓度为0.1932mol·L-1的Na2S2O3标准溶液滴定至溶液呈浅黄色,再加入2mL0.5%淀粉溶液;
Ⅲ.继续滴定到溶液变成浅蓝色,加入5mL10%KSCN溶液,振荡,溶液蓝色加深;
Ⅳ.继续滴定至终点,共消耗5.00mL标准溶液。
已知:①Cu2++I-→CuI↓+I2;I2+S2O
 →I-+S4O
→I-+S4O ,I2+I-
,I2+I- I
I (方程式未配平);
(方程式未配平);②CuI可吸附I
 ,[Ksp(CuI)=1.1×10-10,Ksp(CuSCN)=1.1×10-14];
,[Ksp(CuI)=1.1×10-10,Ksp(CuSCN)=1.1×10-14];③样品中的杂质不参与任何反应。
回答下列问题:
(1)准确称取0.1540g样品应选用
A.托盘天平 B.分析天平(精确度:0.01g) C.分析天平(精确度:0.0001g)
(2)滴定时用
(3)步骤Ⅰ加硫酸调节溶液pH≤3的目的是
(4)滴定终点的实验现象是
(5)步骤Ⅲ中加入5mL10%KSCN溶液的目的是
(6)淀粉溶液和碘单质显色原理:I
 钻入淀粉螺旋隧道中(如图)。若实验一开始就加入淀粉溶液会使滴定终点滞后,导致实验结果
钻入淀粉螺旋隧道中(如图)。若实验一开始就加入淀粉溶液会使滴定终点滞后,导致实验结果
(7)样品的纯度为
(8)在上述方案基础上,下列措施能进一步提高准确度的有
| A.适当提高称量样品的质量 |
| B.用硝酸代替硫酸 |
| C.进行平行实验 |
| D.将标准溶液稀释至更低的浓度 |
更新时间:2022/03/07 21:20:18
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】某小组通过实验验证Ag++Fe2+ Fe3++Ag↓为可逆反应并测定其平衡常数。
Fe3++Ag↓为可逆反应并测定其平衡常数。
(1)实验验证Ag++Fe2+ Fe3++Ag↓为可逆反应。
Fe3++Ag↓为可逆反应。
实验I:将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀。
实验II:向少量Ag粉中加入0.0100mol·L-1Fe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,灰黑色固体溶解,产生红棕色气体,证实沉淀为_______ 。综合。上述实验,证实Ag++Fe2+ Fe3++Ag↓为可逆反应。
Fe3++Ag↓为可逆反应。
②小组成员结合实验结论提出FeCl3溶液也可以溶解Ag单质,你认为是否合理?_______ (填“是”或“否”);并解释原因:_______ 。
(2)测定平衡常数
实验III:一定温度下,待实验I中反应达到平衡状态时,取vmL上层清液,用clmol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时,消耗KSCN标准溶液v1mL。
资料:Ag++SCN- AgSCN(白色) K=1012
AgSCN(白色) K=1012
Fe3++SCN- [FeSCN]2+(红色) K=1023
[FeSCN]2+(红色) K=1023
①滴定过程中Fe3+的作用是_______ 。
②测得平衡常数K=_______ 。
(3)思考并回答问题:
①不用实验II中清液测定K的原因是_______ 。
②取实验I的浊液测定c(Ag+),消耗KSCN标准溶液的体积_______ (填“偏大”、“偏小”或“不受影响”。
 Fe3++Ag↓为可逆反应并测定其平衡常数。
Fe3++Ag↓为可逆反应并测定其平衡常数。(1)实验验证Ag++Fe2+
 Fe3++Ag↓为可逆反应。
Fe3++Ag↓为可逆反应。实验I:将0.0100mol·L-1Ag2SO4溶液与0.0400mol·L-1FeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀。
实验II:向少量Ag粉中加入0.0100mol·L-1Fe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,灰黑色固体溶解,产生红棕色气体,证实沉淀为
 Fe3++Ag↓为可逆反应。
Fe3++Ag↓为可逆反应。②小组成员结合实验结论提出FeCl3溶液也可以溶解Ag单质,你认为是否合理?
(2)测定平衡常数
实验III:一定温度下,待实验I中反应达到平衡状态时,取vmL上层清液,用clmol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时,消耗KSCN标准溶液v1mL。
资料:Ag++SCN-
 AgSCN(白色) K=1012
AgSCN(白色) K=1012Fe3++SCN-
 [FeSCN]2+(红色) K=1023
[FeSCN]2+(红色) K=1023①滴定过程中Fe3+的作用是
②测得平衡常数K=
(3)思考并回答问题:
①不用实验II中清液测定K的原因是
②取实验I的浊液测定c(Ag+),消耗KSCN标准溶液的体积
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
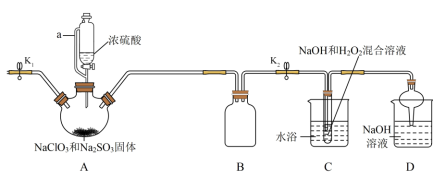
【推荐2】NaClO2在工业生产中常用作漂白剂、脱色剂、消毒剂、拔染剂等。实验室中可用H2O2和NaOH混合溶液吸收ClO2的方法制取NaClO2,利用如下装置及试剂制备NaClO2晶体:
已知:①NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
②ClO2气体浓度较大时易发生爆炸。___________ 。装置D中NaOH溶液的作用是___________ 。
(2)装置A中生成ClO2的化学方程式为___________ 。
(3)仪器A中NaClO3需稍微过量,原因是___________ 。实验过程中,常需要打开K1,鼓入一定量空气,该操作的目的是___________ 。
(4)NaClO2纯度的测定:“间接碘量法”测定样品(杂质与I−不发生反应)纯度,过程如下:
取样品1.810g配制成250mL溶液,从中取出25.00mL;加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液(已知:ClO +4I−+4H+=2H2O+2I2+Cl−),然后用cmol·L−1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O
+4I−+4H+=2H2O+2I2+Cl−),然后用cmol·L−1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
样品中NaClO2的纯度为___________ %(用含c、V的代数式表示)。
已知:①NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
②ClO2气体浓度较大时易发生爆炸。
(2)装置A中生成ClO2的化学方程式为
(3)仪器A中NaClO3需稍微过量,原因是
(4)NaClO2纯度的测定:“间接碘量法”测定样品(杂质与I−不发生反应)纯度,过程如下:
取样品1.810g配制成250mL溶液,从中取出25.00mL;加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液(已知:ClO
 +4I−+4H+=2H2O+2I2+Cl−),然后用cmol·L−1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O
+4I−+4H+=2H2O+2I2+Cl−),然后用cmol·L−1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O =S4O
=S4O +2I-)。
+2I-)。样品中NaClO2的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某兴趣小组利用摩尔盐( )制备三草酸合铁酸钾(
)制备三草酸合铁酸钾( )晶体。
)晶体。
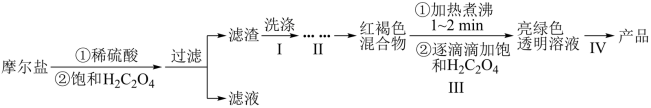
操作Ⅱ:
①饱和
②恒温40℃,逐滴滴加6%
已知: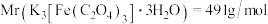
请回答下列问题:
(1)操作Ⅰ中应选择以下何种洗涤剂___________ 。
A.冷水 B.热水 C.浓盐酸 D.乙醇
(2)操作Ⅱ、Ⅲ均生成了三草酸合铁酸钾,该过程的化学反应方程式依次为:___________ ; 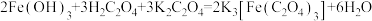 。
。
(3)下列操作或描述正确的是___________ 。
A.操作Ⅲ中煮沸时间不宜过长,否则会使生成的 沉淀颗粒较粗,使后续酸溶速度慢,时间增长
沉淀颗粒较粗,使后续酸溶速度慢,时间增长
B.向亮绿色溶液中滴加酸性高锰酸钾溶液,若紫红色褪去,则溶液中包含
C.操作Ⅳ包含蒸发结晶、过滤、洗涤、烘干等若干步骤
D.获得的产品应保存在阴暗避光、低温的环境
(4)科研人员在研究过程中发现,不同的实验条件对产物的产率有如下影响。
结合表中信息分析,该制备试验中合适的条件是___________ 。并简述控制该pH范围的原因___________ 。
(5)准确称取已制备晶体8.500g溶于水中,加水定容至250mL,取试样溶液25.00mL于锥形瓶中,用0.1000mol/L 溶液滴定,消耗
溶液滴定,消耗 标准液20.00mL,则该产品的纯度是
标准液20.00mL,则该产品的纯度是___________ 。
 )制备三草酸合铁酸钾(
)制备三草酸合铁酸钾( )晶体。
)晶体。
操作Ⅱ:
①饱和

②恒温40℃,逐滴滴加6%

已知:
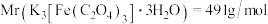
| 物质 | 性质 |
 | 见光易分解,强酸性环境下不稳定;易溶于水,难溶于乙醇。 |
 | 溶解性:冷水为0.22/100g,热水为0.026g/100g; 能溶于冷浓盐酸;难溶于稀硫酸、乙醇。 |
(1)操作Ⅰ中应选择以下何种洗涤剂
A.冷水 B.热水 C.浓盐酸 D.乙醇
(2)操作Ⅱ、Ⅲ均生成了三草酸合铁酸钾,该过程的化学反应方程式依次为:
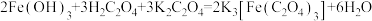 。
。(3)下列操作或描述正确的是
A.操作Ⅲ中煮沸时间不宜过长,否则会使生成的
 沉淀颗粒较粗,使后续酸溶速度慢,时间增长
沉淀颗粒较粗,使后续酸溶速度慢,时间增长B.向亮绿色溶液中滴加酸性高锰酸钾溶液,若紫红色褪去,则溶液中包含

C.操作Ⅳ包含蒸发结晶、过滤、洗涤、烘干等若干步骤
D.获得的产品应保存在阴暗避光、低温的环境
(4)科研人员在研究过程中发现,不同的实验条件对产物的产率有如下影响。
| 实验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 终了pH值 | 2.0 | 2.5 | 2.5 | 3.0 | 3.0 | 3.0 | 3.5 | 3.5 | 4.0 |
| 搅拌速度 | 快 | 快 | 快 | 快 | 快 | 慢 | 快 | 慢 | 快 |
| 草酸加入方式 | 滴加 | 滴加 | 倒入 | 滴加 | 倒入 | 倒入 | 滴加 | 倒入 | 滴加 |
| 产率/% | 65 | 74 | 54 | 86 | 72 | 56 | 88 | 75 | 72 |
(5)准确称取已制备晶体8.500g溶于水中,加水定容至250mL,取试样溶液25.00mL于锥形瓶中,用0.1000mol/L
 溶液滴定,消耗
溶液滴定,消耗 标准液20.00mL,则该产品的纯度是
标准液20.00mL,则该产品的纯度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】为测定某氟化稀土样品中氟元素的质量分数,某化学兴趣小组进行了如下实验。利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再滴定测量。实验装置如图所示。
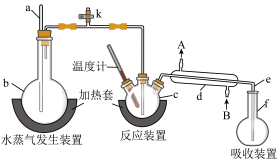
(1)a 的作用是_____ ,仪器 d 中冷凝水的方向为_____ 进_____ 出。(填 A 或 B)
(2)检查装置气密性:_____ (填操作),关闭 k,微热 c,导管 e 末端有气泡冒出;停止加热,导管e 内有一段稳定的水柱,说明装置气密性良好。
(3)c 中加入一定体积高氯酸和 m g 氟化稀土样品,f中盛有滴加酚酞的NaOH 溶液。加热 b、c,使b 中产生的水蒸气进入 c。
①下列物质可代替高氯酸的是_____ (填序号)。
A.硝酸 B.盐酸 C.硫酸 D.磷酸
②实验中除有HF 气体外,可能还有少量 SiF4(易水解)气体生成。若有 SiF4生成,实验结果将_____ (填“偏高”“偏低”或“不受影响”)。
③若观察到 f 中溶液红色褪去,需_____ (填操作),否则会使 实验结果偏低。
(4)向馏出液中加入 V1 mL c1mol·L-1La(NO3)3溶液,得到 LaF3沉淀(不考虑其他沉淀的生成),再用 c2mol·L-1 EDTA 标准溶液滴定剩余 La3+(La3+与 EDTA 按 1∶1 配合),消耗 EDTA 标准溶液 V2 mL,则氟化稀土样品中氟的质量分数为_____ 。

(1)a 的作用是
(2)检查装置气密性:
(3)c 中加入一定体积高氯酸和 m g 氟化稀土样品,f中盛有滴加酚酞的NaOH 溶液。加热 b、c,使b 中产生的水蒸气进入 c。
①下列物质可代替高氯酸的是
A.硝酸 B.盐酸 C.硫酸 D.磷酸
②实验中除有HF 气体外,可能还有少量 SiF4(易水解)气体生成。若有 SiF4生成,实验结果将
③若观察到 f 中溶液红色褪去,需
(4)向馏出液中加入 V1 mL c1mol·L-1La(NO3)3溶液,得到 LaF3沉淀(不考虑其他沉淀的生成),再用 c2mol·L-1 EDTA 标准溶液滴定剩余 La3+(La3+与 EDTA 按 1∶1 配合),消耗 EDTA 标准溶液 V2 mL,则氟化稀土样品中氟的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
名校
【推荐2】医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~103.0%)的主要流程如下:
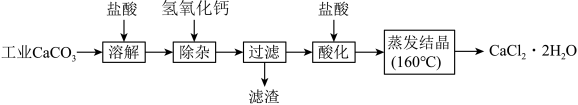
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是________________ 。
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③_______________ 。
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:____________________ 。
②计算上述样品中CaCl2·2H2O的质量分数为:____________________ 。
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:__________ ;___________ 。

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:
②计算上述样品中CaCl2·2H2O的质量分数为:
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以水氯镁石样品(主要成分 ,含少量有机色素和
,含少量有机色素和 、
、 、
、 、
、 )为原料,制备氯化镁的流程如下:
)为原料,制备氯化镁的流程如下:
①此过程中 能产生·OH(羟基自由基),可使部分有机色素转化为
能产生·OH(羟基自由基),可使部分有机色素转化为 和
和 。·OH体现的性质是
。·OH体现的性质是___________ 。
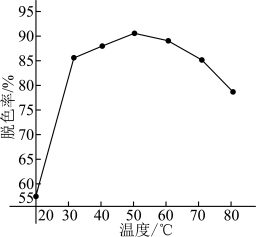
②相同时间内,测得不同温度下脱色率的变化如图所示。50℃前脱色率随着温度升高而升高,原因是___________ 。
①加氨水调节pH时, 转化成
转化成 的离子方程式为
的离子方程式为___________ 。加入 之前需进行的操作及原因是
之前需进行的操作及原因是___________ 。
②已知:室温下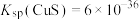 、
、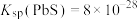 ,溶液中离子浓度小于或等于
,溶液中离子浓度小于或等于 mol⋅L-1即认为已经除尽。除
mol⋅L-1即认为已经除尽。除 、
、 离子时,
离子时, 、
、 均沉淀完全,此时需控制溶液中
均沉淀完全,此时需控制溶液中 不低于
不低于___________ 。
(3)测定产品中 含量的实验方案如下:
含量的实验方案如下:
取一定量样品溶于水,加水定容至500 mL。取10.00 mL所得溶液于锥形瓶中,滴加0.2500 mol⋅L-1的 溶液20.00 mL,充分反应后,过滤。向滤液中加入指示剂,用0.1000 mol⋅L-1
溶液20.00 mL,充分反应后,过滤。向滤液中加入指示剂,用0.1000 mol⋅L-1 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液10.00 mL。
溶液10.00 mL。
已知:
样品中 的物质的量为
的物质的量为___________ (写出计算过程)
 ,含少量有机色素和
,含少量有机色素和 、
、 、
、 、
、 )为原料,制备氯化镁的流程如下:
)为原料,制备氯化镁的流程如下: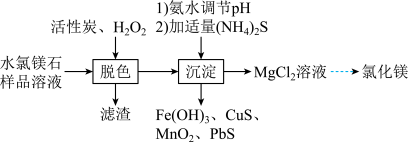
①此过程中
 能产生·OH(羟基自由基),可使部分有机色素转化为
能产生·OH(羟基自由基),可使部分有机色素转化为 和
和 。·OH体现的性质是
。·OH体现的性质是②相同时间内,测得不同温度下脱色率的变化如图所示。50℃前脱色率随着温度升高而升高,原因是
①加氨水调节pH时,
 转化成
转化成 的离子方程式为
的离子方程式为 之前需进行的操作及原因是
之前需进行的操作及原因是②已知:室温下
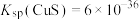 、
、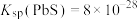 ,溶液中离子浓度小于或等于
,溶液中离子浓度小于或等于 mol⋅L-1即认为已经除尽。除
mol⋅L-1即认为已经除尽。除 、
、 离子时,
离子时, 、
、 均沉淀完全,此时需控制溶液中
均沉淀完全,此时需控制溶液中 不低于
不低于(3)测定产品中
 含量的实验方案如下:
含量的实验方案如下:取一定量样品溶于水,加水定容至500 mL。取10.00 mL所得溶液于锥形瓶中,滴加0.2500 mol⋅L-1的
 溶液20.00 mL,充分反应后,过滤。向滤液中加入指示剂,用0.1000 mol⋅L-1
溶液20.00 mL,充分反应后,过滤。向滤液中加入指示剂,用0.1000 mol⋅L-1 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液10.00 mL。
溶液10.00 mL。已知:

样品中
 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】使用磷肥副产物氟硅酸钠(Na2SiF6)为原料合成冰晶石(Na3AlF6)成为一条合理利用资源、提高经济效益的新方法。工艺流程如下图所示:
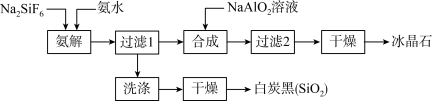
(1)传统合成冰晶石的方法是萤石(CaF2)法:使用萤石、石英和纯碱在高温下煅烧生成NaF,在NaF溶液中加入Al2(SO4)3溶液制得。在加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,
否则可能产生副产物____ (填物质的化学式),但酸度不宜过强的原因是____ 。
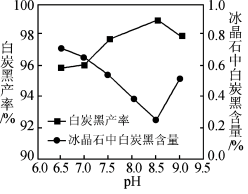
(2)氨解时白炭黑产率和冰晶石纯度与pH的关系如图,氨解时需要控制溶液的pH=____ ;能提高氨解速率的措施有____ (填字母)。
A.快速搅拌
B.加热混合液至100℃
C.减小氨水浓度
(3)工艺流程中氨解反应的化学方程式为____ ;冰晶石合成反应的离子方程式为______ 。
(4)为了提高原料利用率,减少环境污染,可采取的措施是___ 。

(1)传统合成冰晶石的方法是萤石(CaF2)法:使用萤石、石英和纯碱在高温下煅烧生成NaF,在NaF溶液中加入Al2(SO4)3溶液制得。在加入硫酸铝溶液前,需先用硫酸将NaF溶液的pH下调至5左右,

否则可能产生副产物
(2)氨解时白炭黑产率和冰晶石纯度与pH的关系如图,氨解时需要控制溶液的pH=
A.快速搅拌
B.加热混合液至100℃
C.减小氨水浓度
(3)工艺流程中氨解反应的化学方程式为
(4)为了提高原料利用率,减少环境污染,可采取的措施是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知甲、乙、丙、丁是四种可溶性物质,其中甲是碱,乙是酸,丙、丁是盐,它们分别溶于水后电离产生的离子只有 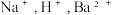 三种阳离子和
三种阳离子和 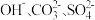 三种阴离子。乙、丙溶液均可与丁溶液反应生成气体,乙、丙、丁溶液均可与甲溶液反应生成白色沉淀,其中丁中生成的白色沉淀C可溶于稀硝酸。回答下列问题:
三种阴离子。乙、丙溶液均可与丁溶液反应生成气体,乙、丙、丁溶液均可与甲溶液反应生成白色沉淀,其中丁中生成的白色沉淀C可溶于稀硝酸。回答下列问题:
(1)在两份相同的甲溶液中,分别滴入物质的量浓度相等的乙、丙溶液,其导电能力随滴入溶液体积变化的曲线如图所示。____ (填化学式)溶液的变化曲线,曲线Ⅰ反应开始到 点的离子方程式是
点的离子方程式是_____ ,曲线Ⅱ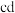 段对应的化学方程式是
段对应的化学方程式是___ 。
(2)鉴别乙中的阴离子的操作是______ 。
(3)白色沉淀C溶于稀硝酸的离子方程式为_____ 。
(4)实验发现丁溶液能使酚酞溶液变红,为探究其呈碱性的原因,设计如下实验方案:取少量丁固体,加入无水酒精,充分振荡、静置,取上层清液,滴加酚酞溶液,溶液仍为无色;再加入少量水,溶液变为红色;向该红色溶液中滴加足量 溶液(中性),红色褪去。
溶液(中性),红色褪去。
①根据上述实验结果,推测溶液丁显碱性的原因可能是___ (填标号)。
A.溶液丁中含有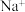 B.溶液丁中含有
B.溶液丁中含有 
C.溶液丁提供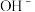 D.固体丁遇水能产生
D.固体丁遇水能产生 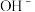
②酚酞是一种酸碱指示剂,要得出以上实验结论,酚酞溶液的溶剂不能是水,可能是酒精,理由是___ 。
③从形成盐的酸和碱的强弱角度看,丁属于___ (填标号)。
A.强酸强碱盐 B.强酸弱碱盐 C.弱酸强碱盐 D.弱酸弱碱盐
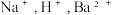 三种阳离子和
三种阳离子和 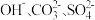 三种阴离子。乙、丙溶液均可与丁溶液反应生成气体,乙、丙、丁溶液均可与甲溶液反应生成白色沉淀,其中丁中生成的白色沉淀C可溶于稀硝酸。回答下列问题:
三种阴离子。乙、丙溶液均可与丁溶液反应生成气体,乙、丙、丁溶液均可与甲溶液反应生成白色沉淀,其中丁中生成的白色沉淀C可溶于稀硝酸。回答下列问题:(1)在两份相同的甲溶液中,分别滴入物质的量浓度相等的乙、丙溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
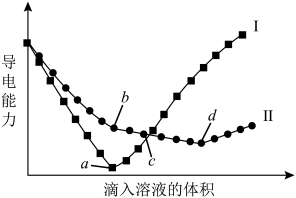
 点的离子方程式是
点的离子方程式是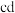 段对应的化学方程式是
段对应的化学方程式是(2)鉴别乙中的阴离子的操作是
(3)白色沉淀C溶于稀硝酸的离子方程式为
(4)实验发现丁溶液能使酚酞溶液变红,为探究其呈碱性的原因,设计如下实验方案:取少量丁固体,加入无水酒精,充分振荡、静置,取上层清液,滴加酚酞溶液,溶液仍为无色;再加入少量水,溶液变为红色;向该红色溶液中滴加足量
 溶液(中性),红色褪去。
溶液(中性),红色褪去。①根据上述实验结果,推测溶液丁显碱性的原因可能是
A.溶液丁中含有
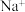 B.溶液丁中含有
B.溶液丁中含有 
C.溶液丁提供
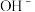 D.固体丁遇水能产生
D.固体丁遇水能产生 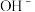
②酚酞是一种酸碱指示剂,要得出以上实验结论,酚酞溶液的溶剂不能是水,可能是酒精,理由是
③从形成盐的酸和碱的强弱角度看,丁属于
A.强酸强碱盐 B.强酸弱碱盐 C.弱酸强碱盐 D.弱酸弱碱盐
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】亚硫酰氯( )是一种重要的化工原料,其熔点-105℃,沸点79℃,140℃以上时易分解,遇水剧烈反应生成两种酸性物质。某小组利用反应
)是一种重要的化工原料,其熔点-105℃,沸点79℃,140℃以上时易分解,遇水剧烈反应生成两种酸性物质。某小组利用反应 制备
制备 ,并探究其性质、测定其纯度。
,并探究其性质、测定其纯度。
实验一:制备产品并探究SOCl2的性质
根据图示装置设计实验(装置可以重复使用),已知SCl2遇水易分解。____ →d、e←____ ←h。
(2)碱石灰的作用为___________ 。
(3)实验室用亚硫酸钠固体与70%硫酸制备SO2,不用稀硫酸的原因为___________ 。
(4)已知 在稍高于沸点的温度下会发生明显的分解,分解产物为
在稍高于沸点的温度下会发生明显的分解,分解产物为 和一种无色刺激性气味气体A和单质气体B,写出化学反应方程式
和一种无色刺激性气味气体A和单质气体B,写出化学反应方程式___________ 。
(5)AlCl3ˑ6H2O与 混合加热以制备无水AlCl3,
混合加热以制备无水AlCl3, 的作用是
的作用是___________ 。
 )是一种重要的化工原料,其熔点-105℃,沸点79℃,140℃以上时易分解,遇水剧烈反应生成两种酸性物质。某小组利用反应
)是一种重要的化工原料,其熔点-105℃,沸点79℃,140℃以上时易分解,遇水剧烈反应生成两种酸性物质。某小组利用反应 制备
制备 ,并探究其性质、测定其纯度。
,并探究其性质、测定其纯度。实验一:制备产品并探究SOCl2的性质
根据图示装置设计实验(装置可以重复使用),已知SCl2遇水易分解。
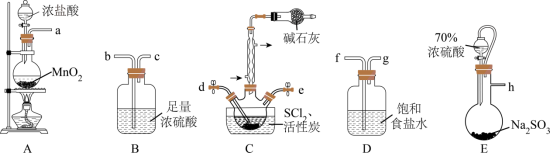
(2)碱石灰的作用为
(3)实验室用亚硫酸钠固体与70%硫酸制备SO2,不用稀硫酸的原因为
(4)已知
 在稍高于沸点的温度下会发生明显的分解,分解产物为
在稍高于沸点的温度下会发生明显的分解,分解产物为 和一种无色刺激性气味气体A和单质气体B,写出化学反应方程式
和一种无色刺激性气味气体A和单质气体B,写出化学反应方程式(5)AlCl3ˑ6H2O与
 混合加热以制备无水AlCl3,
混合加热以制备无水AlCl3, 的作用是
的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.实验室有一瓶失去标签的某白色固体X,已知其成分可能是碳酸钠,碳酸钾,亚硫酸钠,亚硫酸钾这四种物质中的一种,且成分单一、现成都外国语学校某化学兴趣小组通过如下步骤来确定其成分:
(1)阳离子的确定
实验方法及现象:___________ 。
结论:此白色固体是钠盐。
(2)阴离子的确定
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需继续进行如下实验:取适量白色固体配成溶液,取少许该溶液于试管中,加入BaCl2溶液,出现白色沉淀。
结论:___________ 。
Ⅱ.确认其成分后,由于某些原因,该白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤①:称取样品1.000 g。
步骤②:将样品溶解后完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤③:移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1酸性KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤③所发生反应的离子方程式:___________ 。
(2)判断滴定终点的现象是___________ 。
(3) 实验前,首先要精确配制一定物质的量浓度的 KMnO4 溶液 250 mL,配制时需要用的仪器除天平、药匙、玻璃棒、烧杯外,还需___________ 。
(4)滴定结果如表所示:
则该变质固体中X的质量分数为___________ 。
(1)阳离子的确定
实验方法及现象:
结论:此白色固体是钠盐。
(2)阴离子的确定
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需继续进行如下实验:取适量白色固体配成溶液,取少许该溶液于试管中,加入BaCl2溶液,出现白色沉淀。
结论:
Ⅱ.确认其成分后,由于某些原因,该白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤①:称取样品1.000 g。
步骤②:将样品溶解后完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤③:移取25.00 mL样品溶液于250 mL锥形瓶中,用0.01 mol·L-1酸性KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤③所发生反应的离子方程式:
(2)判断滴定终点的现象是
(3) 实验前,首先要精确配制一定物质的量浓度的 KMnO4 溶液 250 mL,配制时需要用的仪器除天平、药匙、玻璃棒、烧杯外,还需
(4)滴定结果如表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】以含钴废催化剂(主要成分为 、
、 、
、 )为原料制取复合氧化钴的流程如下:
)为原料制取复合氧化钴的流程如下:
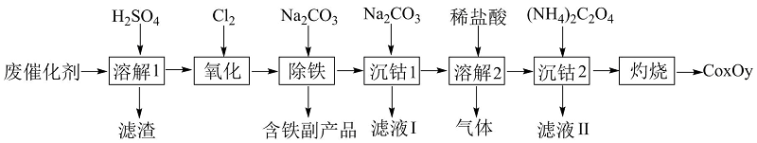
已知: 可与
可与 反应生成氢气;
反应生成氢气;
 难溶于水可溶于稀盐酸;
难溶于水可溶于稀盐酸;
 受热不稳定且
受热不稳定且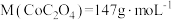 。
。
(1)用 溶解后过滤,得到的滤渣是
溶解后过滤,得到的滤渣是___________ (填化学式)。为提高钻元素的利用率可将滤渣洗涤2~3次,再将洗液与滤液合并,检验滤渣是否洗净的试剂是___________ (填化学式)。
(2)通入 是为了氧化
是为了氧化 ,氧化过程中反应的离子方程式是
,氧化过程中反应的离子方程式是___________ 。为了确定生成了 ,可选的检验试剂是
,可选的检验试剂是___________ (填试剂名称)。
(3)写出溶解2的化学方程式___________ 。
(4)准确称取沉钴2中所得纯净 固体
固体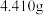 ,
, 在空气中灼烧得到钴的一种氧化物
在空气中灼烧得到钴的一种氧化物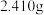 ,所得
,所得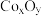 中Co原子与O原子物质的量之比为
中Co原子与O原子物质的量之比为___________ 。
 、
、 、
、 )为原料制取复合氧化钴的流程如下:
)为原料制取复合氧化钴的流程如下:
已知:
 可与
可与 反应生成氢气;
反应生成氢气; 难溶于水可溶于稀盐酸;
难溶于水可溶于稀盐酸; 受热不稳定且
受热不稳定且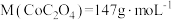 。
。(1)用
 溶解后过滤,得到的滤渣是
溶解后过滤,得到的滤渣是(2)通入
 是为了氧化
是为了氧化 ,氧化过程中反应的离子方程式是
,氧化过程中反应的离子方程式是 ,可选的检验试剂是
,可选的检验试剂是(3)写出溶解2的化学方程式
(4)准确称取沉钴2中所得纯净
 固体
固体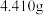 ,
, 在空气中灼烧得到钴的一种氧化物
在空气中灼烧得到钴的一种氧化物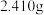 ,所得
,所得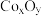 中Co原子与O原子物质的量之比为
中Co原子与O原子物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室模拟“侯氏制碱法”原理,以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3+CO2+H2O=NH4HCO3; NH4HCO3+NaCl=NaHCO3↓+NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(1)利用上述反应原理,设计如图所示装置,制取碳酸氢钠晶体,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉。图中夹持装置已略去。
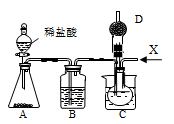
①实验室制备X气体的化学方程式为___________ 。
②B中应盛有___________ 溶液。在实验过程中,应向C中先通入足量的___________ 。
(2)该小组同学为了测定C中所得碳酸氢钠晶体的纯度,称取1.50g样品,将其配成100mL溶液。移取20.00mL溶液于锥形瓶中,用0.2000mol·L−1 的盐酸进行滴定。溶液pH随盐酸溶液加入量变化的曲线如下图所示。
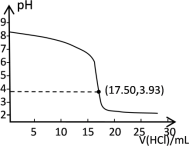
①根据曲线判断能够准确指示滴定终点现象的指示剂为___________ 。
②碳酸氢钠的纯度为___________ 。
 Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。(1)利用上述反应原理,设计如图所示装置,制取碳酸氢钠晶体,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉。图中夹持装置已略去。

①实验室制备X气体的化学方程式为
②B中应盛有
(2)该小组同学为了测定C中所得碳酸氢钠晶体的纯度,称取1.50g样品,将其配成100mL溶液。移取20.00mL溶液于锥形瓶中,用0.2000mol·L−1 的盐酸进行滴定。溶液pH随盐酸溶液加入量变化的曲线如下图所示。
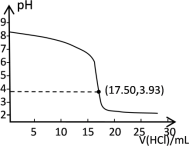
①根据曲线判断能够准确指示滴定终点现象的指示剂为
②碳酸氢钠的纯度为
您最近一年使用:0次



