以印刷线路板的碱性蚀刻废液(主要成分为[Cu(NH3)4]Cl2)或焙烧过的铜精炼炉渣(主要成分为CuO、SiO2少量Fe2O3)为原料均能制备CuSO4·5H2O晶体。
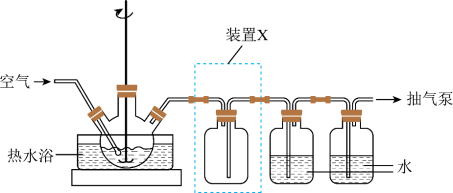
(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。
①写出用蚀刻废液制备CuO反应的化学方程式:___________ 。
②检验CuO固体是否洗净的实验操作是___________ 。
③装置图中装置X的作用是___________ 。
(2)以焙烧过的铜精炼炉渣为原料制备CuSO4·5H2O晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣,___________ ,加热浓缩、冷却结晶、过滤、晾干,得到CuSO4·5H2O晶体。

(1)取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到CuSO4·5H2O晶体。
①写出用蚀刻废液制备CuO反应的化学方程式:
②检验CuO固体是否洗净的实验操作是
③装置图中装置X的作用是
(2)以焙烧过的铜精炼炉渣为原料制备CuSO4·5H2O晶体时,请补充完整相应的实验方案:取一定量焙烧过的铜精炼炉渣,
2022高三·全国·专题练习 查看更多[1]
(已下线)专题17 无机制备实验-2022年高考化学二轮复习重点专题常考点突破练
更新时间:2022-03-11 21:00:20
|
相似题推荐
【推荐1】现有金属单质A、B、C和气体甲、乙、丙及物质D、 E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
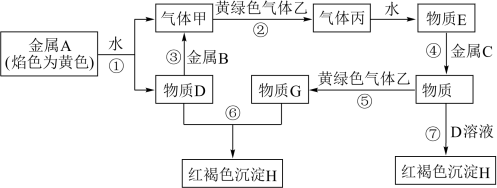
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B__________ 、丙__________ 。
(2)说出黄绿色气体乙的一种用途:________________ 。反应过程⑦可能观察到的实验现象是________________ 。
(3)反应①的离子方程式为________________ 。
(4)反应③中的氧化剂是____________ (写化学式,下同)反应④中的还原剂是____________ 。
(5)写出反应⑤的离子方程式:________________ 。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B
(2)说出黄绿色气体乙的一种用途:
(3)反应①的离子方程式为
(4)反应③中的氧化剂是
(5)写出反应⑤的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)现有铁和铜的混合物,可以通过___________ 把他们分开。
A.盐酸 B.NaOH C.FeCl3
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
请写出FeCl3溶液与铜反应的离子方程式:___________ 。
反应后的废液中含有Fe3+,可以用___________ 检验。
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。___________ ,黄绿色气体C可以把滤液转化成FeCl3腐蚀液,写出反应过程中的离子方程式___________ 。
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,___________ (补全实验现象),此过程涉及氧化还原反应的化学方程式是___________ 。
(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为___________ 。
(1)现有铁和铜的混合物,可以通过
A.盐酸 B.NaOH C.FeCl3
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
请写出FeCl3溶液与铜反应的离子方程式:
反应后的废液中含有Fe3+,可以用
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。

(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某废旧金属材料中主要为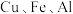 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾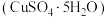 的一种流程如下:
的一种流程如下: 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。
回答下列问题:
(1)“破碎”的目的是___________ 。
(2)“碱浸”时发生反应的离子方程式为___________ 。
(3)“酸浸、氧化”的温度不宜过高,原因是___________ ;“滤渣2”的主要成分是___________ (填化学式)。
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有 的是___________。
的是___________。
(5)测定产品的纯度:准确称取胆矾样品 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为___________ (保留3位有效数字)。
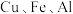 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾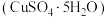 的一种流程如下:
的一种流程如下: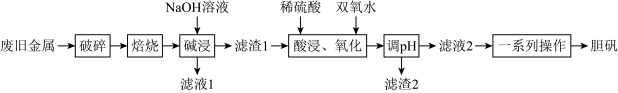
 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。回答下列问题:
(1)“破碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“酸浸、氧化”的温度不宜过高,原因是
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有
 的是___________。
的是___________。A. 溶液,新制氯水 溶液,新制氯水 | B.酸性高锰酸钾溶液 |
C. 溶液 溶液 | D.淀粉 试纸 试纸 |
(5)测定产品的纯度:准确称取胆矾样品
 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制乙醚的反应原理是:2CH3CH2OH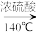 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
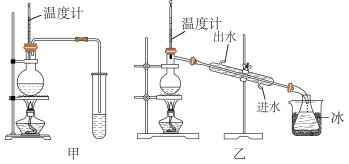
(1)图甲和乙是两套实验室制乙醚的装置,选装置_______ 较合适,理由是 _______ 。
(2)反应液中应加入沸石,其作用是_______ 。
(3)反应中温度计的位置是_______ 。
(4)用装置乙制得的乙醚中可能含有一定量的杂质,这杂质是_______ ,除去这种杂质的简易方法是 _______ 。
(5)请写出温度在170℃左右时发生反应的化学方程式_______ 。
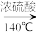 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
(1)图甲和乙是两套实验室制乙醚的装置,选装置
(2)反应液中应加入沸石,其作用是
(3)反应中温度计的位置是
(4)用装置乙制得的乙醚中可能含有一定量的杂质,这杂质是
(5)请写出温度在170℃左右时发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】磷精矿湿法制备磷酸的一种工艺流程如下:
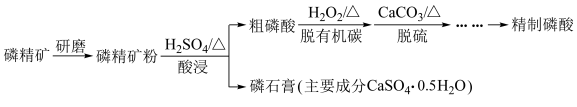
已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)在上述工艺流程中,能起到加快反应速率的措施有_______ 、_______ 。
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4 10CaSO4·0.5H2O+6H3PO4。
10CaSO4·0.5H2O+6H3PO4。
①该反应体现出酸性关系:H3PO4_______ H2SO4(填“>”或“<”)。
②请结合元素周期律解释①中酸性强弱结论:_______ 。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:_______ 。
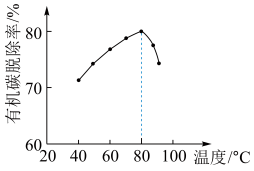
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:_______ 。
(5)脱硫时,CaCO3稍过量,充分反应后仍有SO 残留,原因是
残留,原因是_______ ;加入BaCO3可进一步提高硫的脱除率,说明溶解度BaSO4_______ CaSO4(填“>”或“<”)。

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)在上述工艺流程中,能起到加快反应速率的措施有
(2)磷精矿粉酸浸时发生反应:2Ca5(PO4)3(OH)+3H2O+10H2SO4
 10CaSO4·0.5H2O+6H3PO4。
10CaSO4·0.5H2O+6H3PO4。①该反应体现出酸性关系:H3PO4
②请结合元素周期律解释①中酸性强弱结论:
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:

(5)脱硫时,CaCO3稍过量,充分反应后仍有SO
 残留,原因是
残留,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】我国化学家侯德榜先生发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去):

(1)①一③所涉及的操作方法中,包含过滤的是___________ (填序号),操作中用到的主要玻璃仪器有烧杯、漏斗和___________ 。
(2)根据上述流程图,将化学方程式补充完整:___________ 。
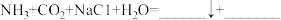
(3)下列关于联合制碱法流程说法正确的是___________ (填字母)。
a.可循环使用的物质有CO2
b.副产物NH4C1可用作氮肥
c.优先通入CO2气体,后通入NH3
(4)该反应能够发生是因为在相同条件下,溶解度:NaCl___________ NaHCO3(填“>”或“<”)。
(5)上述流程中,得到产品纯碱的化学方程式为:___________ 。
(6)鉴别NaHCO3固体中含有NaCl杂质的方法是:取少量固体于试管中,加适量水溶解后,向其中滴加足量的___________ 溶液,然后滴加___________ 溶液,若出现白色沉淀,则证明有NaCl杂质。

(1)①一③所涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
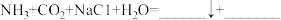
(3)下列关于联合制碱法流程说法正确的是
a.可循环使用的物质有CO2
b.副产物NH4C1可用作氮肥
c.优先通入CO2气体,后通入NH3
(4)该反应能够发生是因为在相同条件下,溶解度:NaCl
(5)上述流程中,得到产品纯碱的化学方程式为:
(6)鉴别NaHCO3固体中含有NaCl杂质的方法是:取少量固体于试管中,加适量水溶解后,向其中滴加足量的
您最近一年使用:0次



