碘元素是我们人体不可或缺的微量元素,某化学兴趣小组在实验室模拟工业提碘,流程图如下,请回答下列问题:
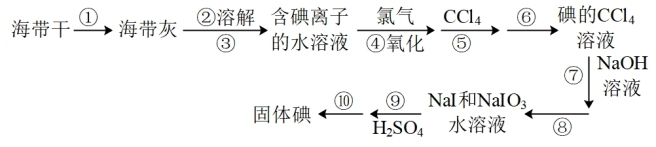
(1)请填写流程图中的操作步骤名称:③___________ ; ⑤___________ ;⑧___________ ;⑩___________ 。
(2)请填写该操作所需要的重要仪器名称:①___________ ;⑥___________ 。
(3)步骤①的目的是:___________ 。步骤④⑤⑥⑦⑧的目的是:___________ 。
(4)检验步骤③后的水溶液中是否含有碘离子的方法是___________ 。
(5)请写出步骤⑦发生的离子方程式:___________ 。
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)

(1)请填写流程图中的操作步骤名称:③
(2)请填写该操作所需要的重要仪器名称:①
(3)步骤①的目的是:
(4)检验步骤③后的水溶液中是否含有碘离子的方法是
(5)请写出步骤⑦发生的离子方程式:
(6)为了获得更纯净的碘单质,针对固体碘可以进行的操作是___________。(填写编号)
| A.加入干燥剂,加热升华 | B.蒸馏 |
| C.重结晶 | D.萃取、分液 |
更新时间:2022/03/16 17:43:36
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室制备1-溴丁烷的原理为CH3CH2CH2CH2OH+NaBr+H2SO4 CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
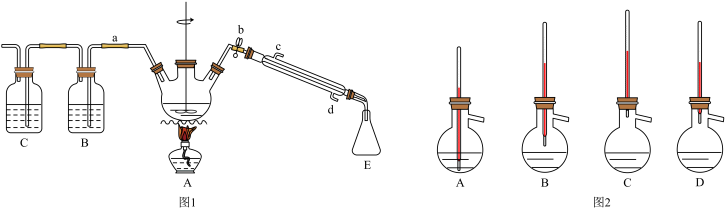
(1)仪器D的名称为________ ,使用玻璃棒搅拌的目的是__________________ 。
(2)1-溴丁烷的制备反应中可能有:________ 、________ 、溴化氢等副产物生成。熄灭图1中A装置中的酒精灯,打开a,余热会使反应继续进行。B、C装置可检验部分副产物,则B、C装置中所盛放的试剂分别是________ 、________ 。
(3)为了精制1-溴丁烷,待烧瓶冷却后,将A装置中的玻璃棒换成温度计,关闭a,打开b,使冷水从________ (填“c”或“d”)处流入。对粗产品进行蒸馏提纯时,图2装置中温度计的位置正确的是________ (填字母,下同),可能会导致收集到的产品中混有低沸点杂质的装置是________ 。
 CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
CH3CH2CH2CH2Br+NaHSO4+H2O,根据原理设计实验装置如图1所示(夹持装置已略去)
(1)仪器D的名称为
(2)1-溴丁烷的制备反应中可能有:
(3)为了精制1-溴丁烷,待烧瓶冷却后,将A装置中的玻璃棒换成温度计,关闭a,打开b,使冷水从
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
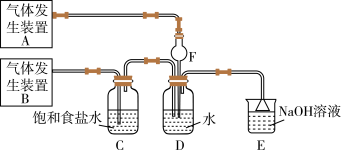
(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是______ ,发生装置B应选择以下三种装置中的______ (填①或②或③)。
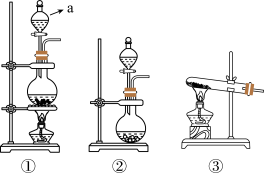
(2)图①中a的仪器名称______ ,D装置中主要反应离子方程式为______ 。
(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。上述现象体现了浓硫酸的_____ (填序号)①酸性②吸水性③脱水性④强氧化性,并写出“体积膨胀,并放出有刺激性气味的气体(SO2)”对应的化学方程式:_____ 。
(4)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
a.氯化铁溶液 b.氯化亚铁溶液 c.硫氰化钾溶液 d.氯化钡溶液 e.品红溶液 f.酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有______ (选填一个序号)试剂的试管内,再加入______ (选填一个序号)试剂。发生的现象是______ 。若SO2过量,取适量D中溶液滴加至盛有_____ (选填一个序号)试剂的试管内,发生的现象是______ 。

(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是

(2)图①中a的仪器名称
(3)将适量的蔗糖放入烧杯中,加少量水拌匀,再加适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。上述现象体现了浓硫酸的
(4)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
a.氯化铁溶液 b.氯化亚铁溶液 c.硫氰化钾溶液 d.氯化钡溶液 e.品红溶液 f.酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】四氯化锡( 熔点为-33℃,沸点为114℃,易水解生成固体
熔点为-33℃,沸点为114℃,易水解生成固体 )可用于分析试剂,有机合成脱水剂,可由熔融态的金属锡(
)可用于分析试剂,有机合成脱水剂,可由熔融态的金属锡( ,熔点为231℃)在300℃左右与氯气作用制得,利用如图所示装置制备无水
,熔点为231℃)在300℃左右与氯气作用制得,利用如图所示装置制备无水 (夹持和控温装置省略):
(夹持和控温装置省略):
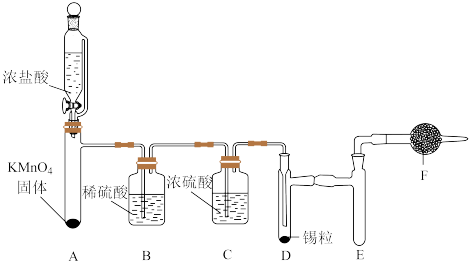
回答下列问题
(1)盛装浓盐酸的仪器名称是________ 。
(2) 装置的作用是
装置的作用是________ ,若无 装置对实验有何影响?请用化学方程式表示
装置对实验有何影响?请用化学方程式表示________ 。
(3)实验开始时,先向 试管中加入浓盐酸,待
试管中加入浓盐酸,待________ 时开始加热 试管;为使
试管;为使 装置起到良好效果,对
装置起到良好效果,对 装置进行的操作为
装置进行的操作为________ 。
(4)可用 测定产品中
测定产品中 含量以判断产品的纯度,取
含量以判断产品的纯度,取 装置中的产品,经过处理后配成
装置中的产品,经过处理后配成 溶液,用
溶液,用________ (填仪器名称)取出 放入锥形瓶中,加入二甲酚橙作指示剂,用
放入锥形瓶中,加入二甲酚橙作指示剂,用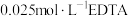 标准液进行滴定,达到滴定终点时消耗
标准液进行滴定,达到滴定终点时消耗 标准液
标准液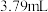 (定量关系:
(定量关系: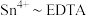 ),则产品纯度为
),则产品纯度为________ (精确到小数点后两位),若滴定管规格为 ,样品溶液起始读数为
,样品溶液起始读数为 ,此时滴定管中样品溶液的实际体积为
,此时滴定管中样品溶液的实际体积为________ 。(填序号)
A. B.
B. C.大于
C.大于 D.小于
D.小于
 熔点为-33℃,沸点为114℃,易水解生成固体
熔点为-33℃,沸点为114℃,易水解生成固体 )可用于分析试剂,有机合成脱水剂,可由熔融态的金属锡(
)可用于分析试剂,有机合成脱水剂,可由熔融态的金属锡( ,熔点为231℃)在300℃左右与氯气作用制得,利用如图所示装置制备无水
,熔点为231℃)在300℃左右与氯气作用制得,利用如图所示装置制备无水 (夹持和控温装置省略):
(夹持和控温装置省略):
回答下列问题
(1)盛装浓盐酸的仪器名称是
(2)
 装置的作用是
装置的作用是 装置对实验有何影响?请用化学方程式表示
装置对实验有何影响?请用化学方程式表示(3)实验开始时,先向
 试管中加入浓盐酸,待
试管中加入浓盐酸,待 试管;为使
试管;为使 装置起到良好效果,对
装置起到良好效果,对 装置进行的操作为
装置进行的操作为(4)可用
 测定产品中
测定产品中 含量以判断产品的纯度,取
含量以判断产品的纯度,取 装置中的产品,经过处理后配成
装置中的产品,经过处理后配成 溶液,用
溶液,用 放入锥形瓶中,加入二甲酚橙作指示剂,用
放入锥形瓶中,加入二甲酚橙作指示剂,用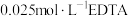 标准液进行滴定,达到滴定终点时消耗
标准液进行滴定,达到滴定终点时消耗 标准液
标准液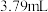 (定量关系:
(定量关系: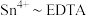 ),则产品纯度为
),则产品纯度为 ,样品溶液起始读数为
,样品溶液起始读数为 ,此时滴定管中样品溶液的实际体积为
,此时滴定管中样品溶液的实际体积为A.
 B.
B. C.大于
C.大于 D.小于
D.小于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】钛有强度高和质地轻的优点,广泛应用于飞机制造业等。工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备钛金属,工业流程如下:(已知: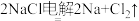 )
)

(1)请写出FeTiO3与稀盐酸反应的离子方程式:________________ 。
(2)请写出“熔融氧化”的化学方程式:_______________________ 。
(3)补充写出实现上述方框内过程A所需的实验操作:___________ 、__________ 过滤、洗涤、在干燥的HCl气流中加热→FeCl2固体
(4)热还原法中能否改用钠代替镁作还原剂:_____________ (填“能”或“不能”);
(5)上流程中可循环利用的物质为:____________________ (填化学式)。
 )
)
(1)请写出FeTiO3与稀盐酸反应的离子方程式:
(2)请写出“熔融氧化”的化学方程式:
(3)补充写出实现上述方框内过程A所需的实验操作:
(4)热还原法中能否改用钠代替镁作还原剂:
(5)上流程中可循环利用的物质为:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化沉淀法是制取 的一种常见方法,其制取流程如下图所示:
的一种常见方法,其制取流程如下图所示:_______ 。
(2)副产品P是_______ (填写化学式),由溶液N获得该副产品的操作是:加热浓缩→_______ →过滤洗涤→晶体加热至完全失去结晶水。
 的一种常见方法,其制取流程如下图所示:
的一种常见方法,其制取流程如下图所示: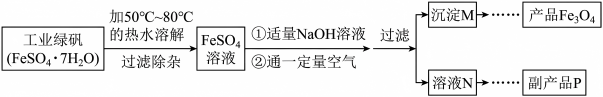
(2)副产品P是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】20℃下,制作网红“天气瓶”流程如下,请根据下述制作流程,结合下列信息和所学知识,回答问题:
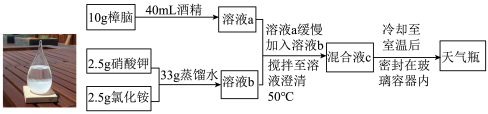
樟脑(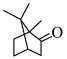 )是一种白色晶体,易溶于酒精、难溶于水。
)是一种白色晶体,易溶于酒精、难溶于水。
(1)樟脑难溶于水,易溶于酒精的原因主要是___________________ 。
(2)由硝酸钾、氯化铵制备得到“溶液b”的过程中需要用到的玻璃仪器有__________________________ 。得到“溶液c”时需控制温度50℃,可采取的方法是_______________ 。
(3)实验中发现硝酸钾溶解速率很慢,请推测原因________________________ 。
(4)温度改变,天气瓶内或清澈干净,或浑浊朦胧,或产生大片美丽的结晶。请通过计算说明0℃时出现的是樟脑晶体_________________ ,推测晶体产生的原因________ 。
(5)从晶体生长析出的角度分析,“天气瓶”制作中硝酸钾和氯化铵的作用是______________ 。

| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 硝酸钾溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| 氯化铵溶解度/g | 29.4 | 33.2 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 60.2 | 65.6 | 71.2 | 77.3 |
 )是一种白色晶体,易溶于酒精、难溶于水。
)是一种白色晶体,易溶于酒精、难溶于水。(1)樟脑难溶于水,易溶于酒精的原因主要是
(2)由硝酸钾、氯化铵制备得到“溶液b”的过程中需要用到的玻璃仪器有
(3)实验中发现硝酸钾溶解速率很慢,请推测原因
(4)温度改变,天气瓶内或清澈干净,或浑浊朦胧,或产生大片美丽的结晶。请通过计算说明0℃时出现的是樟脑晶体
(5)从晶体生长析出的角度分析,“天气瓶”制作中硝酸钾和氯化铵的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】下图是常用的实验仪器:(铁架台和玻璃导管、橡皮管、石棉网、瓶塞等略去)

用仪器对应的英文字母及相关文字填空:
Ⅰ填写以下仪器的名称:E___________________ I_________________
Ⅱ某实验小组用以上的部分仪器进行提取溴水中Br2单质的实验。实验步骤如下:
(1)将溴水倒入分液漏斗中,再加入某种液体,然后盖上塞子,倒转分液漏斗充分振荡,静置。该步骤的操作名称是:_____________ ,向分液漏斗中加入的液体不能选用下列的_____________
A.CCl4 B.苯 C. 酒精 D.汽油
(2)待分液漏斗充分静置后,将Br2的四氯化碳溶液和水分离开的操作叫做:_______________ ,下列是前面两步实验的操作步骤,正确的顺序是:_______________________________
① 将混合物倒入分液漏斗中,充分振荡,并放在铁架台的铁圈上静置、分层;
② 从分液漏斗上口倒出上层水溶液;
③ 将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④ 分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接受溶液
⑤ 检查分液漏斗活塞和颈部的玻璃塞是否漏水
(3)已知Br2的沸点是58.5℃,四氯化碳沸点是78℃。将Br2的四氯化碳溶液分离开的实验操作中所需的仪器除了酒精灯、温度计、冷凝管、牛角管之外还需要___________ (填仪器所对应的字母编号)连接装置时,仪器J的冷凝水应该_______ 进_______ 出(填a、b)。

用仪器对应的英文字母及相关文字填空:
Ⅰ填写以下仪器的名称:E
Ⅱ某实验小组用以上的部分仪器进行提取溴水中Br2单质的实验。实验步骤如下:
(1)将溴水倒入分液漏斗中,再加入某种液体,然后盖上塞子,倒转分液漏斗充分振荡,静置。该步骤的操作名称是:
A.CCl4 B.苯 C. 酒精 D.汽油
(2)待分液漏斗充分静置后,将Br2的四氯化碳溶液和水分离开的操作叫做:
① 将混合物倒入分液漏斗中,充分振荡,并放在铁架台的铁圈上静置、分层;
② 从分液漏斗上口倒出上层水溶液;
③ 将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④ 分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接受溶液
⑤ 检查分液漏斗活塞和颈部的玻璃塞是否漏水
(3)已知Br2的沸点是58.5℃,四氯化碳沸点是78℃。将Br2的四氯化碳溶液分离开的实验操作中所需的仪器除了酒精灯、温度计、冷凝管、牛角管之外还需要
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】蒸馏
(1)蒸馏是分离和提纯_______ 有机化合物的常用方法。
(2)原理:利用混合物中各组分_______ 不同(一般有机物与杂质的沸点应相差30℃以上),达到分离液态混合物的目的。当液态混合物中含有多种沸点不同的有机物组分时,经过多次_______ 和_______ 可以将这些成分(馏分)逐步分离,这一过程称为分馏,如石油的分馏等。
(3)优点:蒸馏的优点是不需要使用混合物组分以外的其他溶剂,_______ 引入新的杂质。
(4)实验装置
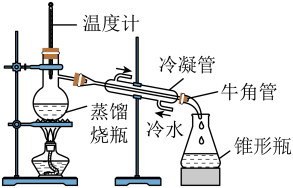
注意事项:
①温度计水银球位于_______ 。
②碎瓷片的作用:_______ 。
③冷凝管中水流的方向是下口进入,上口流出。
(1)蒸馏是分离和提纯
(2)原理:利用混合物中各组分
(3)优点:蒸馏的优点是不需要使用混合物组分以外的其他溶剂,
(4)实验装置

注意事项:
①温度计水银球位于
②碎瓷片的作用:
③冷凝管中水流的方向是下口进入,上口流出。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】水合肼( )是一种易挥发的无色液体,具有强还原性。实验室可通过如图所示流程制取水合肼液体。
)是一种易挥发的无色液体,具有强还原性。实验室可通过如图所示流程制取水合肼液体。
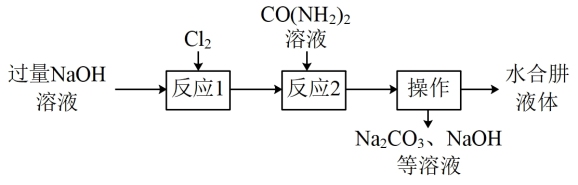
(1)已知反应1为放热反应,反应的目的是制取NaClO,NaClO受热不稳定,受热分解为NaCl和 。
。
①写出反应1的离子方程式:_______ 。
②为防止生成的NaClO分解,可采取的方法是_______ 。
(2)由反应1所得溶液与 溶液混合可以制取水合肼,装置如图所示。混合时应将一种溶液缓慢滴加到另一溶液中并不断搅拌。烧瓶中的溶液是
溶液混合可以制取水合肼,装置如图所示。混合时应将一种溶液缓慢滴加到另一溶液中并不断搅拌。烧瓶中的溶液是_______ ,理由是_______ 。
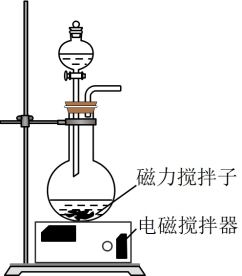
(3)写出反应2的化学方程式:_______
(4)分离出水合肼液体的操作方法是_______
 )是一种易挥发的无色液体,具有强还原性。实验室可通过如图所示流程制取水合肼液体。
)是一种易挥发的无色液体,具有强还原性。实验室可通过如图所示流程制取水合肼液体。
(1)已知反应1为放热反应,反应的目的是制取NaClO,NaClO受热不稳定,受热分解为NaCl和
 。
。①写出反应1的离子方程式:
②为防止生成的NaClO分解,可采取的方法是
(2)由反应1所得溶液与
 溶液混合可以制取水合肼,装置如图所示。混合时应将一种溶液缓慢滴加到另一溶液中并不断搅拌。烧瓶中的溶液是
溶液混合可以制取水合肼,装置如图所示。混合时应将一种溶液缓慢滴加到另一溶液中并不断搅拌。烧瓶中的溶液是
(3)写出反应2的化学方程式:
(4)分离出水合肼液体的操作方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
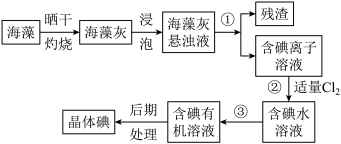
(1)实验室灼烧海带,需要下列仪器中的___ (填字母)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f. 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:
①____ ,③____ 。
(3)提取碘的过程中,可选择的有机试剂是___ 。
A.苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、酒精
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有___ 、__ 。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
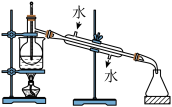
①_____ ;
②_____ ;
③_____ 。
(6)进行上述蒸馏操作时,使用水浴加热的原因是___ 。

(1)实验室灼烧海带,需要下列仪器中的
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f. 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:
①
(3)提取碘的过程中,可选择的有机试剂是
A.苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、酒精
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:

①
②
③
(6)进行上述蒸馏操作时,使用水浴加热的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】海带中含有丰富的碘元素,某学习小组设计如下实验流程提取海带中的碘,请回答下列问题:
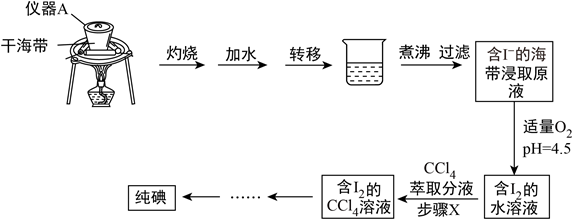
(1)仪器A的名称为__________________ ,实验室取用仪器A必须使用_________ 。
(2)煮沸的作用是______________________ 。
(3)步骤X中,使用了分液漏斗。分液漏斗使用前,须进行的操作是__________ ;萃取后,分液漏斗内观察到的现象是___________ ;分液时,为了保证液体顺利留下,应首先_________ 。
(4)向海带浸取原液中通入适量O2,并控制溶液pH为4.5,此时发生反应的离子反应方程式为:__________________________________________ 。
(5)某同学欲采用蒸馏含I2的CCl4溶液得到纯碘,此方案不合理,理由是_____________ 。
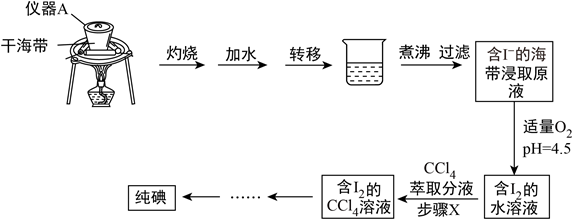
(1)仪器A的名称为
(2)煮沸的作用是
(3)步骤X中,使用了分液漏斗。分液漏斗使用前,须进行的操作是
(4)向海带浸取原液中通入适量O2,并控制溶液pH为4.5,此时发生反应的离子反应方程式为:
(5)某同学欲采用蒸馏含I2的CCl4溶液得到纯碘,此方案不合理,理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)装置图1中A的名称是___________ ,B的名称是___________ 。A中一般要加入碎瓷片,其作用是___________ ;装置图4中盛溶液的仪器名称是___________ 。
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

i.步骤③的实验操作名称是___________ ,使用到的玻璃仪器有___________
ii.步骤⑤的实验操作名称是___________ ,选择上述装置图___________ (填图的序号)。步骤⑤中的提取液能否用酒精代替,请说明理由:___________
(3)某“滤液”中溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度的变化如图所示,请设计从该“滤液”中获取ZnSO4晶体的实验方案:___________ (实验中可能使用的试剂:Zn粉、稀H2SO4、)。


(1)装置图1中A的名称是
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:

i.步骤③的实验操作名称是
ii.步骤⑤的实验操作名称是
(3)某“滤液”中溶质主要是ZnSO4和CuSO4。已知硫酸锌晶体的溶解度随温度的变化如图所示,请设计从该“滤液”中获取ZnSO4晶体的实验方案:

您最近一年使用:0次



