回答下列问题:
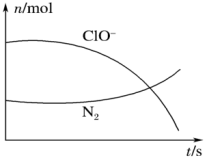
(1)某反应体系中有H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式_______ ,消耗1 mol还原剂,转移电子数为_______ 。
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是_______ ,相关反应的离子方程式是_______ 。
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为_______ ,生成的还原产物的质量为_______ g。
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式_____ 。
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
(1)某反应体系中有H2O、ClO-、NH
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Fe2+的还原性较强,实验室的氯化亚铁溶液常因氧化而变质,除去杂质的方法是
(3)根据反应8NH3+3Cl2=6NH4Cl+N2,当有68 g NH3参加反应时,被氧化的物质为
(4)K2FeO4(铁元素为+6价)可用作水处理剂,它可由以下反应制得,请配平下列离子方程式
_______Cl2 + _______ Fe(OH)3+_______ OH- = _______ FeO
 + _______ Cl- +_______ H2O
+ _______ Cl- +_______ H2O
更新时间:2022-03-20 19:27:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠单质性质活泼,钠有多种化合物。请回答下列问题:
(1) 能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:
能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:___________ 、___________ 。
(2)除去碳酸钠固体中混有的碳酸氢钠的方法为(用化学方程式表示):___________ 。
(3)某碳酸钠溶液中含有NaCl,验证该溶液中含有Cl-的实验操作和现象是:取少量待测液于试管中,___________ ,如果溶液出现白色沉淀,说明溶液中含有氯离子。
(4)已知碳酸钠可用于从海水提取溴,涉及的反应如下: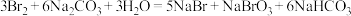
①该反应的离子方程式为___________ 。
②该反应中氧化剂与还原剂的质量之比是___________ 。
(1)
 能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:
能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:(2)除去碳酸钠固体中混有的碳酸氢钠的方法为(用化学方程式表示):
(3)某碳酸钠溶液中含有NaCl,验证该溶液中含有Cl-的实验操作和现象是:取少量待测液于试管中,
(4)已知碳酸钠可用于从海水提取溴,涉及的反应如下:
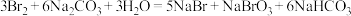
①该反应的离子方程式为
②该反应中氧化剂与还原剂的质量之比是
您最近一年使用:0次
【推荐2】请分析①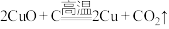 ②
② 完成以下问题:
完成以下问题:
(1)反应①中, 失氧发生
失氧发生_______ 反应(填“氧化”或“还原”),所含元素得到电子化合价_______ (填“升高”或“降低”)
(2)反应②中,氧化剂是_______ ,氧化产物是_______ 。氧化剂与还原剂的质量比_______ 。
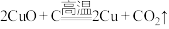 ②
② 完成以下问题:
完成以下问题:(1)反应①中,
 失氧发生
失氧发生(2)反应②中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ、海水是可以综合利用的。从海水中提取食盐和溴的过程:

(1)请写出一种海水淡化的方法________________________ 。
(2)步骤Ⅰ获取Br2的离子方程式为_________________________________________________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr,在该反应中,还原剂是________ (填化学式)。
Ⅱ、海带中的碘元素主要以I-的形式存在,提取时用适当的氧化剂将其氧化成I2,再萃取出来。证明海带中含有碘的实验步骤:
①用剪刀剪碎海带,用酒精湿润,放入坩埚中。
②灼烧海带至完全成灰,停止加热,冷却。
③将海带灰加蒸馏水溶解,搅拌、煮沸、过滤。
④在滤液中滴加稀硫酸及过氧化氢,然后加入几滴淀粉溶液,(涉及反应的离子方程式为2I-+H2O2+2H+=I2+2H2O)。
能证明海带中含有碘的实验步骤是________ (填序号),现象是_________________________ 。

(1)请写出一种海水淡化的方法
(2)步骤Ⅰ获取Br2的离子方程式为
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr,在该反应中,还原剂是
Ⅱ、海带中的碘元素主要以I-的形式存在,提取时用适当的氧化剂将其氧化成I2,再萃取出来。证明海带中含有碘的实验步骤:
①用剪刀剪碎海带,用酒精湿润,放入坩埚中。
②灼烧海带至完全成灰,停止加热,冷却。
③将海带灰加蒸馏水溶解,搅拌、煮沸、过滤。
④在滤液中滴加稀硫酸及过氧化氢,然后加入几滴淀粉溶液,(涉及反应的离子方程式为2I-+H2O2+2H+=I2+2H2O)。
能证明海带中含有碘的实验步骤是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应在生产生活中具有广泛的用途。
(1)在碱性条件下铝粉可与 反应,其化学方程式为
反应,其化学方程式为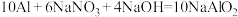
 。反应中氧化剂是
。反应中氧化剂是______ (填化学式)。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为
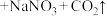 ,氧化剂与还原剂的质量之比为
,氧化剂与还原剂的质量之比为______ 。
(3) 可在野外作生氢剂,反应原理为
可在野外作生氢剂,反应原理为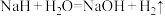 ,
, 中氢元素
中氢元素______ (填“被氧化”或“被还原”)。
(4)在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为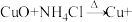
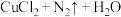 。配平此氧化还原反应方程式并用双线桥法标出电子的转移方向和数目:
。配平此氧化还原反应方程式并用双线桥法标出电子的转移方向和数目:______ 。
(1)在碱性条件下铝粉可与
 反应,其化学方程式为
反应,其化学方程式为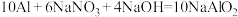
 。反应中氧化剂是
。反应中氧化剂是(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为

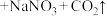 ,氧化剂与还原剂的质量之比为
,氧化剂与还原剂的质量之比为(3)
 可在野外作生氢剂,反应原理为
可在野外作生氢剂,反应原理为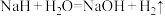 ,
, 中氢元素
中氢元素(4)在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为
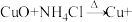
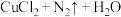 。配平此氧化还原反应方程式并用双线桥法标出电子的转移方向和数目:
。配平此氧化还原反应方程式并用双线桥法标出电子的转移方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】写出下列反应的离子方程式:
(1)自然界中Cr主要以+3价和+6价形式存在。 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:_______ 。
(2)常温下,氰化钠(NaCN)能与过氧化氢溶液反应,生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。写出该反应的离子方程式:_______ 。
(3)连二亚硫酸钠(Na2S2O4)常作木浆造纸的漂白剂。向甲酸钠(HCOONa)与 的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为
的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为_______ ,碱性条件下连二亚硫酸钠溶液与 溶液反应可得到单质银,相应的离子方程式为
溶液反应可得到单质银,相应的离子方程式为_______ 。
(4)煤燃烧排放的烟气含有SO2和 ,形成酸雨,污染大气,采用
,形成酸雨,污染大气,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 和NO的烟气,写出
和NO的烟气,写出 溶液脱硝(主要转化为
溶液脱硝(主要转化为 )过程中主要反应的离子方程式:
)过程中主要反应的离子方程式:_______ 。
(1)自然界中Cr主要以+3价和+6价形式存在。
 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:(2)常温下,氰化钠(NaCN)能与过氧化氢溶液反应,生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。写出该反应的离子方程式:
(3)连二亚硫酸钠(Na2S2O4)常作木浆造纸的漂白剂。向甲酸钠(HCOONa)与
 的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为
的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为 溶液反应可得到单质银,相应的离子方程式为
溶液反应可得到单质银,相应的离子方程式为(4)煤燃烧排放的烟气含有SO2和
 ,形成酸雨,污染大气,采用
,形成酸雨,污染大气,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 和NO的烟气,写出
和NO的烟气,写出 溶液脱硝(主要转化为
溶液脱硝(主要转化为 )过程中主要反应的离子方程式:
)过程中主要反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化硫(SO2)是形成酸雨的“罪魁祸首”,也是大气污染物之一,为了保护环境,应减少二氧化硫在大气中的排放。
(1)二氧化硫与水反应可生成弱酸亚硫酸(H2SO3),亚硫酸的水溶液能够导电。那么二氧化硫是___________ (填“电解质”或“非电解质”)。
(2)工业尾气中的二氧化硫常用氢氧化钠溶液吸收,生成亚硫酸钠(Na2SO3)或亚硫酸氢钠(NaHSO3)。亚硫酸氢钠(NaHSO3)属于___________ (填“酸”、“碱”、或“盐”),写出亚硫酸氢钠(NaHSO3)溶于水的电离方程式___________ 。
(3)二氧化硫在催化剂的作用下可被氧气氧化成三氧化硫,三氧化硫与水反应生成硫酸。
①若将稀H2SO4缓缓加入Ba(OH)2溶液中直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图中的曲线___________ (填序号)表示;
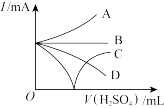
②已知浓H2SO4具有强氧化性,可以在加热条件下与单质Cu发生化学反应,生成CuSO4、SO2、H2O,请写出该化学反应方程式:___________ ,在该反应中还体现出浓硫酸的___________ 性。
(1)二氧化硫与水反应可生成弱酸亚硫酸(H2SO3),亚硫酸的水溶液能够导电。那么二氧化硫是
(2)工业尾气中的二氧化硫常用氢氧化钠溶液吸收,生成亚硫酸钠(Na2SO3)或亚硫酸氢钠(NaHSO3)。亚硫酸氢钠(NaHSO3)属于
(3)二氧化硫在催化剂的作用下可被氧气氧化成三氧化硫,三氧化硫与水反应生成硫酸。
①若将稀H2SO4缓缓加入Ba(OH)2溶液中直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图中的曲线

②已知浓H2SO4具有强氧化性,可以在加热条件下与单质Cu发生化学反应,生成CuSO4、SO2、H2O,请写出该化学反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)通常用小苏打的溶液除去CO2中的HCl,反应的离子方程式为:_______________ ,
不能用NaOH溶液的原因是__________ (用离子方程式表示),也不能用NaCO3的原因是__________ (用离子方程式表示)
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的化学方程式为______________
Fe(OH)2可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应来制备:
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入_______ 来防止Fe2+被氧化.
②生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是___________________ .
不能用NaOH溶液的原因是
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的化学方程式为
Fe(OH)2可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应来制备:
①用硫酸亚铁晶体配制上述FeSO4溶液时还需加入
②生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】向一定量的Fe和Fe2O3的混合物中加入80mL 的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
(1)请写出上述反应中所有属于氧化还原反应的化学方程式______ 。
(2)若忽略反应前后溶液体积变化,则最终所得溶液中溶质的物质的量浓度为______  。
。
(3)原固体混合物的总质量为______ g。
 的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:
的盐酸溶液,使固体混合物恰好完全溶解,放出标准状况下的气体224mL,在溶液中加入KSCN溶液无血红色出现。请回答下列问题:(1)请写出上述反应中所有属于氧化还原反应的化学方程式
(2)若忽略反应前后溶液体积变化,则最终所得溶液中溶质的物质的量浓度为
 。
。(3)原固体混合物的总质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有下列八种物质:①盐酸;②小苏打;③FeSO4•7H2O;④二氧化碳;⑤蔗糖;⑥氢氧化铁胶体;⑦氨水;⑧NaHSO4固体。
(1)上述八种物质中,属于电解质的是_____ (填序号,下同);属于非电解质的是_____ 。
(2)向⑥中滴加①产生的现象为______ 。
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为_____ 。
(4)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式表示铁粉的作用_____ 。
(1)上述八种物质中,属于电解质的是
(2)向⑥中滴加①产生的现象为
(3)将少量②的溶液与澄清石灰水混合,发生反应的离子方程式为
(4)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式表示铁粉的作用
您最近一年使用:0次



