回答下列问题:
(1)推测原子序数为82的元素在元素周期表中的位置是___________
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,同时生成KCl,其反应的离子方程式为___________
(3)bmLAl2(SO4)3溶液中含有agSO ,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为
,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为___________ mol/L
(4)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100mL1mol·L-1的盐酸,好使混合物完全反应,放出11.2mL(标准状况)气体,所得溶液中加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的该混合物,所得铁的质量为___________ 克
(5)在浓度均为4.0mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体体积比为2:3则加入铁粉的质量是___________ 克
(6)a克碳酸钠与碳酸氢钠的混合物,加热灼烧,固体质量为b克,求碳酸钠的质量分数___________
(7)0.2mol/LNa2SO360mL,恰好与含0.1mol/LK2M2O7的溶液40mL完全反应,试推测元素M在还原产物中的化合价___________ 价
(1)推测原子序数为82的元素在元素周期表中的位置是
(2)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,同时生成KCl,其反应的离子方程式为
(3)bmLAl2(SO4)3溶液中含有agSO
 ,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为
,若把此溶液取一半加水稀释至2bmL,则稀释后溶液中Al3+的物质的量浓度为(4)向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100mL1mol·L-1的盐酸,好使混合物完全反应,放出11.2mL(标准状况)气体,所得溶液中加入KSCN溶液不变红色。用足量的CO在高温下还原相同质量的该混合物,所得铁的质量为
(5)在浓度均为4.0mol/L的盐酸和硫酸各100mL溶液中,分别加入等质量的铁粉,充分反应后生成气体体积比为2:3则加入铁粉的质量是
(6)a克碳酸钠与碳酸氢钠的混合物,加热灼烧,固体质量为b克,求碳酸钠的质量分数
(7)0.2mol/LNa2SO360mL,恰好与含0.1mol/LK2M2O7的溶液40mL完全反应,试推测元素M在还原产物中的化合价
更新时间:2022-03-24 16:02:17
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】根据题目要求回答下列问题:
(1)标准状况下,1.7 g 与
与___________ L 气体含有的氢原子数相同。
气体含有的氢原子数相同。
(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为___________ 。
(3)有等体积的NaCl、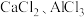 三种溶液,分别与足量的
三种溶液,分别与足量的 溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为 ___________ 。
(4)用20 g NaOH配制成500 mL溶液,其物质的量浓度为___________ mol/L,从中取出1 mL,其物质的量浓度为___________ mol/L,含溶质___________ g。若将这1 mL溶液用水稀释到100 mL,所得溶液中溶质的物质的量浓度为___________ moI/L。
(1)标准状况下,1.7 g
 与
与 气体含有的氢原子数相同。
气体含有的氢原子数相同。(2)在一定温度和压强下,0.4 mol某气体的体积为9.8 L,则该条件下的气体摩尔体积为
(3)有等体积的NaCl、
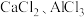 三种溶液,分别与足量的
三种溶液,分别与足量的 溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为 (4)用20 g NaOH配制成500 mL溶液,其物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有下列9种物质,① ②淀粉溶液③
②淀粉溶液③ ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸⑧
⑦纯醋酸⑧ 溶液⑨
溶液⑨ ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(1)以上能发生丁达尔效应的是_______ 。
(2)属于电解质的是_______ (填写序号)
(3)标准状况下,相同体积的④ 和⑤
和⑤ 原子个数之比为
原子个数之比为_______ ,标准状况下,若 和
和 混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为
混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为_______ ,标准状况下,V L 溶入100 mL
溶入100 mL  (1 g/mL)中,溶液密度为ρ g/mL,则氨水物质的量浓度表达式为
(1 g/mL)中,溶液密度为ρ g/mL,则氨水物质的量浓度表达式为_______ mol/L。
 ②淀粉溶液③
②淀粉溶液③ ④
④ ⑤
⑤ ⑥
⑥ ⑦纯醋酸⑧
⑦纯醋酸⑧ 溶液⑨
溶液⑨ ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:(1)以上能发生丁达尔效应的是
(2)属于电解质的是
(3)标准状况下,相同体积的④
 和⑤
和⑤ 原子个数之比为
原子个数之比为 和
和 混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为
混合气体相对于氢气的密度为14.5,则④和⑤物质的量之比为 溶入100 mL
溶入100 mL  (1 g/mL)中,溶液密度为ρ g/mL,则氨水物质的量浓度表达式为
(1 g/mL)中,溶液密度为ρ g/mL,则氨水物质的量浓度表达式为
您最近一年使用:0次
【推荐1】某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。

完成下列填空:
(1)HCN有剧毒,电子式是___ ,其分子属于___ (填“极性”、“非极性”)分子。
(2)选用最详尽描述核外电子运动状态的方式,来表示氮原子的最外层电子:___ ,氮原子核外有___ 种能量不同的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___ 。
a.相同条件下水溶液的酸性:HClO3>H2SO3
b.稳定性:HCl>H2S
c.相同条件下水溶液的pH:Na2S>NaCl
d.还原性:S2->Cl-
(4)写出流程②的离子方程式:___ 。
(5)反应②中,每消耗1.5mol Cr2O72-转移电子的数目为___ 个。
(6)取少量待检水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,用平衡移动原理解释产生该现象的原因___ 。

完成下列填空:
(1)HCN有剧毒,电子式是
(2)选用最详尽描述核外电子运动状态的方式,来表示氮原子的最外层电子:
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的酸性:HClO3>H2SO3
b.稳定性:HCl>H2S
c.相同条件下水溶液的pH:Na2S>NaCl
d.还原性:S2->Cl-
(4)写出流程②的离子方程式:
(5)反应②中,每消耗1.5mol Cr2O72-转移电子的数目为
(6)取少量待检水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,用平衡移动原理解释产生该现象的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学在治理空气污染方面发挥着重要的作用。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:
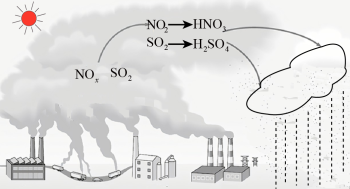
(1)HNO3的电离方程式为_______ 。
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是_______ (用化学方程式表示)。
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.
ii.
①反应i中,每消耗0.3molNO2,转移电子数为_______ 。
②反应ii中,氧化剂和还原剂的物质的量之比为_______ 。
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为_______ 。
②用足量氨水吸收SO2的化学方程式为_______ 。
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。
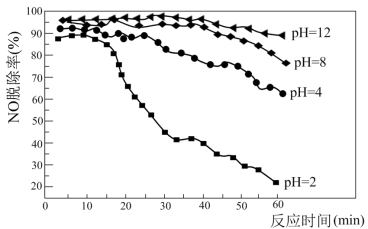
pH=2时,脱除SO2的离子方程式为_______ ;脱硝效率随反应时间的延长而逐渐降低的可能原因是_______ 。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:

(1)HNO3的电离方程式为
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.

ii.

①反应i中,每消耗0.3molNO2,转移电子数为
②反应ii中,氧化剂和还原剂的物质的量之比为
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为
②用足量氨水吸收SO2的化学方程式为
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。

pH=2时,脱除SO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】下图为一个五元环图案,小明在图案上依次写了五种物质,使图中相交的两种物质发生化学反应,A、B、C、D、E表示其相应的化学反应。

回答下列问题:
(1)反应A、B、C、D、E中属于氧化还原反应的是_______ (填字母)。
(2)上图的五个反应中,属于复分解反应的是:_______ (填字母)。
(3)反应A的离子方程式为_______ 。
(4)用双线桥分析反应B的离子方程式:_______ 。
(5)已知反应: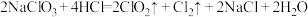 ,该反应的还原产物是
,该反应的还原产物是_______ (写化学式),该反应中氧化剂与还原剂质量之比_______ 。

回答下列问题:
(1)反应A、B、C、D、E中属于氧化还原反应的是
(2)上图的五个反应中,属于复分解反应的是:
(3)反应A的离子方程式为
(4)用双线桥分析反应B的离子方程式:
(5)已知反应:
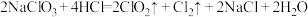 ,该反应的还原产物是
,该反应的还原产物是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】湿法制备K2FeO4的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出湿法制备K2FeO4的离子方程式
、Cl-、H2O。写出湿法制备K2FeO4的离子方程式_______ 。
 、Cl-、H2O。写出湿法制备K2FeO4的离子方程式
、Cl-、H2O。写出湿法制备K2FeO4的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列方程式
(1)完成下列物质的电离方程式
①NaHSO4(在水溶液中):___________
②)H2S:___________
(2)完成下列物质的化学方程式
①钠与水反应:___________
②铁与水蒸气反应:___________
③二氧化氮与水的反应:___________
④碳酸氢钠受热分解的反应:___________
(3)完成下列物质的水解离子方程式
①Al2(SO4)3:___________
②Na2CO3(两步):___________
(4)配平下列化学方程式
①___________ :_____KNO3+______FeCl2+_______HCl—______KCl+_______FeCl3+______NO↑+_______H2O
②___________ :_______ClO-+______Fe(OH)3+_______OH-—_____Cl-+______FeO +______H2O
+______H2O
(1)完成下列物质的电离方程式
①NaHSO4(在水溶液中):
②)H2S:
(2)完成下列物质的化学方程式
①钠与水反应:
②铁与水蒸气反应:
③二氧化氮与水的反应:
④碳酸氢钠受热分解的反应:
(3)完成下列物质的水解离子方程式
①Al2(SO4)3:
②Na2CO3(两步):
(4)配平下列化学方程式
①
②
 +______H2O
+______H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应体系,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质。
(1)该反应中,化合价升高的反应物是__ ,化合价没有发生变化的反应物是__ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)__ 。
(3)上述反应中,氧化剂是__ ,1mol氧化剂在反应中__ (填“得到”或“失去”)__ mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有__ (填“氧化性”或“还原性”)。写出该反应的离子方程式:__ 。
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
(1)该反应中,化合价升高的反应物是
(2)写出一个包含上述七种物质的氧化还原反应方程式(需配平)
(3)上述反应中,氧化剂是
(4)如果在反应后的溶液中加入NaBiO3,溶液又显紫红色。此现象说明NaBiO3具有
(提示:NaBiO3为黄色或棕色粉末,不溶于冷水,在该反应中转化为Bi3+)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】准确称取某种铁的氧化物 ,用足量的
,用足量的 进行还原,将生成的
进行还原,将生成的 全部用足量的澄清石灰水吸收,得到沉淀
全部用足量的澄清石灰水吸收,得到沉淀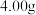 ,计算该氧化物的化学式:
,计算该氧化物的化学式:_______ 。
 ,用足量的
,用足量的 进行还原,将生成的
进行还原,将生成的 全部用足量的澄清石灰水吸收,得到沉淀
全部用足量的澄清石灰水吸收,得到沉淀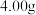 ,计算该氧化物的化学式:
,计算该氧化物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】黄铵铁矾 [化学式可表示为(NH4)xFey(SO4)z(OH)w,摩尔质量为480 g·mol-1]。Min Ristic等曾对黄铵铁矾进行热分解实验,其结果可用下图热重曲线表示(已知:黄铵铁矾在300 ℃前分解释放的物质为H2O,300~575 ℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670 ℃以上得到的是纯净的红棕色粉末)。
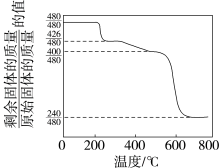
根据以上实验及图中数据确定黄铵铁矾的化学式为_______ 。

根据以上实验及图中数据确定黄铵铁矾的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是______________ ,区别该液体和FeCl3溶液的方法是______________ 。
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为________ ,若有3mol FeS2参加反应,转移________ mol电子。
(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
___ FeSO4+____ KNO3+___ H2SO4═____ K2SO4+_____ Fe2(SO4)3+__ NO↑+_____ H2O。
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为________ g。
(1)向沸水中逐滴滴加1mol·L-1FeCl3溶液至液体呈透明的红褐色,所得分散系中微粒直径的范围是
(2)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2
 Fe3O4+6SO2,氧化产物为
Fe3O4+6SO2,氧化产物为(3)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
(4)铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24L(标准状况)H2,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为
您最近一年使用:0次



