苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钾水溶液中歧化制得,反应原理为:2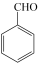 +KOH→
+KOH→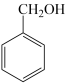 +
+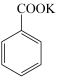 。相关信息如表所示:
。相关信息如表所示:
实验步骤:
步骤1:在250mL的锥形瓶中加入18gKOH溶于18mL水,在略低于常温的水浴中,搅拌并逐滴滴入新蒸馏过的苯甲醛21g,反应6小时,得到白色糊状物。
步骤2:将上述所得白色糊状物全部溶解于60mL水中,再加入乙醚萃取分液,每次用20mL乙醚分3次进行,合并萃取液。取上层溶液,依次加入饱和NaHSO3溶液、Na2CO3溶液、水洗涤。然后用无水K2CO3干燥、过滤,将干燥、过滤后的乙醚溶液蒸馏,收集得到纯净苯甲醇。
(1)步骤2中先将白色糊状物溶解于60mL水中,其目的是___________ 。
(2)步骤2中萃取和分液的操作应在___________ (填仪器名称)中进行。加入饱和NaHSO3溶液目的是___________ 。蒸馏时采取减压蒸馏而不是常压蒸馏的原因是___________ 。
(3)向步骤2萃取液的下层溶液中加入浓盐酸,苯甲酸完全析出并过滤得粗产品。
①将苯甲酸晶体转入漏斗中过滤时,杯壁上往往粘有少量晶体,最好选用___________ (填序号)将杯壁上的晶体冲洗下来后转入漏斗中。
A.无水乙醇 B.饱和NaCl溶液 C.70%乙醇水溶液 D.滤液
②将粗产品进一步提纯的方法如下图:

加入100mL蒸馏水时,控制温度和操作方法最佳的是___________ (填序号)。
A.低温(5℃),将KCl溶解,苯甲酸几乎不溶解
B.常温,将KCl溶解,苯甲酸溶解极少量溶解
C.95℃,将苯甲酸与KCl混合物的粗品全部溶于热的蒸馏水中,再多加5mL蒸馏水,但不冷却
D.95℃,将苯甲酸与KCl混合物的粗品全部溶于热的蒸馏水中,然后冷却到常温、结晶
(4)测定苯甲酸精品含量
称量苯甲酸精品0.3050g放入250mL的锥形瓶中,加入20mL蒸馏水,适当微热,再加入指示剂,用0.1000mol·L-1标准NaOH溶液滴定。重复实验3次,平均消耗NaOH溶液24.80mL。滴定选用的指示剂是___________ ,苯甲酸的含量为___________ %。
 +KOH→
+KOH→ +
+ 。相关信息如表所示:
。相关信息如表所示:| 物质 | 分子量 | 熔点 | 沸点 | 溶解性 | 其他性质 |
| 苯甲醛 | 106 | -26℃ | 179℃ | 微溶于水,易溶于乙醇、乙醚等 | 和NaHSO3反应,产物难溶于有机溶剂易溶于水。 |
| 苯甲醇 | 108 | -15℃ | 206℃ | 微溶于水,易溶于乙醇、乙醚等 | 加热时易分子间脱水成醚 |
| 苯甲酸 | 122 | 122℃ | 249℃ | 水中:0.34g(25℃)、2.2g(75℃),易溶于乙醇 | Ka=6.5×10-5 |
| 氯化钾 | 74.5 | 770 | 1420 | 水中:35g( 25℃)、55g(90℃) | 略 |
步骤1:在250mL的锥形瓶中加入18gKOH溶于18mL水,在略低于常温的水浴中,搅拌并逐滴滴入新蒸馏过的苯甲醛21g,反应6小时,得到白色糊状物。
步骤2:将上述所得白色糊状物全部溶解于60mL水中,再加入乙醚萃取分液,每次用20mL乙醚分3次进行,合并萃取液。取上层溶液,依次加入饱和NaHSO3溶液、Na2CO3溶液、水洗涤。然后用无水K2CO3干燥、过滤,将干燥、过滤后的乙醚溶液蒸馏,收集得到纯净苯甲醇。
(1)步骤2中先将白色糊状物溶解于60mL水中,其目的是
(2)步骤2中萃取和分液的操作应在
(3)向步骤2萃取液的下层溶液中加入浓盐酸,苯甲酸完全析出并过滤得粗产品。
①将苯甲酸晶体转入漏斗中过滤时,杯壁上往往粘有少量晶体,最好选用
A.无水乙醇 B.饱和NaCl溶液 C.70%乙醇水溶液 D.滤液
②将粗产品进一步提纯的方法如下图:

加入100mL蒸馏水时,控制温度和操作方法最佳的是
A.低温(5℃),将KCl溶解,苯甲酸几乎不溶解
B.常温,将KCl溶解,苯甲酸溶解极少量溶解
C.95℃,将苯甲酸与KCl混合物的粗品全部溶于热的蒸馏水中,再多加5mL蒸馏水,但不冷却
D.95℃,将苯甲酸与KCl混合物的粗品全部溶于热的蒸馏水中,然后冷却到常温、结晶
(4)测定苯甲酸精品含量
称量苯甲酸精品0.3050g放入250mL的锥形瓶中,加入20mL蒸馏水,适当微热,再加入指示剂,用0.1000mol·L-1标准NaOH溶液滴定。重复实验3次,平均消耗NaOH溶液24.80mL。滴定选用的指示剂是
更新时间:2022-04-08 16:01:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计实验如下:

①三颈烧瓶中加入10.00g香菇样品和400mL水;锥形瓶中加入125mL水、1mL淀粉溶液,并预加0.30mL 0.0100mol/L的碘标准溶液,搅拌。
②以0.2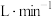 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了1.0mL碘标准溶液。
流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了1.0mL碘标准溶液。
③做空白实验,消耗了0.10mL碘标准溶液。
④用适量 替代香菇样品,重复上述步骤,测得
替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
的平均回收率为95%。
已知: ,
,
回答下列问题:
(1)装置图中仪器d的名称___________ ,仪器a的作用___________ 。
(2)三颈烧瓶适宜的规格为___________ (填标号)。
A.250mL B.500mL C.1000mL
(3)解释加入 的作用
的作用___________ 。
(4)滴定管在使用前需要___________ 、洗涤、润洗;滴定反应的离子方程式为___________ 。
(5)若先加磷酸再通氮气,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
(6)该样品中亚硫酸盐含量为___________ 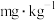 (以
(以 计,结果保留三位有效数字)。
计,结果保留三位有效数字)。

①三颈烧瓶中加入10.00g香菇样品和400mL水;锥形瓶中加入125mL水、1mL淀粉溶液,并预加0.30mL 0.0100mol/L的碘标准溶液,搅拌。
②以0.2
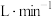 流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了1.0mL碘标准溶液。
流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液滴定,至终点时滴定消耗了1.0mL碘标准溶液。③做空白实验,消耗了0.10mL碘标准溶液。
④用适量
 替代香菇样品,重复上述步骤,测得
替代香菇样品,重复上述步骤,测得 的平均回收率为95%。
的平均回收率为95%。已知:
 ,
,
回答下列问题:
(1)装置图中仪器d的名称
(2)三颈烧瓶适宜的规格为
A.250mL B.500mL C.1000mL
(3)解释加入
 的作用
的作用(4)滴定管在使用前需要
(5)若先加磷酸再通氮气,会使测定结果
(6)该样品中亚硫酸盐含量为
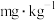 (以
(以 计,结果保留三位有效数字)。
计,结果保留三位有效数字)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室采用高温加热三氟化硼( )与氯化铝(
)与氯化铝(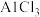 )的方法制备
)的方法制备 ,装置如图所示(夹持装置及加热装置略),已知
,装置如图所示(夹持装置及加热装置略),已知 与
与 均易与水反应,
均易与水反应, 沸点低、易升华。
沸点低、易升华。
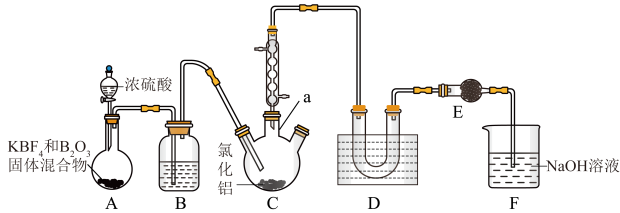
部分物质的沸点如表所示:
回答下列问题:
(1)仪器a的名称为_______ 。
(2)氟硼酸钾(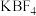 )中阴离子的空间结构为
)中阴离子的空间结构为_______ 形。实验中滴入浓硫酸并加热装置A,除产生气体外,还生成一种酸式盐,写出反应的化学方程式:_______ 。
(3)装置F的作用为_______ 。
(4)实验开始时,A、C两处加热装置应先加热A处,原因是_______ 。
(5)装置D采用的是_______ (填“水浴加热”或“冷水浴”)。
(6) 产品中氯元素含量的测定:称取a g样品置于蒸馏水中完全水解,并配成250mL溶液,量取25.00mL于锥形瓶中,向其中加入
产品中氯元素含量的测定:称取a g样品置于蒸馏水中完全水解,并配成250mL溶液,量取25.00mL于锥形瓶中,向其中加入 mL
mL 

 溶液使
溶液使 充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴
充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴 溶液,用
溶液,用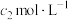 KSCN标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗KSCN标准溶液的体积为
KSCN标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗KSCN标准溶液的体积为 mL,则产品中氯元素含量为
mL,则产品中氯元素含量为_______ (列出计算式即可)。(已知: )
)
 )与氯化铝(
)与氯化铝(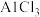 )的方法制备
)的方法制备 ,装置如图所示(夹持装置及加热装置略),已知
,装置如图所示(夹持装置及加热装置略),已知 与
与 均易与水反应,
均易与水反应, 沸点低、易升华。
沸点低、易升华。
部分物质的沸点如表所示:
| 物质 |  |  | 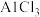 |
| 沸点/℃ | -101 | 12.5 | 180 |
(1)仪器a的名称为
(2)氟硼酸钾(
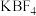 )中阴离子的空间结构为
)中阴离子的空间结构为(3)装置F的作用为
(4)实验开始时,A、C两处加热装置应先加热A处,原因是
(5)装置D采用的是
(6)
 产品中氯元素含量的测定:称取a g样品置于蒸馏水中完全水解,并配成250mL溶液,量取25.00mL于锥形瓶中,向其中加入
产品中氯元素含量的测定:称取a g样品置于蒸馏水中完全水解,并配成250mL溶液,量取25.00mL于锥形瓶中,向其中加入 mL
mL 

 溶液使
溶液使 充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴
充分沉淀,加入一定量硝基苯用力振荡,静置后,滴加几滴 溶液,用
溶液,用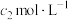 KSCN标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗KSCN标准溶液的体积为
KSCN标准溶液滴定至溶液变为红色且半分钟内不褪色,消耗KSCN标准溶液的体积为 mL,则产品中氯元素含量为
mL,则产品中氯元素含量为 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室模仿工业上生产过氧化钙的主要流程如下:
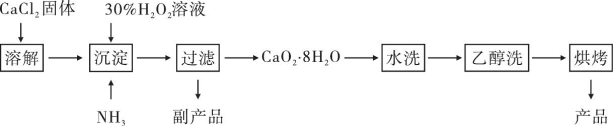
已知:①沉淀时需控制温度为0℃左右;
②CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)实验装置如下:
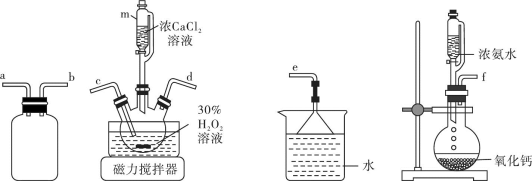
①过氧化钙的电子式为_______ 。图中使用的两种烧瓶的名称分别为_______ 、_______ 。
②沉淀步骤需控制温度为0℃左右,控温直接有效的方法是_______ 。
③装置连接顺序为_______ (填接口字母)。
④产生沉淀的化学方程式为_______ 。
(2)用无水乙醇洗涤的目的是_______ 。
(3)产品纯度测定实验步骤如下:
产品纯度测定:第一步:准确称取ag产品于有塞锥形瓶中,加入适量的蒸馏水和bgKI晶体(过量)。再滴入量盐酸溶液充分反应。
第二步:向锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为cmol·L-1的Na2S2O3溶液至滴定终点,消耗Na2S2O3溶液VmL。(已知: I2+2 =2I -+
=2I -+ )。
)。
①滴定终点判断标志_______ 。
②产品(CaO2)的纯度为_______ (列出计算式)。

已知:①沉淀时需控制温度为0℃左右;
②CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)实验装置如下:

①过氧化钙的电子式为
②沉淀步骤需控制温度为0℃左右,控温直接有效的方法是
③装置连接顺序为
④产生沉淀的化学方程式为
(2)用无水乙醇洗涤的目的是
(3)产品纯度测定实验步骤如下:
产品纯度测定:第一步:准确称取ag产品于有塞锥形瓶中,加入适量的蒸馏水和bgKI晶体(过量)。再滴入量盐酸溶液充分反应。
第二步:向锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为cmol·L-1的Na2S2O3溶液至滴定终点,消耗Na2S2O3溶液VmL。(已知: I2+2
 =2I -+
=2I -+ )。
)。①滴定终点判断标志
②产品(CaO2)的纯度为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】某芳香烃 是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体
是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体 等多种物质。
等多种物质。

已知: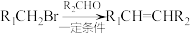
(1)由 转化为
转化为 的反应类型是
的反应类型是___________ 。
(2)扁桃酸中所含官能团的名称___________ ;可以准确判断其中所含官能团的方法是___________ (填序号)。
a.质谱 b.核磁共振氢谱 c.红外光谱 d.x射线衍射
(3) 的名称是
的名称是___________ 。
(4)写出由单体 通过某种聚合反应所得产物的结构简式
通过某种聚合反应所得产物的结构简式___________ 。
(5) 有多种同分异构体,同时满足下列条件的同分异构体有
有多种同分异构体,同时满足下列条件的同分异构体有___________ 种(不考虑立体异构)。
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
(6)已知 ,某兴趣小组拟用
,某兴趣小组拟用 合成阿司匹林前体水杨酸
合成阿司匹林前体水杨酸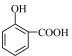 ,合成路线如图所示:
,合成路线如图所示:

写出由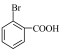 生成
生成 发生反应的化学方程式
发生反应的化学方程式___________ 。
 是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体
是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体 等多种物质。
等多种物质。
已知:
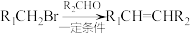
(1)由
 转化为
转化为 的反应类型是
的反应类型是(2)扁桃酸中所含官能团的名称
a.质谱 b.核磁共振氢谱 c.红外光谱 d.x射线衍射
(3)
 的名称是
的名称是(4)写出由单体
 通过某种聚合反应所得产物的结构简式
通过某种聚合反应所得产物的结构简式(5)
 有多种同分异构体,同时满足下列条件的同分异构体有
有多种同分异构体,同时满足下列条件的同分异构体有①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
(6)已知
 ,某兴趣小组拟用
,某兴趣小组拟用 合成阿司匹林前体水杨酸
合成阿司匹林前体水杨酸 ,合成路线如图所示:
,合成路线如图所示:
写出由
 生成
生成 发生反应的化学方程式
发生反应的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】某研究小组以对氨基水杨酸和乙炔为主要原料,按下列路线合成便秘治疗药物——琥珀酸普卡必利。
已知:①化合物B中含有羟基;
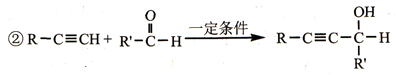
请回答:
(1)下列说法不正确的是_________
A.对氨基水杨酸能发生缩聚反应生成高分子化合物
B.化合物B能发生氧化反应,不能发生还原反应
C.化合物C能形成内盐
D.化合物F能与NaHCO3溶液反应
(2)化合物B的结构简式是_________ 。
(3)C+D→E的化学方程式是____________ 。
(4)写出同时符合下列条件的A 的所有同分异构体的结构简式_________ 。
①分子中含有硝基且直接连在苯环上
②1H-NMR谱显示苯环上有两种示同花学环境的氢原子
③不能与FeCl3溶液发生显色反应
(5)设计以乙炔和甲醛为原料制备化合物F的合成路线(用流程图表示,无机试剂任选)_________________ 。
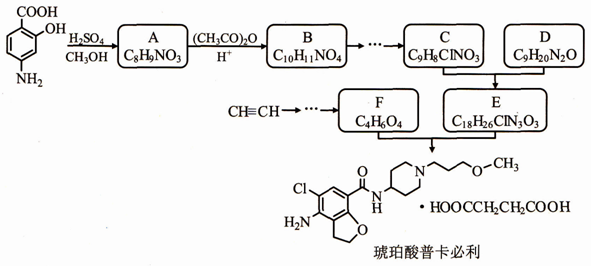
已知:①化合物B中含有羟基;
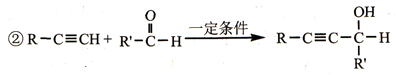
请回答:
(1)下列说法不正确的是
A.对氨基水杨酸能发生缩聚反应生成高分子化合物
B.化合物B能发生氧化反应,不能发生还原反应
C.化合物C能形成内盐
D.化合物F能与NaHCO3溶液反应
(2)化合物B的结构简式是
(3)C+D→E的化学方程式是
(4)写出同时符合下列条件的A 的所有同分异构体的结构简式
①分子中含有硝基且直接连在苯环上
②1H-NMR谱显示苯环上有两种示同花学环境的氢原子
③不能与FeCl3溶液发生显色反应
(5)设计以乙炔和甲醛为原料制备化合物F的合成路线(用流程图表示,无机试剂任选)
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
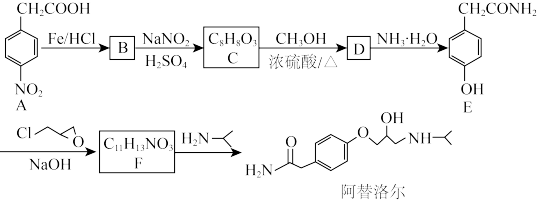
【推荐3】某研究小组按下列路线合成治疗高血压药阿替洛尔:
已知: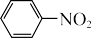

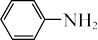
回答下列问题:
(1)A的化学名称为_______ 。
(2)阿替洛尔的分子式_______ 。
(3)A→B的反应类型为_______ ;C的结构简式为_______ 。
(4)写出F-阿替洛尔的化学方程式:_______ 。
(5)E有多种同分异构体,同时满足下列条件的同分异构体有_______ 种(不包括立体异构);其中核磁共振氢谱显示有5组峰,且峰面积之比为1:2:2:2:2的结构简式为_______ (任写一种)。
①含有苯环和-NH2;
②能与碳酸氢钠反应产生CO2气体。

已知:
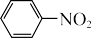

回答下列问题:
(1)A的化学名称为
(2)阿替洛尔的分子式
(3)A→B的反应类型为
(4)写出F-阿替洛尔的化学方程式:
(5)E有多种同分异构体,同时满足下列条件的同分异构体有
①含有苯环和-NH2;
②能与碳酸氢钠反应产生CO2气体。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学生查阅资料得知溴乙烷的物理性质与制取方法如下表:
制取溴乙烷的化学方程式:C2H5OH+HBr C2H5Br+H2O
C2H5Br+H2O
联想所学溴苯的制取,他设计了制取溴苯和溴乙烷的装置(如下图),主要实验步骤如下:

①检查气密性后,向烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓硫酸的混合液至恰好于进气导管口。
③将A装置中的纯铁丝向下插入混合液中。
④点燃B装置中酒精灯,且小火缓缓对锥形瓶加热10min。
请填写下列空白:
(1)写出A中发生反应的方程式:_____ 。
(2)装置长导管a的作用是_____ 。
(3)C装置中的U形管内用蒸馏水封住管底的作用是_____ 。
(4)反应完毕后,U形管内的现象是_____ ;分离出溴乙烷时所用的最主要的仪器名称是_____ (只填一种)。
(5)粗溴苯的精制常进行如下操作:a.蒸馏b.水洗、分液c.用干燥剂干燥d.10%的NaOH溶液碱洗、分液。正确的操作顺序是_____。
| 物理性质 | 颜色 | 状态 | 溶解性 | 熔点 | 沸点 | 密度 |
| 溴乙烷 | 无色 | 液体 | 难溶于水 | 38.4℃ | 119℃ | 1.46g/cm3 |
 C2H5Br+H2O
C2H5Br+H2O联想所学溴苯的制取,他设计了制取溴苯和溴乙烷的装置(如下图),主要实验步骤如下:

①检查气密性后,向烧瓶中加入一定量的苯和液溴。
②向锥形瓶中加入乙醇和浓硫酸的混合液至恰好于进气导管口。
③将A装置中的纯铁丝向下插入混合液中。
④点燃B装置中酒精灯,且小火缓缓对锥形瓶加热10min。
请填写下列空白:
(1)写出A中发生反应的方程式:
(2)装置长导管a的作用是
(3)C装置中的U形管内用蒸馏水封住管底的作用是
(4)反应完毕后,U形管内的现象是
(5)粗溴苯的精制常进行如下操作:a.蒸馏b.水洗、分液c.用干燥剂干燥d.10%的NaOH溶液碱洗、分液。正确的操作顺序是_____。
| A.abcdb | B.bdbca | C.dbcab | D.bdabc |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】亚硝酰硫酸(NOSO4H)是一种浅黄色或蓝紫色液体,遇水分解,溶于浓硫酸不分解,主要用于染料、医药领域的重氮化反应中取代亚硝酸钠,有效降低硫酸使用量,增加反应的流动性,不产生无机盐,从而可以降低成本,提高产品质量,使染料成品色泽鲜艳、固色能力强,并减少污水。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。

(1)装置B中浓HNO3与SO2在浓作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了加快搅拌速度外,还可以将三颈烧瓶置于___ 中。
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是________ 。
③该实验装置存在可能导致NOSO4H产量降低的缺陷是____________ 。
④已知亚硝酸不稳定、易分解,发生反应2HNO2=NO2+NO+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式__________ .
(2)测定亚硝酰硫酸(NOSO4H)的纯度
准确称取1.380g产品放入250ml的碘量瓶中,加入60.00ml 0.1000mol/L KMnO4标准溶液和10ml25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500mol/L 的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00ml.已知:2KMnO4+5NOSO4H+2H2O=K2SO4+5HNO2+2MnSO4+2H2SO4。求亚硝酰硫酸(NOSO4H)的纯度_________ 。(计算结果保留四位有效数字。M(NOSO4H)=127g/mol)

(1)装置B中浓HNO3与SO2在浓作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了加快搅拌速度外,还可以将三颈烧瓶置于
②开始时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
③该实验装置存在可能导致NOSO4H产量降低的缺陷是
④已知亚硝酸不稳定、易分解,发生反应2HNO2=NO2+NO+H2O。请写出NOSO4H遇水分解时发生反应的化学方程式
(2)测定亚硝酰硫酸(NOSO4H)的纯度
准确称取1.380g产品放入250ml的碘量瓶中,加入60.00ml 0.1000mol/L KMnO4标准溶液和10ml25%的H2SO4溶液,然后摇匀(过程中无气体产生)。用0.2500mol/L 的草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00ml.已知:2KMnO4+5NOSO4H+2H2O=K2SO4+5HNO2+2MnSO4+2H2SO4。求亚硝酰硫酸(NOSO4H)的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,反应式为:2 +NaOH
+NaOH
 +
+ ,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:

重结晶过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。请根据以上信息,回答问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是_______ ,其理由是_______ 充分萃取并静置分层,打开分液漏斗上口的玻璃塞后,上、下层依次分离。
(2)苯甲酸在A、B、C三种溶剂中的溶解度(s)随温度变化的曲线如下图所示:

①重结晶时,合适的溶剂是_______ (填字母)。
②洗涤时采用的合适洗涤剂是_______ (填字母)。
A.饱和食盐水 B.Na2CO3溶液 C.稀硫酸 D.蒸馏水
(3)如图是减压过滤装置,请指出其中一处明显错误:_______ 。

 +NaOH
+NaOH
 +
+ ,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
,某研究小组在实验室制备苯甲醇与苯甲酸,反应结束后对反应液按下列步骤处理:
重结晶过程:溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
已知:苯甲醇易溶于乙醚、乙醇,在水中溶解度较小。请根据以上信息,回答问题:
(1)萃取分离苯甲醇与苯甲酸钠时,合适的萃取剂是
(2)苯甲酸在A、B、C三种溶剂中的溶解度(s)随温度变化的曲线如下图所示:

①重结晶时,合适的溶剂是
②洗涤时采用的合适洗涤剂是
A.饱和食盐水 B.Na2CO3溶液 C.稀硫酸 D.蒸馏水
(3)如图是减压过滤装置,请指出其中一处明显错误:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】甲苯( )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛( )、苯甲酸(
)、苯甲酸( )等产品。表列出了有关物质的部分物理性质,请回答:
)等产品。表列出了有关物质的部分物理性质,请回答:
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是______________ 。
(2)三颈瓶中发生反应的化学方程式为_______________________________________ 。
(3)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是_____________________________________________ 。
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过_____ 、_____ (填操作名称)等操作,才能得到苯甲醛粗产品。
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是_______ (按步骤顺序填字母)。
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/L KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为_____ 。【苯甲酸相对分子质量:122.0】
 )是一种重要的化工原料,能用于生产苯甲醛(
)是一种重要的化工原料,能用于生产苯甲醛( )、苯甲酸(
)、苯甲酸( )等产品。表列出了有关物质的部分物理性质,请回答:
)等产品。表列出了有关物质的部分物理性质,请回答:| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 (ρ水=1g/cm3) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
注:甲苯、苯甲醛、苯甲酸三者互溶。
实验室可用如图装置模拟制备苯甲醛。实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸(作为溶剂)和2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时。

(1)装置a的名称是
(2)三颈瓶中发生反应的化学方程式为
(3)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是
(4)反应完毕后,反应混合液经过自然冷却至室温时,还应经过
(5)实验中加入过量过氧化氢且反应时间较长,会使苯甲醛产品中产生较多的苯甲酸。
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加入盐酸调节pH=2 d.加入适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于200mL乙醇配成溶液,量取所得的乙醇溶液20.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/L KOH标准液滴定,到达滴定终点时消耗KOH溶液18.00mL。产品中苯甲酸的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】难溶络合物X由3种元素组成,某实验小组按如下流程进行相关实验:

已知:反应①生成两种正盐及一种弱酸,E是空气中含量最多的气体。
(1)X所含元素有____________ (填元素符号),X的化学式为____________ 。
(2)写出反应①的离子方程式____________ 。
(3)已知反应①中生成的弱酸有剧毒,工业上常采用碱性氯化法处理该物质,处理过程分两个阶段,请写出第二阶段(即反应②)的化学方程式____________ 。
(4)请设计实验检验溶液A中的金属阳离子____________ 。

已知:反应①生成两种正盐及一种弱酸,E是空气中含量最多的气体。
(1)X所含元素有
(2)写出反应①的离子方程式
(3)已知反应①中生成的弱酸有剧毒,工业上常采用碱性氯化法处理该物质,处理过程分两个阶段,请写出第二阶段(即反应②)的化学方程式
(4)请设计实验检验溶液A中的金属阳离子
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】阴阳离子比为1:2的固体离子化合物X由3种元素组成,某学习小组开展如下探究实验:
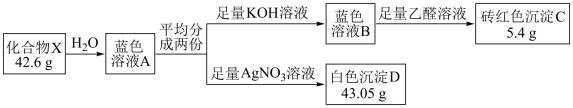
已知,溶液B中仅有一种阳离子(氢离子除外),溶液B中的某种溶质阴离子结构与化合物X阴离子结构相似,C、D均为纯净物。请回答:
(1)砖红色沉淀C的化学式为___________ 。
(2)化合物X的化学式为___________ 。
(3)蓝色溶液B中含有的溶质是___________ (用化学式表示)。
(4)写出溶液B与乙醛反应的离子方程式___________ 。
(5)某同学怀疑砖红色沉淀中可能含有Cu单质,请设计实验验证此猜想___________ 。

已知,溶液B中仅有一种阳离子(氢离子除外),溶液B中的某种溶质阴离子结构与化合物X阴离子结构相似,C、D均为纯净物。请回答:
(1)砖红色沉淀C的化学式为
(2)化合物X的化学式为
(3)蓝色溶液B中含有的溶质是
(4)写出溶液B与乙醛反应的离子方程式
(5)某同学怀疑砖红色沉淀中可能含有Cu单质,请设计实验验证此猜想
您最近一年使用:0次



