已知X、Y、Z、W、Q是前四周期的核电荷数依次增大的元素,X的价电子层中有3个未成对电子,X与Z同主族;Y与W同主族,W元素原子M层有两对成对电子;Q的最外层只有1个电子,但次外层有18个电子。
(1)X、Y、W的第一电离能由大到小的顺序是_______ (填字母对应的元素符号)。
(2)已知元素Z的某钾盐(KH2ZO4)是其酸(H3ZO2)的正盐,则酸H3ZO2的结构式为_______ (元素Z用对应的元素符号书写)。
(3)某同学画出基态碳原子的核外电子排布图: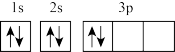 ,该电子排布图违背了
,该电子排布图违背了_______ ;
(4)元素W的含氧酸根离子(WO )的空间构型为
)的空间构型为_______ ,与之互为等电子体的阴离子有_______ (写出一种离子符号;等电子体指化学通式相同且价电子总数相等的分子或离子)。
(5)对于基态Q原子,下列叙述正确的是_______(填标号)。
(6)配合物CrCl3·6H2O中心离子Cr3+的配位数为6,向含0.1molCrCl3·6H2O的溶液中滴加2mol·L-1AgNO3溶液,反应完全后共消耗AgNO3溶液50mL,则配合物的化学式应该写为_______ 。
(1)X、Y、W的第一电离能由大到小的顺序是
(2)已知元素Z的某钾盐(KH2ZO4)是其酸(H3ZO2)的正盐,则酸H3ZO2的结构式为
(3)某同学画出基态碳原子的核外电子排布图:
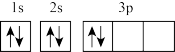 ,该电子排布图违背了
,该电子排布图违背了(4)元素W的含氧酸根离子(WO
 )的空间构型为
)的空间构型为(5)对于基态Q原子,下列叙述正确的是_______(填标号)。
| A.遵循能量最低原理,核外电子排布应为[Ar]3d94s2 |
| B.排布在外层的电子总是比排布在内层的电子离核更远 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
| D.电子先排入4s轨道,再排进3d轨道,故3d轨道的电子能量比4s高 |
更新时间:2022-04-08 21:30:32
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】原子序数依次增大的A、B、C、D、E、F五种元素的原子位于前四周期,A元素原子核外有三种不同能级且各个能级所填充的电子数相同,C原子的核外已成对的电子数是未成对电子数的3倍;D核内质子数比E少1;E与C同主族;F2+的M能层里电子全满。
(1)B元素的名称为_____ ,F元素基态原子的价电子排布式为_____ 。
(2)元素A、B、C第一电离能顺序为_____ (填元素符号)。
(3)C与E分别形成的最简单氢化物沸点高低顺序为_____ (用化学式表示),原因是______ 。
(4)D与溴形成的化合物DBr5,加压条件下95℃液化,发生完全电离得到一种能够导电的液体,经测定,该熔体中含有一种正四面体结构的阳离子和Br-,请写出该条件下DBr5电离的电离方程式____ 。该熔体中阳离子的中心原子的杂化方式为_____ 。
(5)请写出E的两种常见氧化物的分子空间构型:_____ ,____ 。

(6)F与E形成的离子晶体晶胞如图所示,该晶体的化学式为______ (用元素符号表示);若晶体的密度为ρ g/cm3,则该晶胞的棱长为_____ pm。
(1)B元素的名称为
(2)元素A、B、C第一电离能顺序为
(3)C与E分别形成的最简单氢化物沸点高低顺序为
(4)D与溴形成的化合物DBr5,加压条件下95℃液化,发生完全电离得到一种能够导电的液体,经测定,该熔体中含有一种正四面体结构的阳离子和Br-,请写出该条件下DBr5电离的电离方程式
(5)请写出E的两种常见氧化物的分子空间构型:

(6)F与E形成的离子晶体晶胞如图所示,该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】铜是人类最早发现并广泛使用的一种金属。回答下列问题:
(1)黄铜矿(CuFeS2)是其中铜的主要存在形式。CuFeS2中存在的化学键类型是___________ 。试比较组成黄铁矿的三种组成元素的电负性的相对强弱__________ 。
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①则X是__________ (填名称),X分子的立体构型是______ ,中心原子杂化类型为___ 。
②X的沸点比水的沸点____ (填“高”、“低"),主要原因是___________ 。
(3)[Cu(NH3)4]2+中,提供孤对电子的是_________ 。Cu(NH3)2Cl2有两种同分异构体,其中种可溶于水,则此种化合物是_____ (填“极性"或“非极性")分子,由此推知[Cu(NH3)4]2+的空间构型是____________ 。
(4)某镍白铜合金的立方晶胞结构如图所示:
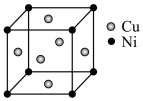
①晶胞中铜原子与镍原子的数量比为__________ 。
②若合金的密度为d g/cm3,晶胞参数a=_____ nm。(设NA代表阿伏加德罗常数)
(1)黄铜矿(CuFeS2)是其中铜的主要存在形式。CuFeS2中存在的化学键类型是
(2)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①则X是
②X的沸点比水的沸点
(3)[Cu(NH3)4]2+中,提供孤对电子的是
(4)某镍白铜合金的立方晶胞结构如图所示:

①晶胞中铜原子与镍原子的数量比为
②若合金的密度为d g/cm3,晶胞参数a=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】科学家预测21世纪中叶将进入“氢能经济”时代,许多化合物或合金都是具有广阔应用前景的储氢材料。回答下列问题:
(1)基态Li原子核外电子有___ 种不同的运动状态,占据最高能层电子的电子云轮廓图形状为__ 。
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为__________ 。
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是_________ 。
(4)咔唑( )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是_______ 。
(5)NH3BH3 (氨硼烷,熔点104℃)与______ (写出一种分子)互为等电子体。可通过红外光谱测定该分子的立体构型,NH3BH3中B的杂化轨道类型为________ 。
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu原子处于面心,Au原子处于顶点位置。该晶体中,原子之间的作用力是_______ 。实现储氢功能时,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为______ 。

(1)基态Li原子核外电子有
(2)Li的焰色反应为紫红色,很多金属元素能产生焰色反应的原因为
(3)亚氨基锂(Li2NH) 中所含的元素,电负性由大到小排列的顺序是
(4)咔唑(
 )的沸点比芴(
)的沸点比芴( )高的主要原因是
)高的主要原因是(5)NH3BH3 (氨硼烷,熔点104℃)与
(6)一种储氢合金的晶胞结构如图所示。在晶胞中Cu原子处于面心,Au原子处于顶点位置。该晶体中,原子之间的作用力是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】元素A、B、C、D、E的原子序数依次增大,且均小于36。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;D的价电子数为2且与E同周期;E的基态原子的内部各能层均排满,且4s能级有1个单电子。回答下列问题:
(1)基态E原子的价电子排布式为____________________
(2)A、B、C三种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)与A的单质分子互为等电子体的分子和离子分别是________ (用分子和离子符号表示)。AB2的空间构型为___________ ,其中A原子的杂化类型是_______________
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是_____________
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为____________
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=______________ cm(用含ρ、NA的计算式表示)。

(1)基态E原子的价电子排布式为
(2)A、B、C三种元素第一电离能由大到小的顺序为
(3)与A的单质分子互为等电子体的分子和离子分别是
(4)B元素简单氢化物的沸点是同族元素中最高的,原因是
(5)向含E元素的硫酸盐溶液中加入过量氨水,可得到深蓝色透明溶液。向溶液中加入乙醇,将析出深蓝色晶体。该晶体的化学式为[Cu(NH3)4]SO4∙H2O晶体中阳离子的结构式为
(6)C和D形成化合物的晶胞结构如图所示,已知晶体的密度为ρg/cm,阿伏加 德罗常数为NA,则晶胞边长a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知:周期表中前四周期的六种元素A、B、C、D、E、F核电荷数依次增大,其中A原子核外有三个未成对电子:化合物B2E的晶体为离子晶体,E原子核外的M层中有两对成对电子:C元素是底壳中含量最高的金属元素:D单质的熔点在同周期元素形成的单质中是最高的:F2+离子核外各层电子均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为______ (用元素符号表示)
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是______ 。
(3)E的最高价氧化物分子的空间构型是______ 。是______ 分子(填“极性”“非极性”)
(4)F原子的价层电子排布式是_____ 。
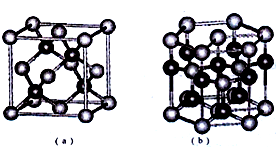
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子)。其化学式为_____ 。(a)中E原子的配位数为______ ,若在(b)的结构中取出一个平行六面体作为晶胞,则平均一个晶胞中含有_____ 个F原子。结构(a)与(b)中晶胞的原子空间利用率相比,(a)________ (b)(填“>”“<”或“=”)
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)B的氯化物的熔点比D的氯化物的熔点高,理由是
(3)E的最高价氧化物分子的空间构型是
(4)F原子的价层电子排布式是
(5)E、F形成某种化合物有如图所示两种晶体结构(深色球表示F原子)。其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碳、氮、氧、磷、硫、铁,锌、铜等都是组成蛋白质的重要元素。回答下列问题:
(1)Fe的基态原子的核外电子排布式为______ 。
(2)在C、N、O、P、S五种元素中,第一电离能最大的元素是______ (填元素符号,下同),电负性最大的元素是______
(3)氨基乙酸(H2NCH2COOH)是蛋白质完全水解的产物之一,其中C原子的杂化轨道类型为______ ;1molH2NCH2COOH中含有σ键的数目为______ NA。
(4)蛋白质在体内部分被氧化生成尿素[CO(NH2)2]、二氧化碳、水等排出体外。
①H2O分子的空间构型为______ 。
②尿素易溶于水,其原因除都是极性分子外,还有______ 。
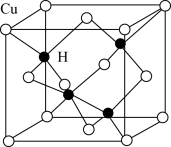
(5)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为______ 。若该晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则该晶胞的棱长为______ nm(用含ρ和NA的式子表示)
(1)Fe的基态原子的核外电子排布式为
(2)在C、N、O、P、S五种元素中,第一电离能最大的元素是
(3)氨基乙酸(H2NCH2COOH)是蛋白质完全水解的产物之一,其中C原子的杂化轨道类型为
(4)蛋白质在体内部分被氧化生成尿素[CO(NH2)2]、二氧化碳、水等排出体外。
①H2O分子的空间构型为
②尿素易溶于水,其原因除都是极性分子外,还有
(5)Cu与H元素形成某种晶体的结构如图所示,则该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】钛酸锌锂(Li2ZnTi3O8)是锂离子电池电极材料的一种,具有循环性能良好、安全性能优异、结构性能稳定的优点,可以通过TiO2、Li2CO3、(CH3COO)2Zn·2H2O等原料,采用高温固相法合成。请回答下列问题:
(1)基态Ti原子的价电子排布式为_______ ,第四周期的基态原子中,未成对电子数与基态Ti原子相等的元素有_______ (填元素符号)。
(2)CH3COO−中含有的σ键和π键的个数比为_______ ;在Li2CO3中,三种元素的第一电离能从大到小的顺序是_______ 。
(3)Ti与Zn原子都采用六方最密堆积形成金属晶体,两者半径大小相近:Ti(144.8 pm)、Zn(133.3 pm),但金属Ti的熔点(1660℃)比Zn(419.53℃)高得多,原因是_______ 。
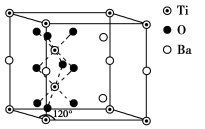
(4)某六方晶系的一种钛钡矿石的晶胞如图所示,距离晶胞内的钛原子最近的氧原子有_______ 个,Ti原子可看成填充在周围的氧原子组成的正八面体空隙中,则其O—Ti—O的键角为_______ (填度数)。设该六方晶胞的棱长分别记为a cm、b cm、c cm,阿伏加德罗常数的值为NA,该晶胞密度的表达式为_______ g·cm−3。
(1)基态Ti原子的价电子排布式为
(2)CH3COO−中含有的σ键和π键的个数比为
(3)Ti与Zn原子都采用六方最密堆积形成金属晶体,两者半径大小相近:Ti(144.8 pm)、Zn(133.3 pm),但金属Ti的熔点(1660℃)比Zn(419.53℃)高得多,原因是
(4)某六方晶系的一种钛钡矿石的晶胞如图所示,距离晶胞内的钛原子最近的氧原子有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】半导体产业是全球经济增长的支柱产业。半导体材料经历“元素半导体”到“化合物半导体”的发展。
I.第一代元素半导体以Si、Ge为代表。
(1)基态Si原子的价电子轨道表示式为_____ ;基态Ge原子核外电子占据最高能级的电子云轮廓图为_____ 形。
II.第二代化合物半导体以GaAs、GaN等为代表。砷化镓 太阳能电池为我国“玉兔二号”月球车提供充足能量;GaN手机快充充电器受到广大消费者的喜爱。
太阳能电池为我国“玉兔二号”月球车提供充足能量;GaN手机快充充电器受到广大消费者的喜爱。
(2)N、Ga、As的第一电离能由大到小的顺序是_____  。
。
(3)GaAs可由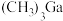 和
和 反应制得。在常温常压下,
反应制得。在常温常压下,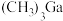 为无色透明液体,则
为无色透明液体,则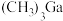 固体属于
固体属于____ 晶体,(CH3)3Ga中Ga原子的杂化方式为____ ; 分子的空间构型为
分子的空间构型为_____ ;与 互为等电子体的一种微粒为
互为等电子体的一种微粒为_____ 。
(4)砷化镓的立方晶胞结构如图所示。
①砷化镓晶体属于原子晶体。该晶体中____  填“有”或“无”
填“有”或“无” 配位键存在。GaN、GaP、GaAs具有相同的晶体类型,熔点如下表所示,分析其变化原因:
配位键存在。GaN、GaP、GaAs具有相同的晶体类型,熔点如下表所示,分析其变化原因:______ 。
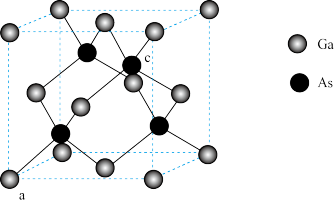
②原子坐标参数是晶胞的基本要素之一,表示晶胞内部各原子的相对位置。图中a(0,0,0)、b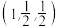 ,则c原子的坐标参数为
,则c原子的坐标参数为_____ 。
③砷化镓的摩尔质量为M g·mol-1,Ga的原子半径为pnm,则砷化镓晶体的密度为_______ g·cm-3。
I.第一代元素半导体以Si、Ge为代表。
(1)基态Si原子的价电子轨道表示式为
II.第二代化合物半导体以GaAs、GaN等为代表。砷化镓
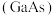 太阳能电池为我国“玉兔二号”月球车提供充足能量;GaN手机快充充电器受到广大消费者的喜爱。
太阳能电池为我国“玉兔二号”月球车提供充足能量;GaN手机快充充电器受到广大消费者的喜爱。(2)N、Ga、As的第一电离能由大到小的顺序是
 。
。(3)GaAs可由
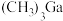 和
和 反应制得。在常温常压下,
反应制得。在常温常压下,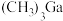 为无色透明液体,则
为无色透明液体,则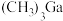 固体属于
固体属于 分子的空间构型为
分子的空间构型为 互为等电子体的一种微粒为
互为等电子体的一种微粒为(4)砷化镓的立方晶胞结构如图所示。
①砷化镓晶体属于原子晶体。该晶体中
 填“有”或“无”
填“有”或“无” 配位键存在。GaN、GaP、GaAs具有相同的晶体类型,熔点如下表所示,分析其变化原因:
配位键存在。GaN、GaP、GaAs具有相同的晶体类型,熔点如下表所示,分析其变化原因:| 晶体 | GaN | GaP | GaAs |
熔点 | 1700 | 1480 | 1238 |

②原子坐标参数是晶胞的基本要素之一,表示晶胞内部各原子的相对位置。图中a(0,0,0)、b
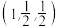 ,则c原子的坐标参数为
,则c原子的坐标参数为③砷化镓的摩尔质量为M g·mol-1,Ga的原子半径为pnm,则砷化镓晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,J元素的焰色试验呈黄色,Q的最外层电子数与其电子总数之比为3∶8,X能与J形成离子化合物,且J+的半径大于X—的半径,Y的氧化物是形成酸雨的主要物质之一。请回答:
(1)Q元素在周期表中的位置为__ 。
(2)将这五种元素的原子半径从大到小排列,排在第三的元素是__ (填元素符号)。
(3)元素的非金属性Z__ (填“>”或“<”)Q。下列各项中,不能说明这一结论的事实有__ (填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,该阳离子的中心原子的杂化方式为__ ,与该离子互为等电子体的是__ (填一个即可);A的键角__ B的键角(填“大于”或“小于”);X与Q形成的化合物易溶于水,原因是__ 。
(1)Q元素在周期表中的位置为
(2)将这五种元素的原子半径从大到小排列,排在第三的元素是
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,该阳离子的中心原子的杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】物质结构与性质自然界中存在大量的金属元素,其中镁、铜、锌等在工农业生产中有着广泛的应用。
(1)金属A的原子只有3个电子层,其第一至第四电离能(kJ/mol)如下表,则A原子的核外电子排布式为_______ 。
(2)向硫酸铜溶液中逐滴滴加浓氨水,先出现蓝色絮状沉淀,后沉淀逐渐溶解得到 深蓝色透明溶液。在
深蓝色透明溶液。在 中含有的化学键为
中含有的化学键为_______ ,游离的 分子相比,其H—N—H键角
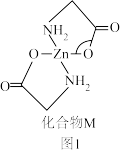
分子相比,其H—N—H键角_______ (填“较大,“较小”或“相同”)。 也能形成一种补锌剂化合物M(图1),化合物M中配位原子是
也能形成一种补锌剂化合物M(图1),化合物M中配位原子是_______ ,配位数为_______ 。
(3)Zn的某种硫化物的晶胞如图2所示,由图可知, 位于
位于 所围成的
所围成的_______ ,空隙中(填“四面体”或“八面体”)。已知晶体密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的边长表达式为
,则该晶胞的边长表达式为_______ pm(写计算表达式)。

(4) 的熔点为283℃,验证
的熔点为283℃,验证 晶体类型的实验方案为
晶体类型的实验方案为_______ 。
(1)金属A的原子只有3个电子层,其第一至第四电离能(kJ/mol)如下表,则A原子的核外电子排布式为
 |  |  |  |
| 932 | 1821 | 15390 | 21771 |
(2)向硫酸铜溶液中逐滴滴加浓氨水,先出现蓝色絮状沉淀,后沉淀逐渐溶解得到
 深蓝色透明溶液。在
深蓝色透明溶液。在 中含有的化学键为
中含有的化学键为 分子相比,其H—N—H键角
分子相比,其H—N—H键角 也能形成一种补锌剂化合物M(图1),化合物M中配位原子是
也能形成一种补锌剂化合物M(图1),化合物M中配位原子是
(3)Zn的某种硫化物的晶胞如图2所示,由图可知,
 位于
位于 所围成的
所围成的 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的边长表达式为
,则该晶胞的边长表达式为
(4)
 的熔点为283℃,验证
的熔点为283℃,验证 晶体类型的实验方案为
晶体类型的实验方案为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___ ,3d能级上的未成对电子数为___ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___ ,提供孤电子对的成键原子是___ 。
③氨的沸点___ (填“高于”或“低于”)膦(PH3),原因是___ 。
(3)单质铜及镍都是由___ 键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___ 。
(4)某镍白铜合金的立方晶胞结构如图所示。
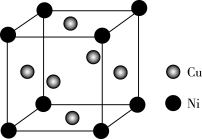
①晶胞中铜原子与镍原子的数量比为___ 。
(1)镍元素基态原子的电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③氨的沸点
(3)单质铜及镍都是由
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
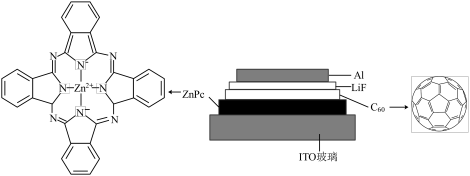
【推荐3】我国科学家制备了一种ZnPc/C60太阳能电池,其结构示意图如下。
(1)铝元素属于_____________ 区(填“s”“d”“ ”或“p”)。
”或“p”)。
(2)C60分子中60个碳原子都是等价的,均以近似_____________ 杂化的方式形成3个不共平面的σ键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,π电子云分布在C60分子笼的内外层表面上。循环伏安测试表明:C60在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
(3)①ZnPc中Zn2+的价层电子排布式是_____________ 。
②ZnPc中存在配位键的原因是_____________ 。
(4)某溶剂中,ZnPc可以和C60形成分子间电荷转移复合物,反应方程式可表示为:ZnPc+C60 ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
反应:ZnPc+C60 ZnPc-C60△H
ZnPc-C60△H_____________ 0(填“>”或“<”),ZnPc-C60中ZnPc是电子_____________ (填“给体”或“受体”)。
(5)LiF晶体结构属于氯化钠型,其晶胞结构如图所示。
①LiF的熔点和沸点比NaCl的高,请解释原因_____________ 。
②LiF晶体的密度约为2.6g/cm3,LiF晶胞的体积约为_____________ cm3(计算结果保留一位有效数字)。


(1)铝元素属于
 ”或“p”)。
”或“p”)。(2)C60分子中60个碳原子都是等价的,均以近似
(3)①ZnPc中Zn2+的价层电子排布式是
②ZnPc中存在配位键的原因是
(4)某溶剂中,ZnPc可以和C60形成分子间电荷转移复合物,反应方程式可表示为:ZnPc+C60
 ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。温度 | 生成ZnPc-C60的K |
24℃ | 1.2329 |
44℃ | 0.9674 |
64℃ | 0.4923 |
 ZnPc-C60△H
ZnPc-C60△H(5)LiF晶体结构属于氯化钠型,其晶胞结构如图所示。
①LiF的熔点和沸点比NaCl的高,请解释原因
②LiF晶体的密度约为2.6g/cm3,LiF晶胞的体积约为

您最近一年使用:0次



