研究表明,在一定条件下,气态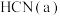 与
与 两种分子的互变反应过程能量变化如图所示。下列说法正确的是
两种分子的互变反应过程能量变化如图所示。下列说法正确的是
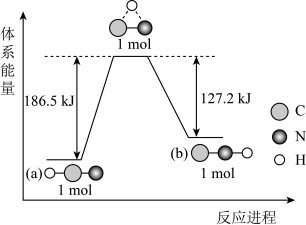
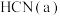 与
与 两种分子的互变反应过程能量变化如图所示。下列说法正确的是
两种分子的互变反应过程能量变化如图所示。下列说法正确的是
A.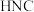 比 比 更稳定 更稳定 |
B. 转化为 转化为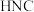 ,反应条件一定要加热 ,反应条件一定要加热 |
C. 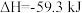 /mol /mol |
| D.加入催化剂,可以减小反应的热效应 |
2022高三·浙江·专题练习 查看更多[11]
上海市育才中学2022-2023学年高二下学期(等级考)期末调研化学试题上海市崇明中学2022-2023学年高二下学期期末(等级)考试化学试题江苏省徐州市铜山区2022-2023学年高一下学期期中化学(选择考)试题湖北省武昌实验中学2022-2023学年高一下学期3月月考化学试题辽宁省彰武县高级中学2021-2022学年高一下学期第二次月考化学试题重庆市重庆实验外国语学校2021-2022学年高二上学期1月月考化学试题江苏省海州高级中学2021-2022学年高一下学期期中考试化学试题上海市南洋模范中学2021-2022学年高一下学期3月月考化学试题上海市南洋模范中学2021-2022学年高一下学期3月考化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
更新时间:2022/04/14 16:15:01
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知在 、
、 条件下,
条件下,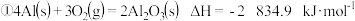 ,
, 。下列说法正确的是
。下列说法正确的是
 、
、 条件下,
条件下,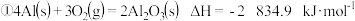 ,
, 。下列说法正确的是
。下列说法正确的是
A.等质量的 比 比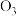 的能量低,由 的能量低,由 变为 变为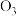 是吸热反应 是吸热反应 |
B.等质量的 比 比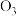 的能量高,由 的能量高,由 变为 变为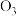 是放热反应 是放热反应 |
C.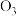 比 比 稳定,由 稳定,由 变为 变为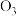 是吸热反应 是吸热反应 |
D. 比 比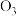 稳定,由 稳定,由 变为 变为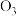 是放热反应 是放热反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知C(石墨) = C(金刚石),在该反应进程中其能量变化如图所示,有关该反应的描述正确的是

| A.该反应为放热反应 | B.金刚石与石墨互为同位素 |
| C.该反应为氧化还原反应 | D.石墨比金刚石稳定 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列依据热化学方程式得出的结论正确的是
| A.若将等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C.已知2C(s)+2O2(g)=2CO2(g);△H1,2C(s)+O2(g)=2CO(g);△H2,则△H1>△H2 |
| D.在101kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式可表 示为 2H2(g)+O2(g)=2H2O(l) △H=﹣571.6 kJ•mol﹣1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据如下能量关系示意图,下列说法正确的是
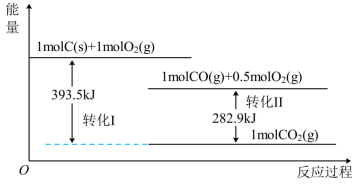
A.1mol 与1mol 与1mol  的能量之和为393.5kJ 的能量之和为393.5kJ |
| B.CO比CO2的能量高 |
C.C的燃烧热的热化学方程式为:C(s)+ O2(g)=CO(g) △H=110.6kJ·mol-1 O2(g)=CO(g) △H=110.6kJ·mol-1 |
D.CO气体燃烧的热化学方程式为: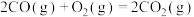  |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】氢气是人类最理想的能源。已知在25℃、101 kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是
| A.2H2+O2===2H2OΔH=-571.6kJ/mol |
| B.H2(g)+1/2O2(g)===H2O(g)ΔH=-285.8kJ/mol |
| C.2H2(g)+O2(g)===2H2O(l)ΔH=-571.6kJ/mol |
| D.2H2(g)+O2(g)===2H2O(l)ΔH=+571.6kJ/mol |
您最近半年使用:0次
【推荐1】 可以作为
可以作为 分解的催化剂,催化机理是:
分解的催化剂,催化机理是:
ⅰ. ;
;
ⅱ._______。
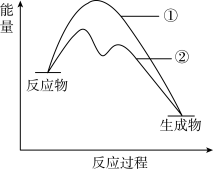
分解反应过程中能量变化如下图所示,下列判断不正确的是
 可以作为
可以作为 分解的催化剂,催化机理是:
分解的催化剂,催化机理是:ⅰ.
 ;
;ⅱ._______。
分解反应过程中能量变化如下图所示,下列判断

A.曲线②为含有 的反应过程 的反应过程 |
B.反应ii为 |
| C.反应ⅰ和ⅱ均为放热过程 |
| D.反应ⅰ的反应速率可能比反应ⅱ慢 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某研究小组对 甲烷化的反应路径和机理进行了研究。经过研究发现
甲烷化的反应路径和机理进行了研究。经过研究发现 负载金属
负载金属 傕化
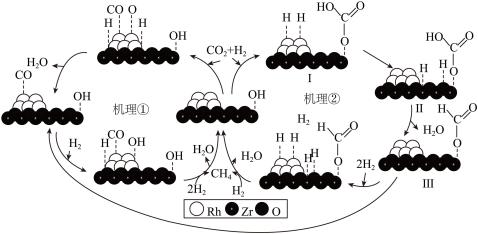
傕化 甲烷化可能存在的两种反应机理如图所示。下列说法中错误的是
甲烷化可能存在的两种反应机理如图所示。下列说法中错误的是
 甲烷化的反应路径和机理进行了研究。经过研究发现
甲烷化的反应路径和机理进行了研究。经过研究发现 负载金属
负载金属 傕化
傕化 甲烷化可能存在的两种反应机理如图所示。下列说法中错误的是
甲烷化可能存在的两种反应机理如图所示。下列说法中错误的是
A.机理①和机理②的不同点在于 的吸附、活化位置的不同 的吸附、活化位置的不同 |
B.吸附在活性金属 表面的中间体 表面的中间体 ,可能是由吸附在其表面的 ,可能是由吸附在其表面的 直接解离产生的 直接解离产生的 |
| C.同种催化剂,化学反应的途径不同,反应物的转化率也不同,反应的热效应也不同 |
| D.反应中既有极性键的断裂和形成,又有非极性键的断裂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】萘与三氧化硫反应,同时生成α-萘磺酸(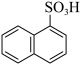 )与β-萘磺酸(
)与β-萘磺酸(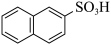 ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
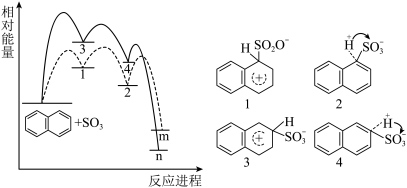
 )与β-萘磺酸(
)与β-萘磺酸( ),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A
),反应过程中的能量变化如图所示,1、2、3、4是中间产物,m、n各代表一种产物(已知速率常数k与温度T的关系式为k=A ,其中A、R为常数,Ea为活化能)。下列说法错误的是
,其中A、R为常数,Ea为活化能)。下列说法错误的是
| A.m代表α-萘磺酸,n代表β-萘磺酸 |
| B.稳定性:β-萘磺酸>α-萘磺酸 |
| C.升高相同温度,生成α-萘磺酸的反应速率变化更大 |
| D.平衡时,适当降低温度有利于提高混合物中β-萘磺酸的含量 |
您最近半年使用:0次

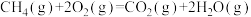

 和1.5mol
和1.5mol 置于密闭的容器中充分反应生成
置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为:
,放热19.3kJ,其热化学反应方程式为:


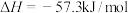 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量
则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量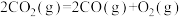 反应的
反应的


