化学是一门以实验为基础的学科。
Ⅰ.[Cu(NH3)4]SO4·H2O 晶体制备。
向盛有 4 mL 0.1 mol/L CuSO4 溶液的试管里滴加几滴 1 mol/L 氨水,首先形成蓝色沉淀,继续添加氨水并振荡试管,可以观察到沉淀溶解,得到深蓝色透明溶液。再向试管中加入适量乙醇,并用玻璃棒摩擦试管壁,可以观察到有深蓝色的[Cu(NH3)4]SO4·H2O 晶体析出。回答下列问题:
(1)写出蓝色沉淀溶解得透明溶液的离子方程式_______ 。
(2)加入适量乙醇有深蓝色的[Cu(NH3)4]SO4·H2O 晶体析出的原因_______ 。
(3)设计检验晶体中是否含有 SO 的实验方案:
的实验方案:_______ 。
Ⅱ.探究卤代烃的消去反应的产物。
如图所示,向圆底烧瓶中加入2g NaOH和15mL无水乙醇,搅拌。再向其中加入5mL 溴乙烷和几片碎瓷片,微热。将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验。
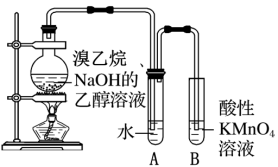
(4)气体在通入酸性高锰酸钾溶液前先通入盛水的试管是为了_______ 。
(5)若无A试管,B试管中应盛放试剂_______ 来检验消去反应产物。
(6)将气体缓慢通入酸性高锰酸钾溶液时发现小试管中溶液颜色褪色不明显。请结合以下资料:
资料1:溴乙烷发生消去反应比较适宜的反应温度为90 ℃~110 ℃,在该范围,温度越高,产生乙烯的速率越快。
资料2:溴乙烷的沸点:38.4 ℃。
分析可能的原因_______ 。
Ⅰ.[Cu(NH3)4]SO4·H2O 晶体制备。
向盛有 4 mL 0.1 mol/L CuSO4 溶液的试管里滴加几滴 1 mol/L 氨水,首先形成蓝色沉淀,继续添加氨水并振荡试管,可以观察到沉淀溶解,得到深蓝色透明溶液。再向试管中加入适量乙醇,并用玻璃棒摩擦试管壁,可以观察到有深蓝色的[Cu(NH3)4]SO4·H2O 晶体析出。回答下列问题:
(1)写出蓝色沉淀溶解得透明溶液的离子方程式
(2)加入适量乙醇有深蓝色的[Cu(NH3)4]SO4·H2O 晶体析出的原因
(3)设计检验晶体中是否含有 SO
 的实验方案:
的实验方案:Ⅱ.探究卤代烃的消去反应的产物。
如图所示,向圆底烧瓶中加入2g NaOH和15mL无水乙醇,搅拌。再向其中加入5mL 溴乙烷和几片碎瓷片,微热。将产生的气体通入盛水的试管后,再用酸性高锰酸钾溶液进行检验。

(4)气体在通入酸性高锰酸钾溶液前先通入盛水的试管是为了
(5)若无A试管,B试管中应盛放试剂
(6)将气体缓慢通入酸性高锰酸钾溶液时发现小试管中溶液颜色褪色不明显。请结合以下资料:
资料1:溴乙烷发生消去反应比较适宜的反应温度为90 ℃~110 ℃,在该范围,温度越高,产生乙烯的速率越快。
资料2:溴乙烷的沸点:38.4 ℃。
分析可能的原因
更新时间:2022-04-15 20:09:37
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】I.下列实验中仪器的下端必须插入反应物液面下的是:_________ 。(填写序号)
①制备氢气的简易装置中的长颈漏斗;②制备氯气装置中的分液漏斗; ③制备硝基苯时的温度计;④用乙醇制取乙烯时的温度计; ⑤分馏石油时的温度计。
II.完成以下实验:①
用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题:

(1)试管I中反应的化学方程式_______________________________ 。
(2)反应结束后,U形管中粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的_______________ (填字母)
(3)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后__________________ (填代号)。
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。

用上图装置进行实验的目的是______ ;上图中右边试管中的现象是_____ ;水的作用是_______ 。
(5)溴乙烷(C2H5Br)多一个碳的同系物在氢氧化钠的醇溶液中能发生反应,生成的产物为_________________
①制备氢气的简易装置中的长颈漏斗;②制备氯气装置中的分液漏斗; ③制备硝基苯时的温度计;④用乙醇制取乙烯时的温度计; ⑤分馏石油时的温度计。
II.完成以下实验:①
用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题:

(1)试管I中反应的化学方程式
(2)反应结束后,U形管中粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的
| A.NaOH溶液 | B.H2O | C.Na2SO3溶液 | D.CCl4 |
(3)下列几项实验步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后
①加热;②加入AgNO3溶液;③加入稀HNO3酸化;④加入NaOH溶液;⑤冷却
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。

用上图装置进行实验的目的是
(5)溴乙烷(C2H5Br)多一个碳的同系物在氢氧化钠的醇溶液中能发生反应,生成的产物为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室制得气体中常含有杂质,影响其性质的检验。下图A为除杂装置,B为性质检验装置,完成下列表格:


| 序号 | 气体 | 反应原理 | A中试剂 |
| ① | 乙烯 | 无水乙醇与浓硫酸共热,反应的化学方程式是 | |
| ② | 乙烯 | 溴乙烷与NaOH的乙醇溶液共热,反应的化学方程式是 | |
| ③ | 乙炔 | 向电石中滴加饱和食盐水反应,CaC2的电子式 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】溴乙烷(无色液体,难溶于水,沸点38.4℃)在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1) 用水浴加热而不直接用酒精灯加热的原因是__________ 。
(2) 观察到_____________________ 现象时,表明溴乙烷与NaOH溶液已完全反应。
(3) 鉴定生成物中乙醇的结构,可用的波谱是________________________ 。
(4) 为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是___________ ,检验的方法是____________________________________ (需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
(5)写出由乙烯→溴乙烷→乙醇(其他试剂自选)反应的化学方程式:______________________
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
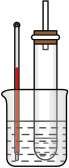
(1) 用水浴加热而不直接用酒精灯加热的原因是
(2) 观察到
(3) 鉴定生成物中乙醇的结构,可用的波谱是
(4) 为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是
(5)写出由乙烯→溴乙烷→乙醇(其他试剂自选)反应的化学方程式:
您最近一年使用:0次
【推荐1】氮、磷及其化合物在工农业生产中都有重要用逾。
(1)基态磷原子价电子排布的轨道表示式为_____ 。
(2)元素B、N、O的第一电离能由大到小的顺序为_____ 。
(3)一种食品添加剂NaNO2中NO2﹣中心原子的杂化类型是_____ ,与NO2﹣互为等电子体的分子的化学式为_____ (写1种)
(4)N2H4是火箭的燃料,与氧气的相对分子质量相同,它在常温常压下是液态,而氧气是气态,造成这种差异的主要原因是_____ 。
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层,磷化硼可由三溴化硼和三溴化磷于高温下在氢气中反应合成。
①三溴化磷分子的空间构型是_____ ,三溴化硼键角是_____ 。
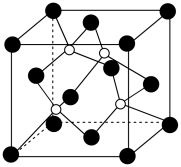
②磷化硼晶体晶胞如图所示,其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为_____ ,磷原子的配位数为是_____ ,该结构中有一个配位键,提供空轨道的原子是_____ ;已知该晶胞边长apm,阿伏伽德罗常数为NA,则磷化硼晶体的密度为_____ g•cm﹣3。
(1)基态磷原子价电子排布的轨道表示式为
(2)元素B、N、O的第一电离能由大到小的顺序为
(3)一种食品添加剂NaNO2中NO2﹣中心原子的杂化类型是
(4)N2H4是火箭的燃料,与氧气的相对分子质量相同,它在常温常压下是液态,而氧气是气态,造成这种差异的主要原因是
(5)磷化硼是一种耐磨涂料,它可用作金属的表面保护层,磷化硼可由三溴化硼和三溴化磷于高温下在氢气中反应合成。
①三溴化磷分子的空间构型是
②磷化硼晶体晶胞如图所示,其中实心球为磷原子,在一个晶胞中磷原子空间堆积方式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】B、C、N、O、F、Fe是地壳中常见的元素。回答下列问题
(1)基态碳、氮、氧原子的未成对电子数之比是___________ ;电负性由大到小的顺序是___________ 。
(2)三氟化硼( )是一种无色气体。
)是一种无色气体。 水解生成
水解生成 和另一种一元无氧酸(甲),甲的化学式是
和另一种一元无氧酸(甲),甲的化学式是___________ 。
(3)三氟化硼( )分子中心原子的杂化轨道类型是
)分子中心原子的杂化轨道类型是___________ ;分子空间构型是___________ 。
(4)图1是一种太阳能电池工作原理的示意图。其中电解质溶液为 和
和 的混合溶液。
的混合溶液。 中,中心离子为
中,中心离子为___________ 。
②电池工作时,下列描述正确的是___________ 。
A.电极a为正极 B. 向电极a移动
向电极a移动
C.电子由电极a经导线流向电极b D.电极b上发生氧化反应
③正极上发生的电极反应为___________ 。
(5)氮化铁晶体,其晶胞结构如图2所示:___________ 个
A.2 B.4 C.6 D.8
②该氮化铁晶体的化学式为___________
A.FeN B.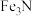 C.
C. D.
D.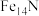
(1)基态碳、氮、氧原子的未成对电子数之比是
(2)三氟化硼(
 )是一种无色气体。
)是一种无色气体。 水解生成
水解生成 和另一种一元无氧酸(甲),甲的化学式是
和另一种一元无氧酸(甲),甲的化学式是(3)三氟化硼(
 )分子中心原子的杂化轨道类型是
)分子中心原子的杂化轨道类型是(4)图1是一种太阳能电池工作原理的示意图。其中电解质溶液为
 和
和 的混合溶液。
的混合溶液。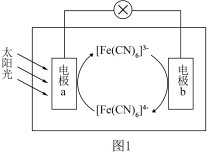
 中,中心离子为
中,中心离子为②电池工作时,下列描述正确的是
A.电极a为正极 B.
 向电极a移动
向电极a移动C.电子由电极a经导线流向电极b D.电极b上发生氧化反应
③正极上发生的电极反应为
(5)氮化铁晶体,其晶胞结构如图2所示:

A.2 B.4 C.6 D.8
②该氮化铁晶体的化学式为
A.FeN B.
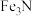 C.
C. D.
D.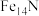
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钴的合金及其配合物用途非常广泛。已知Co3+比Fe3+的氧化性更强,在水溶液中不能大量存在。
(1)Co3+的核外电子排布式为__________________________ 。
(2)无水CoCl2的熔点为735℃、沸点为1049℃,FeCl3熔点为306℃、沸点为315℃。CoCl2属于_________ 晶体,FeCl3属于__________ 晶体。
(3)BNCP可用于激光起爆器等,可由HClO4、CTCN、NaNT共反应制备。
① 的空间构型为
的空间构型为______________ 。
②CTCN的化学式为[Co(NH3)4CO3]NO3,与Co(Ⅲ)形成配位键的原子是_______ {已知 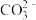 的结构式为
的结构式为 }。
}。
③NaNT可以 (双聚氰胺)为原料制备。1 mol双聚氰胺分子中含σ键的数目为
(双聚氰胺)为原料制备。1 mol双聚氰胺分子中含σ键的数目为____________ 。
(4)Co与CO作用可生成Co2(CO)8,其结构如图所示。该分子中C原子的杂化方式为_________________ 。

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为___________ 。已知NA为阿伏加 德罗常数的数值,则该晶胞的密度为__________ (用含a、b、NA的代数式表示)g·cm-3。
(1)Co3+的核外电子排布式为
(2)无水CoCl2的熔点为735℃、沸点为1049℃,FeCl3熔点为306℃、沸点为315℃。CoCl2属于
(3)BNCP可用于激光起爆器等,可由HClO4、CTCN、NaNT共反应制备。
①
 的空间构型为
的空间构型为②CTCN的化学式为[Co(NH3)4CO3]NO3,与Co(Ⅲ)形成配位键的原子是
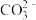 的结构式为
的结构式为 }。
}。③NaNT可以
 (双聚氰胺)为原料制备。1 mol双聚氰胺分子中含σ键的数目为
(双聚氰胺)为原料制备。1 mol双聚氰胺分子中含σ键的数目为(4)Co与CO作用可生成Co2(CO)8,其结构如图所示。该分子中C原子的杂化方式为

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】化学实验室某次实验产生的废液中可能含有大量的 、
、 、CO
、CO 、SO
、SO 、
、 、HCO
、HCO 等。设计实验进行鉴别,步骤如下:
等。设计实验进行鉴别,步骤如下:
①加入NaOH溶液产生蓝色沉淀;
②向①所得的溶液中滴加足量 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀无变化。
由此判断:
(1)该废液中确定存在的离子有___________ 。
(2)步骤①发生反应的离子方程式为___________ 。
(3)某兴趣小组要除去废液中确定的离子,并回收其中的金属,最后得到NaCl溶液。设计实验方案如下:
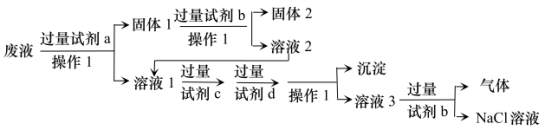
①操作1为___________ ,固体2为___________ ,试剂d为___________ 。
②溶液2所含溶质为___________ (填化学式)。
③写出加入试剂a的离子方程式___________ 。
 、
、 、CO
、CO 、SO
、SO 、
、 、HCO
、HCO 等。设计实验进行鉴别,步骤如下:
等。设计实验进行鉴别,步骤如下:①加入NaOH溶液产生蓝色沉淀;
②向①所得的溶液中滴加足量
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;③过滤,然后向所得白色沉淀中加入过量稀硝酸,沉淀无变化。
由此判断:
(1)该废液中确定存在的离子有
(2)步骤①发生反应的离子方程式为
(3)某兴趣小组要除去废液中确定的离子,并回收其中的金属,最后得到NaCl溶液。设计实验方案如下:

①操作1为
②溶液2所含溶质为
③写出加入试剂a的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某工厂排放的无色废水中可能含有 、Ba2+、Fe3+、
、Ba2+、Fe3+、 、Cl-中的两种或多种。取少量废水,向其中滴加稀盐酸有气体产生。回答下列问题:
、Cl-中的两种或多种。取少量废水,向其中滴加稀盐酸有气体产生。回答下列问题:
(1)废水中一定没有的离子是___________ (填离子符号)。
(2)向废水中滴加稀盐酸发生反应的离子方程式为___________ 。
(3)向废水中加过量浓氢氧化钠溶液,可能出现的现象是___________ 。
(4)为确定废水中还可能存在的以上离子,具体的实验方法是___________ 。
 、Ba2+、Fe3+、
、Ba2+、Fe3+、 、Cl-中的两种或多种。取少量废水,向其中滴加稀盐酸有气体产生。回答下列问题:
、Cl-中的两种或多种。取少量废水,向其中滴加稀盐酸有气体产生。回答下列问题:(1)废水中一定没有的离子是
(2)向废水中滴加稀盐酸发生反应的离子方程式为
(3)向废水中加过量浓氢氧化钠溶液,可能出现的现象是
(4)为确定废水中还可能存在的以上离子,具体的实验方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2SO4、Na2CO3中的一种或几种,现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是___________ ,一定不含有的物质是___________ 。(均填化学式)
(2)写出②步变化的离子方程式:___________ 。
(3)为了进一步确定可能含有的物质,将步骤④所得混合液过滤,得到白色沉淀,向白色沉淀中加入足量的___________ 溶液。若白色沉淀完全溶解,则___________ ;若白色沉淀部分溶解,则___________ 。
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出②步变化的离子方程式:
(3)为了进一步确定可能含有的物质,将步骤④所得混合液过滤,得到白色沉淀,向白色沉淀中加入足量的
您最近一年使用:0次



