印刷电路板的制作原理是用足量的FeCl3溶液腐蚀覆铜板上不需要的铜箔。下列说法正确的是
| A.用KSCN溶液可检验腐蚀后溶液中的Fe2+ |
| B.Fe3+能溶解Cu,说明金属性Cu>Fe |
| C.当有1mol电子转移时,溶液中Cu2+增加1mol |
| D.腐蚀后溶液中的金属阳离子有Fe3+、Fe2+、Cu2+ |
21-22高一下·湖南长沙·期中 查看更多[3]
湖南省长沙市长郡中学2021-2022学年高一下学期期中考试化学试题上海市嘉定区第一中学2021-2022学年高一下学期质量诊断二 化学试题(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)
更新时间:2022-04-26 15:13:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将金属钠分散在氯化钠中,控制温度280~1100℃在搅拌条件下通入氢气即可生成氢化钠(NaH),已知NaH+H2O=NaOH+H2↑,下列有关说法错误的是
| A.NaH中H的化合价为-1 |
| B.NaH与H2O的反应属于置换反应 |
| C.氢化钠由氢气与金属钠反应生成 |
| D.等质量的Na和NaH分别与水反应,NaH产生H2物质的量多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】硫难溶于水,微溶于酒精,易溶于CS2。硫的氧化物、氢化物、硫酸在工业中有很多应用。高压发电系统常用 作为绝缘气体,该气体分子呈正八面体结构,如图所示。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源的方法。硫元素的几种化合物存在下列转化关系。下列说法正确的是
作为绝缘气体,该气体分子呈正八面体结构,如图所示。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源的方法。硫元素的几种化合物存在下列转化关系。下列说法正确的是
浓H2SO4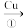 SO2
SO2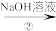 Na2SO3溶液
Na2SO3溶液 Na2S2O3溶液
Na2S2O3溶液 S
S
 作为绝缘气体,该气体分子呈正八面体结构,如图所示。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源的方法。硫元素的几种化合物存在下列转化关系。下列说法正确的是
作为绝缘气体,该气体分子呈正八面体结构,如图所示。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源的方法。硫元素的几种化合物存在下列转化关系。下列说法正确的是浓H2SO4
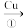 SO2
SO2 Na2SO3溶液
Na2SO3溶液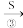 Na2S2O3溶液
Na2S2O3溶液 S
S| A.反应①中生成的SO2具有漂白性,可使溴水褪色 |
| B.反应②中若SO2过量,就会生成NaHSO3 |
| C.反应④中生成 S 既是氧化产物,也是还原产物 |
| D.反应④中当消耗 1mol 稀硫酸时,电子转移为4mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列离子方程式或化学方程式错误的是
A.浅黄色过氧化钠吸收 后变为白色: 后变为白色: |
B.向 溶液中滴加 溶液中滴加 溶液产生蓝色沉淀: 溶液产生蓝色沉淀: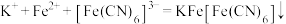 |
C.向浓氨水中滴加明矾溶液产生白色沉淀: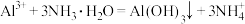 |
D.向 溶液中通入少量 溶液中通入少量 气体: 气体: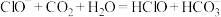 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向苯酚浊液中加入Na2CO3溶液,溶液变澄清 | 酸性:苯酚>HCO3- |
| B | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液,溶液变成血红色 | Fe(NO3)2已变质 |
| C | 氯乙烷与NaOH溶液共热后,滴加AgNO3溶液,生成白色沉淀 | 氯乙烷发生水解 |
| D | 在2 mL 0.01 mol·L-1的Na2S溶液中先滴入几滴0.01 mol·L-1 ZnSO4溶液有白色沉淀生成,再滴入0.01 mol·L-1 CuSO4溶液,又出现黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向 、
、 的混合溶液中加入铁粉,充分反应后仍有固体剩余,已知氧化性:
的混合溶液中加入铁粉,充分反应后仍有固体剩余,已知氧化性: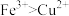 ,则下列判断
,则下列判断不正确 的是
 、
、 的混合溶液中加入铁粉,充分反应后仍有固体剩余,已知氧化性:
的混合溶液中加入铁粉,充分反应后仍有固体剩余,已知氧化性: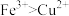 ,则下列判断
,则下列判断A.溶液中可能没有 | B.剩余固体中一定含铁 |
C.溶液中一定含有 | D.加入 溶液一定不变红色 溶液一定不变红色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均受热分解 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝不能熔化 | 金属铝的熔点较高 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向100mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示(忽略溶液体积的变化)。下列说法正确的是


| A.a点时溶液中阳离子只有Cu2+、Fe2+ |
| B.b点时溶液中发生的反应为Fe+2Fe3+=3Fe2+ |
| C.c点时溶液中溶质的物质的量浓度为0.4mol∙L-1 |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为2∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.硫酸铜是可用于饮用水的消毒 |
| B.氯化亚铁溶液与铜反应可用于制作印刷电路板 |
| C.SiO2 可用于制作光导纤维,也可以制成光电池 |
| D.纯碱可用于玻璃、肥皂、造纸、食品等工业 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】取 1LFeCl3 溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法不正确的是
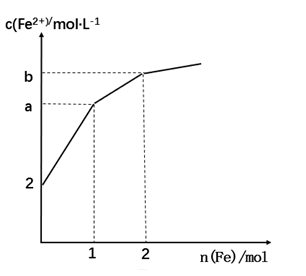

| A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+ |
| B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu |
| C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1 |
| D.腐蚀之前原溶液中 c(Fe3+)=4 mol·L-1 |
您最近一年使用:0次



