为了探究市售Fe3O4能否与常见的酸(盐酸、稀硫酸)发生反应,实验小组做了以下工作。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为_______ 。
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为_______ mL(保留1位小数)。
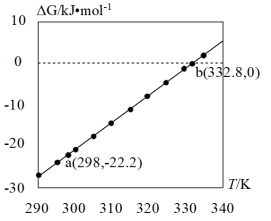
(3)查阅文献:吉布斯自由能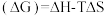 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是_______ 。
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)
(4)实验ⅱ的作用是_______ 。
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是_______ 。
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入_______ ,然后重复实验i。
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是_______ 。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为
(3)查阅文献:吉布斯自由能
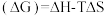 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用
 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)| 编号 | i | ii |
| 实验操作 | 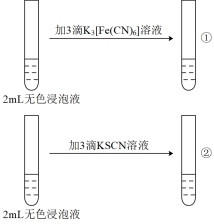 | 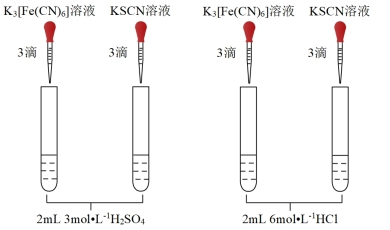 |
| 现象 | ①无蓝色沉淀 ②溶液显红色 | 均无明显现象 |
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是
2022·福建三明·三模 查看更多[3]
福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编福建省泉州第一中学2023-2024学年高三上学期12月月考化学试题
更新时间:2022-05-05 18:53:40
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,化学实验室产生的废液必须经处理后才能排放。某化学实验室产生的酸性废液中含有Fe3+、Cu2+、Ba2+三种金属阳离子和Cl-一种阴离子,实验室设计了下述方案对废液进行处理,以回收金属并测定含量,保护环境。
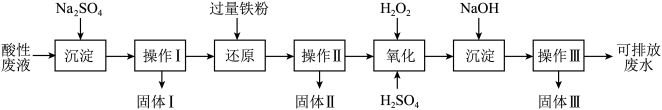
已知实验中处理的酸性废液的体积为1L,用pH计测定出其中H+物质的量浓度为0.10mol/L。
请回答下列问题:
(1)实验中操作I、Ⅱ、Ⅲ的方法相同,操作步骤依次为过滤、_________ 、干燥。
(2)“氧化”步骤所得溶液颜色为棕黄色,该反应的离子方程式为:__________ 。
(3)实验中称量固体I 的质量为4.66g,固体II 的质量为15.2g,用足量的稀硝酸溶解固体Ⅱ后产生了标准状况下的无色气体4.48L,则固体Ⅱ中金属铜的质量为________ g。
(4)实验中将固体Ⅲ进行充分灼烧,使用仪器除了酒精灯、三脚架、泥三角、玻璃棒外,还有_____ (填名称)。最后得到的红棕色固体质量为40.0g,则原溶液中氯离子的物质的量浓度为________ (写出计算过程)。

已知实验中处理的酸性废液的体积为1L,用pH计测定出其中H+物质的量浓度为0.10mol/L。
请回答下列问题:
(1)实验中操作I、Ⅱ、Ⅲ的方法相同,操作步骤依次为过滤、
(2)“氧化”步骤所得溶液颜色为棕黄色,该反应的离子方程式为:
(3)实验中称量固体I 的质量为4.66g,固体II 的质量为15.2g,用足量的稀硝酸溶解固体Ⅱ后产生了标准状况下的无色气体4.48L,则固体Ⅱ中金属铜的质量为
(4)实验中将固体Ⅲ进行充分灼烧,使用仪器除了酒精灯、三脚架、泥三角、玻璃棒外,还有
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59 ℃,沸点为11.0 ℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60 ℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。
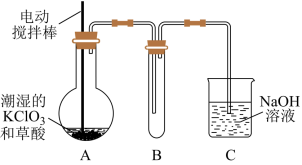
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、__________ 。
(2)B装置必须放在冰水浴中,其原因是______________________________ 。
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图
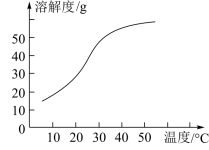
获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③______________________________________ ;
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:_______ 。
②若步骤2所得溶液放置时间太长,则测定结果____________ (填“偏高”、“偏低”或“不变”)
③ClO2溶液的浓度为________ g·L-1(用含字母的代数式表示)。

(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、
(2)B装置必须放在冰水浴中,其原因是
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2•3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图

获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:
②若步骤2所得溶液放置时间太长,则测定结果
③ClO2溶液的浓度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】Ⅰ.完成下列问题
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为_______ ;若将100g此盐酸加水稀释至5.82mol/L,则加入水的质量_______ 100g。(填“大于”、“等于”或“小于”);
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:
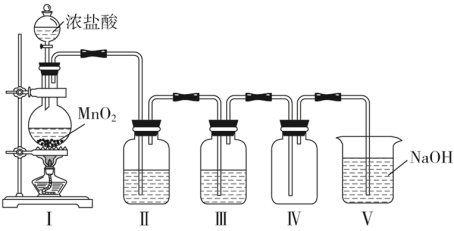
(2)装置Ⅰ中盛装浓盐酸的仪器名称为_______ ;圆底烧瓶中发生反应的离子方程式为_______ ;此反应中HCl体现出性质有_______ 和 _______ 。若生成标准状况下22.4L Cl2,被氧化的HCl分子数是_______ 。
(3)Ⅱ和Ⅲ中盛装的试剂分别是_______ 和_______ 。
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为_______ ;
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______
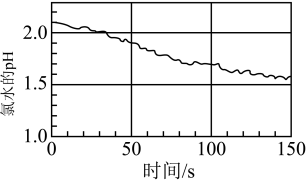
(6)装置Ⅴ中NaOH溶液的作用是吸收尾气,其中发生反应的化学方程式为 _______ 。
(1)市售浓盐酸的密度为1.180 g/mL,物质的量浓度为 11.64 mol/L,此浓盐酸的质量分数为
Ⅱ.某同学在实验室中用此浓盐酸与MnO2为原料制取纯净干燥的Cl2,装置如下图:

(2)装置Ⅰ中盛装浓盐酸的仪器名称为
(3)Ⅱ和Ⅲ中盛装的试剂分别是
(4)氯气的水溶液为氯水,Cl2与H2O反应的离子方程式为
(5)如图是数字化实验得到的光照过程中氯水的pH变化情况。对此,下列有关说法正确的是_______

| A.光照使氯水中的次氯酸分解为盐酸,溶液的酸性增强 |
| B.随着对氯水光照时间的延长,氯水的漂白性将增强 |
| C.随着对氯水光照时间的延长,溶液中Cl-的浓度不断减小 |
| D.随着对氯水光照时间的延长,氯水颜色逐渐变浅 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】利用软锰矿(主要成分是MnO2,还含少量CaO、MgO、SiO2、Al2O3等杂质)制取高纯硫酸锰的工艺流程如图所示。

已知:常温下,一些金属氢氧化物沉淀的pH如表:
常温下,一些难溶电解质的溶度积常数如表:
回答下列问题:
(1)滤渣1的主要成分是_______ (填化学式);将软锰矿、铁屑和硫酸按一定比例放入反应装置中,搅拌、加热反应一定时间,其中搅拌、加热的目的是_______ ;从“深度除杂”后的溶液中得到MnSO4固体的操作为_______ 、降温结晶、过滤、洗涤和干燥。
(2)“浸取”时,溶液中的Fe2+与MnO2反应生成Fe3+的离子方程式为_______ ,“浸出液”需要鼓入一段时间空气后,再进行“沉铁”的原因是_______ 。
(3)“沉铁、铝”时,加CaCO3控制溶液pH范围是_______ ;常温下,Ksp[Al(OH)3]=________ 。
(4)“深度除杂”中加入MnF2可以除去_______ 离子和_______ 离子,原因是_______ 。

已知:常温下,一些金属氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀pH | 1.5 | 6.5 | 7.7 | 3.8 |
| 沉淀完全pH | 3.7 | 9.7 | 9.8 | 5.2 |
| 难溶电解质 | MnF2 | CaF2 | MgF2 |
| Ksp | 5.3×10-3 | 1.5×10-10 | 7.4×10-11 |
(1)滤渣1的主要成分是
(2)“浸取”时,溶液中的Fe2+与MnO2反应生成Fe3+的离子方程式为
(3)“沉铁、铝”时,加CaCO3控制溶液pH范围是
(4)“深度除杂”中加入MnF2可以除去
您最近一年使用:0次
【推荐2】化合物X由两种元素组成,某学习小组按如下流程进行实验:化合反应 得到溶液A(含4种元素)。B和D为纯净物。
请回答:
(1)X的组成元素是___________ ,X的化学式是___________ 。
(2)写出X→A的化学方程式___________ 。
(3)写出C→D的离子方程式___________ 。
(4)实验室制得的黄绿气体单质B含有HCl,设计实验验证___________ 。
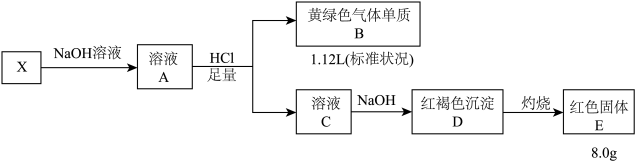
请回答:
(1)X的组成元素是
(2)写出X→A的化学方程式
(3)写出C→D的离子方程式
(4)实验室制得的黄绿气体单质B含有HCl,设计实验验证
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】纳米磁性流体材料广泛应用于减震、医疗器械、声音调节等高科技领域.如图是制备纳米 磁流体的两种流程:
磁流体的两种流程:
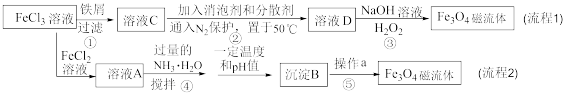
 分析流程图中的两种流程,其中
分析流程图中的两种流程,其中______  填“流程1”、“流程2”
填“流程1”、“流程2” 所有反应不涉及氧化还原反应.步骤
所有反应不涉及氧化还原反应.步骤 反应的离子方程式为
反应的离子方程式为______ .
 步骤
步骤 保持
保持 的方法是
的方法是______ .
 步骤
步骤 中加入的
中加入的 电子式是
电子式是______ ,步骤 制备
制备 磁流体的化学方程式为
磁流体的化学方程式为______ .
 流程2中
流程2中 和
和 制备
制备 磁流体,理论上
磁流体,理论上 和
和 物质的量之比为
物质的量之比为______  已知沉淀B为四氧化三铁.步骤
已知沉淀B为四氧化三铁.步骤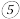 中操作a具体的步骤是
中操作a具体的步骤是______ .
 利用
利用 可测定
可测定 磁流体中的
磁流体中的 含量.若
含量.若 磁流体与
磁流体与 充分反应消耗了
充分反应消耗了 的
的 标准溶液100mL,则磁流体中含有
标准溶液100mL,则磁流体中含有 的物质的量为
的物质的量为______ mol.
 磁流体的两种流程:
磁流体的两种流程: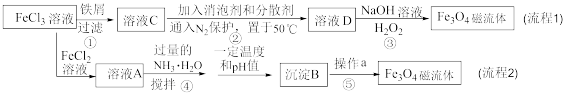
 分析流程图中的两种流程,其中
分析流程图中的两种流程,其中 填“流程1”、“流程2”
填“流程1”、“流程2” 所有反应不涉及氧化还原反应.步骤
所有反应不涉及氧化还原反应.步骤 反应的离子方程式为
反应的离子方程式为 步骤
步骤 保持
保持 的方法是
的方法是 步骤
步骤 中加入的
中加入的 电子式是
电子式是 制备
制备 磁流体的化学方程式为
磁流体的化学方程式为 流程2中
流程2中 和
和 制备
制备 磁流体,理论上
磁流体,理论上 和
和 物质的量之比为
物质的量之比为 已知沉淀B为四氧化三铁.步骤
已知沉淀B为四氧化三铁.步骤 中操作a具体的步骤是
中操作a具体的步骤是 利用
利用 可测定
可测定 磁流体中的
磁流体中的 含量.若
含量.若 磁流体与
磁流体与 充分反应消耗了
充分反应消耗了 的
的 标准溶液100mL,则磁流体中含有
标准溶液100mL,则磁流体中含有 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验Ⅰ:一组同学按下图装置(固定装置已略去)进行实验。
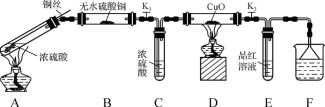
(1) A中反应的化学方程式为__________________ 。
(2) 实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是__________ 。
(3) 为说明浓硫酸中的水是否影响B装置现象的判断,还需进行一次实验。实验方案为___________ 。
实验Ⅱ:另一组同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
i. 将光亮铜丝插入浓硫酸,加热;
ii. 待产生黑色沉淀和气体时,抽出铜丝,停止加热;
iii. 冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
查阅文献:检验微量Cu2+的方法是向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+。
(4) 该同学假设黑色沉淀是CuO。检验过程如下:
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,产生红褐色沉淀。
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,未见红褐色沉淀。由该检验过程所得结论:________________ 。
(5) 再次假设,黑色沉淀是铜的硫化物。实验如下:
①现象2说明黑色沉淀具有____ 性。
②能确认黑色沉淀中含有S元素的现象是_______ ,相应的离子方程式是_____________ 。
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是________ 。
实验Ⅰ:一组同学按下图装置(固定装置已略去)进行实验。

(1) A中反应的化学方程式为
(2) 实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是
(3) 为说明浓硫酸中的水是否影响B装置现象的判断,还需进行一次实验。实验方案为
实验Ⅱ:另一组同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
i. 将光亮铜丝插入浓硫酸,加热;
ii. 待产生黑色沉淀和气体时,抽出铜丝,停止加热;
iii. 冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
查阅文献:检验微量Cu2+的方法是向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+。
(4) 该同学假设黑色沉淀是CuO。检验过程如下:
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,产生红褐色沉淀。
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,未见红褐色沉淀。由该检验过程所得结论:
(5) 再次假设,黑色沉淀是铜的硫化物。实验如下:
| 实验装置 | 现象 |
 | 1. A试管中黑色沉淀逐渐溶解 2. A试管内上方出现红棕色气体 3. B试管中出现白色沉淀 |
②能确认黑色沉淀中含有S元素的现象是
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是
您最近一年使用:0次
【推荐2】I.X是一种集洗涤、漂白、杀菌于一体的新型漂白剂(由四种短周期元素组成的纯净物),无毒无味,性能温和,且对环境友好。X从组成形式上可看成是某种正盐M与活性物质N的加合产物(mM·nN ,类似于结晶水合物,相对分子量不超过400)。现将X按如下流程实验,气体A能使带火星的木条复燃,固体B溶于水所得溶液显碱性,且焰色反应呈黄色。
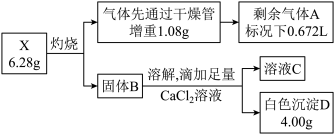
请回答:
(1)X中含有的非金属元素是_______ ,写出X灼烧的化学方程式是_______ 。
(2)向X的溶液中通入少量SO2,请写出离子方程式_______ 。
II.某化学兴趣小组为了探究硫酸铁溶液与铜粉反应的限度问题,向一定量的硫酸铁溶液中加入过量的铜粉,充分振荡后溶液逐渐变蓝,过滤,向滤液中滴加2滴0.2mol/L KSCN溶液。实验现象为:溶液变为红色,但振荡后红色迅速褪去并有白色沉淀生成。甲同学猜想出现异常现象是由于溶液中的Cu2+干扰了Fe3+的检验,查阅相关资料如下:
①CuSCN是一种白色沉淀物
②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
(3)该兴趣小组所记录的实验现象说明铜与铁离子的反应_______ (填有或没有)限度。
(4)请用离子方程式分别解释“溶液变为红色”、“振荡后红色迅速褪去并有白色沉淀生成”现象的原因:_______ 、_______ 。
(5)为了进一步探究,该小组向盛有2mL 0.5mol/L FeSO4和0.2mol/L KSCN混合溶液的试管中,滴加5滴0.05mol/L硫酸铜溶液,有白色沉淀生成,且溶液变红。请解释溶液变红的可能原因(可以不止一种):_______ 。

请回答:
(1)X中含有的非金属元素是
(2)向X的溶液中通入少量SO2,请写出离子方程式
II.某化学兴趣小组为了探究硫酸铁溶液与铜粉反应的限度问题,向一定量的硫酸铁溶液中加入过量的铜粉,充分振荡后溶液逐渐变蓝,过滤,向滤液中滴加2滴0.2mol/L KSCN溶液。实验现象为:溶液变为红色,但振荡后红色迅速褪去并有白色沉淀生成。甲同学猜想出现异常现象是由于溶液中的Cu2+干扰了Fe3+的检验,查阅相关资料如下:
①CuSCN是一种白色沉淀物
②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
(3)该兴趣小组所记录的实验现象说明铜与铁离子的反应
(4)请用离子方程式分别解释“溶液变为红色”、“振荡后红色迅速褪去并有白色沉淀生成”现象的原因:
(5)为了进一步探究,该小组向盛有2mL 0.5mol/L FeSO4和0.2mol/L KSCN混合溶液的试管中,滴加5滴0.05mol/L硫酸铜溶液,有白色沉淀生成,且溶液变红。请解释溶液变红的可能原因(可以不止一种):
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】亚氯酸钠(NaClO2)是一种应用广泛的氧化剂和漂白剂。
(1)亚氯酸钠(NaClO2)中氯元素的化合价是____________ ;
(2)某同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。该同学利用下图所示装置制取NaClO2晶体:
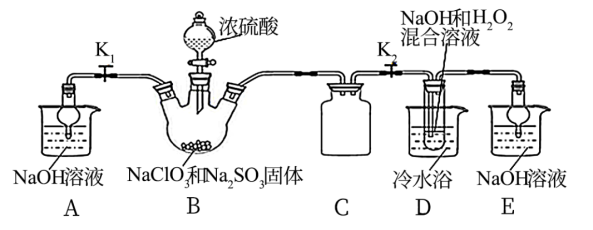
①装置B中盛装浓硫酸的仪器名称是______ ,装置C的作用是_________ ;
②已知装置B中的产物有ClO2气体,装置B中反应的化学方程式为___________________ ;
③装置D中发生反应的化学方程式为______________________________ ,反应后的溶液中除了ClO2-、ClO3-、Cl-、ClO-、OH-外还可能含有一种阴离子是_____ ,检验该离子的方法是_____________ ;
④反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后趁热过滤,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。如果撤去装置D中的冷水浴,可能导致产品中混有的杂质是______________________ ;
(1)亚氯酸钠(NaClO2)中氯元素的化合价是
(2)某同学通过查阅文献发现:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。该同学利用下图所示装置制取NaClO2晶体:

①装置B中盛装浓硫酸的仪器名称是
②已知装置B中的产物有ClO2气体,装置B中反应的化学方程式为
③装置D中发生反应的化学方程式为
④反应结束后,先将装置D反应后的溶液在55℃条件下减压蒸发结晶,然后趁热过滤,再用38℃~60℃的温水洗涤,最后在低于60℃条件下干燥,得到NaClO2晶体。如果撤去装置D中的冷水浴,可能导致产品中混有的杂质是
您最近一年使用:0次



