根据下图所示N2(g)和O2(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是
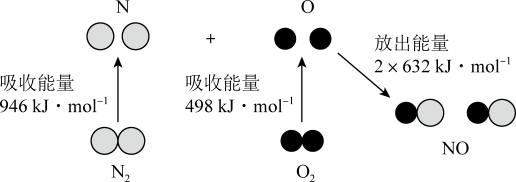

| A.N2(g)与O2(g)反应生成NO(g)是放热反应 |
| B.2 mol O原子结合生成O2(g)时需要吸收498 kJ能量 |
| C.1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量 |
| D.该反应断开反应物中化学键吸收的总能量小于形成生成物中化学键释放的总能量 |
更新时间:2022-06-11 21:59:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】肼 在不同条件下分解产物不同,200℃时在
在不同条件下分解产物不同,200℃时在 表面分解的机理如图1。
表面分解的机理如图1。
已知200℃时:反应 I : =
=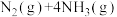
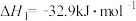
反应II: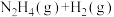 =
=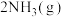
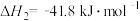
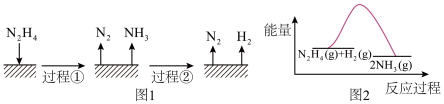
下列说法不正确的是( )
 在不同条件下分解产物不同,200℃时在
在不同条件下分解产物不同,200℃时在 表面分解的机理如图1。
表面分解的机理如图1。已知200℃时:反应 I :
 =
=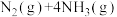
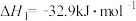
反应II:
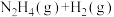 =
=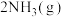
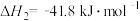

下列说法不正确的是( )
A.200℃时,肼分解生成氮气和氢气的热化学方程式为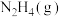 = =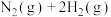 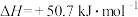 |
| B.反应Ⅱ的能量过程示意图如图2所示 |
C.断开3 mol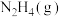 中的化学键吸收的能量大于形成1 mol 中的化学键吸收的能量大于形成1 mol 和4 mol 和4 mol 中的化学键释放的能量 中的化学键释放的能量 |
| D.图l所示过程①是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
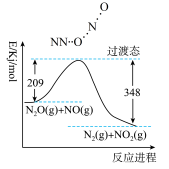
【推荐2】由 和
和 反应生成
反应生成 和
和 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是
 和
和 反应生成
反应生成 和
和 的能量变化如图所示。下列说法不正确的是
的能量变化如图所示。下列说法不正确的是
A.反应生成 时转移 时转移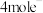 |
| B.反应物能量之和大于生成物能量之和 |
C.每有 氮氮三键形成时,该反应放出139KJ的能量 氮氮三键形成时,该反应放出139KJ的能量 |
| D.断键吸收能量之和小于成键释放能量之和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列说法不正确的是
A.CO(g)的燃烧热是283.0 kJ/mol,则表示CO(g)燃烧热的热化学方程式为:CO (g)+ O2(g)=CO2 (g) △H=−283.0 kJ•mol−1 O2(g)=CO2 (g) △H=−283.0 kJ•mol−1 |
B.稀盐酸和稀氢氧化钠溶液反应的中和热为57.3 kJ•mol−1,则表示稀硫酸与稀氢氧化钾溶液中和热的热化学方程式为: H2SO4(l)+KOH(l)= H2SO4(l)+KOH(l)= K2SO4(l)+H2O(l) △H=−57.3 kJ•mol−1 K2SO4(l)+H2O(l) △H=−57.3 kJ•mol−1 |
| C.已知H−H键键能为436 kJ•mol−1,H−N键键能为391 kJ•mol−1,根据化学方程式:N2(g)+3H2(g)=2NH3(g) △H=−92.4kJ•mol−1,则N≡N键的键能约为946kJ•mol−1 |
| D.一定条件下,反应2CO(g)=CO2(g)+C(s)可自发进行,则该反应的△H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
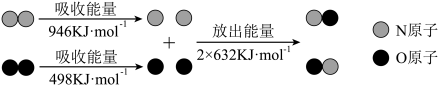
【推荐1】 和
和 反应生成
反应生成 过程中的能量变化如图所示。下列说法正确的是
过程中的能量变化如图所示。下列说法正确的是
 和
和 反应生成
反应生成 过程中的能量变化如图所示。下列说法正确的是
过程中的能量变化如图所示。下列说法正确的是
A.通常情况下,NO比 稳定 稳定 |
B. 的总能量小于 的总能量小于 和 和 的能量总和 的能量总和 |
C.  |
D.断开1mol  中化学键需要放出632 kJ能量 中化学键需要放出632 kJ能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据热化学方程式S(s)+O2(g)═SO2(g) △H=﹣297.23kJ•mol﹣1,分析下列说法正确的是
| A.S(g)═S(s)△H>0 |
| B.S(g)+O2(g)═SO2(g) △H=297.23kJ•mol﹣1 |
| C.S(g)+O2(g)═SO2(g) △H<297.23kJ•mol﹣1 |
| D.1molSO2(g)所具有的能量小于1molS(s)与1molO2(g)所具有的能量之和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某反应使用催化剂后,其反应过程中能量变化如图所示。下列说法错误的是


| A.该反应的总反应为放热反应 | B.使用催化剂,可以改变反应热 |
| C.反应①是吸热反应,反应②是放热反应 | D.ΔH=ΔH1+ΔH2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.使用催化剂可以有效减少反应放出的热量 |
| B.升高温度增加了反应物中活化分子百分数 |
| C.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g) △H2;则:△H1>△H2 |
| D.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则:石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】2013年以来,全国很多地区都曾陷入严重的雾霾和污染天气中,冬季取暖排放的CO2、汽车尾气等都是形成雾霾的因素。已知:
① N2(g) + O2(g)=2NO(g) △H=+179.5 kJ/mol
②2NO(g) + O2(g)=2NO2(g) △H=-112.3 kJ/mol
③2NO(g) +2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol
下图是在101kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中能量变化的示意图。则a的值为

① N2(g) + O2(g)=2NO(g) △H=+179.5 kJ/mol
②2NO(g) + O2(g)=2NO2(g) △H=-112.3 kJ/mol
③2NO(g) +2CO(g)=N2(g) +2CO2(g) △H=-759.8 kJ/mol
下图是在101kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中能量变化的示意图。则a的值为

| A.368 | B.100 | C.602 | D.334 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国科研人员提出了由 CO2和 CH4 转化为高附加值产品CH3COOH 的催化反应历程,该历程如图所示:下列说法正确的是
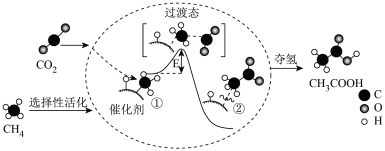

| A.该反应为吸热反应 |
| B.反应过程中,只有 C-H 键发生断裂 |
| C.状态①②之间的能量差即该反应的焓变 |
| D.反应速率与催化剂表面积有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知一定条件下断裂或生成某些化学键的能量关系如下表:
对于反应:H2(g)+ Cl2 (g) =2HCl (g) ,下列说法错误的是
| 断裂或生成的化学键 | 能量数据 |
| 断裂1mol H2分子中的化学键 | 吸收能量436kJ |
| 断裂1mol Cl2分子中的化学键 | 吸收能量243kJ |
| 形成1mol HCl分子中的化学键 | 释放能量431kJ |
| A.该反应的反应热 △H < 0 |
| B.形成1mol HCl化学键时放热431 kJ |
| C.氯化氢分子中的化学键比氯气分子中的化学键更稳定 |
| D.相同条件下,氢气分子具有的总能量高于氯化氢分子具有的能量 |
您最近一年使用:0次

 反应过程的能量变化如图所示,下列说法
反应过程的能量变化如图所示,下列说法






