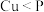已知四种晶体的熔点:
由此得出的推论错误的是
| 物质 | CF4 | SiF4 | BF3 | AlF3 |
| 熔点/℃ | -184 | -90 | -127 | >1000 |
| A.CF4在常温常压下不是固体 | B.分子间作用力: SiF4>CF4 |
| C.BF3一定是分子晶体 | D.AlF3一定是原子晶体 |
更新时间:2022-06-03 20:44:35
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】根据表中数据,下列说法错误的是
| AlCl3 | NaCl | MgO | Na | W(钨) | |
| 熔点/℃ | 190 | 801 | 2852 | 98 | 3410 |
| 沸点/℃ | 182.7 | 1412 | 3600 | 883 | 5927 |
| A.金属晶体的熔沸点比离子晶体低 |
| B.MgO 的晶格能高于 NaCl |
| C.AlCl3是分子晶体,加热能升华 |
| D.钨的金属键强于钠导致其熔点高于钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于晶体的说法中,不正确的是( )
①含有离子的晶体一定是离子晶体
②分子晶体若是密堆积方式,其配位数都是12
③晶胞是晶体结构的基本单元
④共价键的强弱决定分子晶体熔沸点的高低
⑤MgO远比NaCl的晶格能大
⑥含有共价键的晶体一定是原子晶体
⑦分子晶体的熔点一定比金属晶体低
⑧NaCl晶体中,阴、阳离子的配位数都为6
①含有离子的晶体一定是离子晶体
②分子晶体若是密堆积方式,其配位数都是12
③晶胞是晶体结构的基本单元
④共价键的强弱决定分子晶体熔沸点的高低
⑤MgO远比NaCl的晶格能大
⑥含有共价键的晶体一定是原子晶体
⑦分子晶体的熔点一定比金属晶体低
⑧NaCl晶体中,阴、阳离子的配位数都为6
| A.①④⑥⑦ | B.②④⑥⑧ | C.③⑤⑦⑧ | D.③④⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关说法,正确的是
| A.H2O 的沸点高于HF,是因为氢键作用O-H•••O大于F-H•••F |
| B.晶体硅的熔点大于SiO2,因为Si-Si键能大于Si-O键能 |
| C.乙硫醇(CH3CH2SH)沸点大于乙醇(CH3CH2OH),因为前者相对分子质量大 |
D.NO 的等电子体有CO 的等电子体有CO 、BF3,它们的结构均为平面正三角形 、BF3,它们的结构均为平面正三角形 |
您最近一年使用:0次
【推荐2】已知: 发生水解反应的机理如图:
发生水解反应的机理如图:
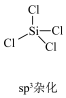
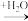


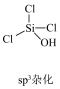
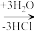
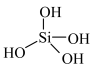
下列叙述正确的是
 发生水解反应的机理如图:
发生水解反应的机理如图:
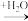



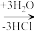

下列叙述正确的是
A. 的键角与白磷( 的键角与白磷( )的键角相同 )的键角相同 |
B. 脱水后加热分解得到的晶体中每个 脱水后加热分解得到的晶体中每个 可构成12个12元环 可构成12个12元环 |
C. 属于原子晶体(共价晶体) 属于原子晶体(共价晶体) |
D. 不能按照上述机理发生水解反应,原因是 不能按照上述机理发生水解反应,原因是 的原子半径小 的原子半径小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】关于下列晶体物质的熔沸点高低排列判断正确的是( )
| A.Rb>K>Na | B.金刚石>晶体硅>二氧化硅>碳化硅 |
| C.H2O>H2S>H2Se>H2Te | D.CaO>BaO>NaCl>KCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列物质按沸点降低顺序的一组是
| A.CI4、CBr4、CCl4、CF4 | B.O、S、Se、Te |
| C.HF、HCl、HBr、HI | D.H2Te、H2Se、H2S、H2O |
您最近一年使用:0次

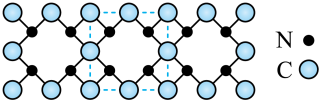
 价,氮显
价,氮显 价
价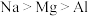
 用于制造磷青铜,电负性:
用于制造磷青铜,电负性: