硫是人类认识最早的元素之一,含硫物质在现代生产和生活中发挥着重要作用。某小组同学验证SO2的性质。装置如图所示,培养皿中A、B、C三个塑料瓶盖内盛不同物质。向Na2SO3固体上滴加70%硫酸,迅速用玻璃片将培养皿盖严,实验记录下。
已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
(1)瓶盖_______ (填字母)中的实验现象能证明SO2具有还原性,并写出反应的现象_______ 。
(2)瓶盖B中的现象证明SO2具有的性质是_______ ;瓶盖C中发生反应的化学方程式为_______ 。
(3)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是_______ (填字母)。
a.石蕊溶液 b.NaCl溶液
(4)将SO2气体通入H2S的水溶液中,生成淡黄色的浑浊,证明SO2具有的性质是_______ ;写出反应的化学方程式_______ 。
| 实验装置 | 瓶盖 | 物质 | 实验现象 |
 | A | KMnO4酸性溶液 | 溶液褪色 |
| B | 蘸有品红溶液的棉花 | 品红溶液褪色 | |
| C | 蒸馏水 | 无明显变化 |
(1)瓶盖
(2)瓶盖B中的现象证明SO2具有的性质是
(3)瓶盖C中无明显变化,若要证明C中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.石蕊溶液 b.NaCl溶液
(4)将SO2气体通入H2S的水溶液中,生成淡黄色的浑浊,证明SO2具有的性质是
更新时间:2022-06-08 20:17:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某小组同学利用下图所示装置探究 性质。回答下列问题:
性质。回答下列问题:

(1)实验室常用亚硫酸钠与浓硫酸共热制取二氧化硫,反应的化学方程式为_____ 。
(2)试管② 溶液的作用是
溶液的作用是_____ (用化学方程式解释)。
(3)若X为品红溶液,可观察到试管①中溶液_____ (填实验现象,下同),反应后取下试管①并加热,观察到的现象是_____ 。
(4)若 为酸性
为酸性 溶液,可观察到试管①中溶液由紫色变为无色,由此可知
溶液,可观察到试管①中溶液由紫色变为无色,由此可知 具有
具有_____ (填“氧化性”或“还原性”);推断无色溶液中所含的离子是 、
、 、
、 和
和_____ 。
(5)若 为
为 溶液,写出试管①中反应的化学方程式
溶液,写出试管①中反应的化学方程式_____ 。
 性质。回答下列问题:
性质。回答下列问题:
(1)实验室常用亚硫酸钠与浓硫酸共热制取二氧化硫,反应的化学方程式为
(2)试管②
 溶液的作用是
溶液的作用是(3)若X为品红溶液,可观察到试管①中溶液
(4)若
 为酸性
为酸性 溶液,可观察到试管①中溶液由紫色变为无色,由此可知
溶液,可观察到试管①中溶液由紫色变为无色,由此可知 具有
具有 、
、 、
、 和
和(5)若
 为
为 溶液,写出试管①中反应的化学方程式
溶液,写出试管①中反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有关FeSO4的转化关系如图所示(无关物质已略去)。

已知:①X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,产生白色沉淀。
②Y是红棕色的化合物。
(1)气体X的成分是____________________________________________ (填化学式)。
(2)反应Ⅰ的反应类型属于______________ (填字母)。
a.分解反应 b.复分解反应 c.置换反应
d.化合反应 e.氧化还原反应
(3)溶液2中金属阳离子的检验方法是_____________________________________________ 。
(4)若经反应Ⅰ得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol·L-1 NaOH溶液完全吸收,则反应Ⅰ的化学方程式是________________________________ ,反应Ⅳ中生成FeSO4的离子方程式是____________________________________________________ 。

已知:①X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,产生白色沉淀。
②Y是红棕色的化合物。
(1)气体X的成分是
(2)反应Ⅰ的反应类型属于
a.分解反应 b.复分解反应 c.置换反应
d.化合反应 e.氧化还原反应
(3)溶液2中金属阳离子的检验方法是
(4)若经反应Ⅰ得到16 g固体Y,产生的气体X恰好被0.4 L 1 mol·L-1 NaOH溶液完全吸收,则反应Ⅰ的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校兴趣小组设计实验探究SO2与新制Cu(OH)2悬浊液反应的产物。按图连接好装置(夹持装置省略),打开磁搅拌器,先往20 mL 1.0 mol·L-1的CuCl2 溶液中加入20 mL 2.0 mol·L-1的NaOH溶液,再通入一定量SO2,三颈烧瓶中生成大量白色沉淀X。
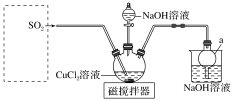
回答下列问题:
(1)以亚硫酸钠和浓硫酸为原料制取SO2,虚框中应选用_______ (填“A”或“B”)装置,写出该装置制备SO2的化学方程式_______ 。实验室制备SO2一般选择70%的浓硫酸,不选择98.3%的浓硫酸的理由是_______ 。

(2)仪器a的名称为_______ ,烧杯中发生反应的离子方程式为_______ 。
(3)据SO2是酸性氧化物,推测X可能为_______ 。取少量X加入稀硫酸进行验证,观察到_______ ,说明该推测错误。
(4)根据实验验证X为CuCl,写出生成X的离子方程式为_____ 。说明SO2具有_____ 。

回答下列问题:
(1)以亚硫酸钠和浓硫酸为原料制取SO2,虚框中应选用

(2)仪器a的名称为
(3)据SO2是酸性氧化物,推测X可能为
(4)根据实验验证X为CuCl,写出生成X的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】如图是硫元素的价类二维图。
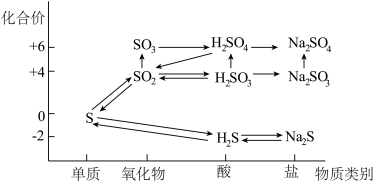
(1)完成上图中的化学方程式:
①S→SO2:_______ ;
②H2S→S:_______ ;
③H2SO3→H2SO4:_______ ;
④H2SO4→SO2:_______ ;
(2)下列关于硫的说法错误的是_______。
(3)分别将足量下列气体通入稀 Na2S 溶液中,可以使溶液变浑浊的是_______。
(4)根据下面的硫元素的“价—类”二维图分析,下列有关说法正确的是_______。
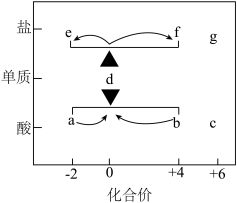

(1)完成上图中的化学方程式:
①S→SO2:
②H2S→S:
③H2SO3→H2SO4:
④H2SO4→SO2:
(2)下列关于硫的说法错误的是_______。
| A.试管内壁附着的硫可用二硫化碳溶解除去 |
| B.游离态的硫存在于火山喷口附近或地壳的岩层里 |
| C.单质硫既有氧化性,又有还原性 |
| D.硫在过量纯氧中的燃烧产物是三氧化硫 |
| A.CO | B.Cl2 | C.SO2 | D.HCl |

| A.在酸性条件下,将 e 和 f 的钠盐溶液混合,会有 d 生成 |
| B.图中 d、f、b 既有氧化性又有还原性 |
| C.将 b 的稀溶液滴加到品红溶液中,品红溶液褪色,体现了 b 的强氧化性 |
| D.将 c 的浓溶液滴加在胆矾晶体上,晶体由蓝色变成白色,体现了 c 的脱水性 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组探究 与
与 溶液的反应,设计实验装置如图1(夹持和加热装置略):
溶液的反应,设计实验装置如图1(夹持和加热装置略):
(1)盛有浓硫酸的仪器名称为___________ ,A中发生反应的化学方程式为___________ 。

(2)反应开始后,A中 固体表面有气泡产生同时有白雾生成,B中有白色沉淀。甲同学认为B中白色沉淀是
固体表面有气泡产生同时有白雾生成,B中有白色沉淀。甲同学认为B中白色沉淀是 。乙同学检验该白色沉淀不溶于盐酸,则该沉淀为
。乙同学检验该白色沉淀不溶于盐酸,则该沉淀为___________ (填化学式),乙就白色沉淀产生的原因提出了两种假设:
①A中产生的白雾是浓硫酸的酸雾,进入B中与 反应生成白色沉淀;
反应生成白色沉淀;
②___________ 。
(3)为证明 与
与 溶液不能得到
溶液不能得到 沉淀,乙设计实验装置如图2。
沉淀,乙设计实验装置如图2。

步骤为:①打开弹簧夹,通入 一段时间后关闭弹簧夹;②滴加浓硫酸,加热A,A中
一段时间后关闭弹簧夹;②滴加浓硫酸,加热A,A中 固体表面有气泡产生同时有白雾生成;B、C试管中有气泡产生,无其它明显现象;D中红色褪去。
固体表面有气泡产生同时有白雾生成;B、C试管中有气泡产生,无其它明显现象;D中红色褪去。
步骤①通 的目的是
的目的是___________ ,试管B中试剂是___________ 。通过实验,得出 与
与 溶液不能得到
溶液不能得到 沉淀。
沉淀。
(4)丙同学取乙实验后的C中溶液,滴加一种无色溶液,有少量白色沉淀生成,滴加的试剂可能是___________。
 与
与 溶液的反应,设计实验装置如图1(夹持和加热装置略):
溶液的反应,设计实验装置如图1(夹持和加热装置略):(1)盛有浓硫酸的仪器名称为

(2)反应开始后,A中
 固体表面有气泡产生同时有白雾生成,B中有白色沉淀。甲同学认为B中白色沉淀是
固体表面有气泡产生同时有白雾生成,B中有白色沉淀。甲同学认为B中白色沉淀是 。乙同学检验该白色沉淀不溶于盐酸,则该沉淀为
。乙同学检验该白色沉淀不溶于盐酸,则该沉淀为①A中产生的白雾是浓硫酸的酸雾,进入B中与
 反应生成白色沉淀;
反应生成白色沉淀;②
(3)为证明
 与
与 溶液不能得到
溶液不能得到 沉淀,乙设计实验装置如图2。
沉淀,乙设计实验装置如图2。
步骤为:①打开弹簧夹,通入
 一段时间后关闭弹簧夹;②滴加浓硫酸,加热A,A中
一段时间后关闭弹簧夹;②滴加浓硫酸,加热A,A中 固体表面有气泡产生同时有白雾生成;B、C试管中有气泡产生,无其它明显现象;D中红色褪去。
固体表面有气泡产生同时有白雾生成;B、C试管中有气泡产生,无其它明显现象;D中红色褪去。步骤①通
 的目的是
的目的是 与
与 溶液不能得到
溶液不能得到 沉淀。
沉淀。(4)丙同学取乙实验后的C中溶液,滴加一种无色溶液,有少量白色沉淀生成,滴加的试剂可能是___________。
| A.氨水 | B.新制氯水 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】非金属单质 经如图所示的过程转化为含氧酸
经如图所示的过程转化为含氧酸 ,已知
,已知 为强酸,请回答下列问题:
为强酸,请回答下列问题:

(1)若 在常温下为固体,
在常温下为固体,  是能使品红溶液褪色的有刺激性气味的无色气体。
是能使品红溶液褪色的有刺激性气味的无色气体。
① 的化学式是
的化学式是__________ 。
②在工业生产中, 气体的大量排放被雨水吸收后形成了
气体的大量排放被雨水吸收后形成了__________ 而污染了环境。
(2)若 在常温下为气体,
在常温下为气体,  是红棕色的气体。
是红棕色的气体。
① 的化学式是
的化学式是__________ 。
② 的浓溶液在常温下可与铜反应并生成
的浓溶液在常温下可与铜反应并生成 气体,请写出该反应的化学方程式
气体,请写出该反应的化学方程式________________ 。
 经如图所示的过程转化为含氧酸
经如图所示的过程转化为含氧酸 ,已知
,已知 为强酸,请回答下列问题:
为强酸,请回答下列问题:
(1)若
 在常温下为固体,
在常温下为固体,  是能使品红溶液褪色的有刺激性气味的无色气体。
是能使品红溶液褪色的有刺激性气味的无色气体。①
 的化学式是
的化学式是②在工业生产中,
 气体的大量排放被雨水吸收后形成了
气体的大量排放被雨水吸收后形成了(2)若
 在常温下为气体,
在常温下为气体,  是红棕色的气体。
是红棕色的气体。①
 的化学式是
的化学式是②
 的浓溶液在常温下可与铜反应并生成
的浓溶液在常温下可与铜反应并生成 气体,请写出该反应的化学方程式
气体,请写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室可用图中装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。___________ ,装置A中发生反应的化学方程式为___________ 。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若___________ ,则整个装置气密性良好。
(3)装置B的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择___________ (填序号)。
a.蒸馏水 b.饱和 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液
(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案II:向第二份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案III:向第三份溶液中加入 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。
上述方案中合理的是方案___________ (填“I”“II”或“III”)。
 并验证其性质。
并验证其性质。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若
(3)装置B的作用之一是通过观察产生气泡的多少判断
 生成的快慢,其中的液体最好选择
生成的快慢,其中的液体最好选择a.蒸馏水 b.饱和
 溶液 c.饱和
溶液 c.饱和 溶液 d.饱和
溶液 d.饱和 溶液
溶液(4)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(5)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案II:向第二份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案III:向第三份溶液中加入
 溶液,有产生白色沉淀。
溶液,有产生白色沉淀。上述方案中合理的是方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。

(1)盛装Na2SO3的仪器名称为_______ 。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若_______ ,则整个装置气密性良好。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择_______ (填字母)。
a.蒸馏水
b.饱和NaHCO3溶液
c.饱和NaHSO3溶液
d.饱和NaOH溶液
(3)装置C中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ :向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);装置D中发生反应的离子方程式为_______ 。
(5)装置E的作用是_______ ,装置F中为_______ 溶液。

(1)盛装Na2SO3的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水
b.饱和NaHCO3溶液
c.饱和NaHSO3溶液
d.饱和NaOH溶液
(3)装置C中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ :向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案合理的是方案
(5)装置E的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室为探究铁与浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验。
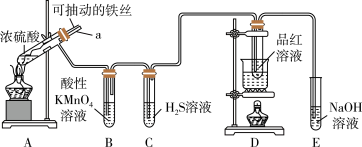
请回答下列问题:
(1)实验时将导管a插入试管中,可使装置B中的溶液不发生倒吸。其原因是______ 。
(2)装置B中酸性KMnO4溶液逐渐褪色,则装置B中发生反应的离子方程式是_____ ;装置C中出现的现象是________ 。
(3)装置D的作用是__________ ;实验结束时需从导管a通入大量空气,其目的是_______ 。
(4)若装置A反应后的溶液中金属阳离子只含有Fe3+,则装置A中发生反应的化学方程式是_____ 。

请回答下列问题:
(1)实验时将导管a插入试管中,可使装置B中的溶液不发生倒吸。其原因是
(2)装置B中酸性KMnO4溶液逐渐褪色,则装置B中发生反应的离子方程式是
(3)装置D的作用是
(4)若装置A反应后的溶液中金属阳离子只含有Fe3+,则装置A中发生反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:氧化性:IO3->Fe3+>I2;还原性:S2O32->I-
3I2+6OH- IO3-+5I-+3H2O;KI+I2
IO3-+5I-+3H2O;KI+I2 KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。
第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是_________ (用化学式表示);CCl4中显紫红的物质是________ (用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为:_________ 、____________ 。
(2)KI作为食盐的加碘剂在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下KI与氧气反应的化学方程式:________________ 。将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?_____ (填“是”或“否”),并说明理由______________ 。
3I2+6OH-
 IO3-+5I-+3H2O;KI+I2
IO3-+5I-+3H2O;KI+I2 KI3
KI3(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。
第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是
②第二份试液中加入足量KI固体后,反应的离子方程式为:
(2)KI作为食盐的加碘剂在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下KI与氧气反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Na2O2能与CO2反应生成氧气,在潜水艇中用作制氧剂。某学生以足量的大理石、足量的盐酸和Na2O2样品为原料,验证Na2O2能与CO2反应生成O2,设计出如下实验装置:
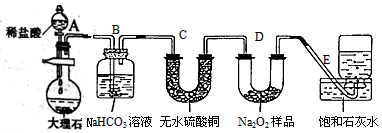
(1)装置B中发生的离子反应方程式是___________________________ ;
(2)装置D的化学反应方程式是_________________________________ ;
(3)若E中的石灰水出现轻微白色浑浊,原因可能是___________________________ ;
(4)如何验证Na2O2能与CO2反应生成O2:____________________________________ ;

(1)装置B中发生的离子反应方程式是
(2)装置D的化学反应方程式是
(3)若E中的石灰水出现轻微白色浑浊,原因可能是
(4)如何验证Na2O2能与CO2反应生成O2:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校化学实验兴趣小组为了探究在实验室制备 的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略).
的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略).

按要求回答问题:
(1)写出制取氯气时装置A中发生的反应的离子方程式______ .
(2)①装置B中盛放的试剂名称为______ ,作用是______ .
②装置D和E中出现的不同现象说明的问题是______ .
③装置F的作用是______ .
(3)写出装置G中发生反应的离子方程式______ .
(4)“洁厕灵”与“84”消毒液反应也能制备 ,写出该反应的化学方程式
,写出该反应的化学方程式______ .
 的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略).
的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略).
按要求回答问题:
(1)写出制取氯气时装置A中发生的反应的离子方程式
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明的问题是
③装置F的作用是
(3)写出装置G中发生反应的离子方程式
(4)“洁厕灵”与“84”消毒液反应也能制备
 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次



