我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。
I.海水的淡化多用蒸馏法,蒸馏法的优点是设备简单、操作简便、淡水质量好,但也有明显缺陷。
(1)海水淡化的方法还有_______ 、_______ 。
II.空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如图。
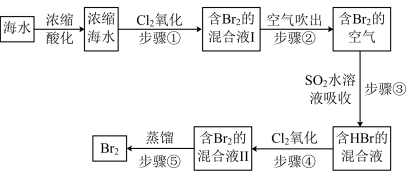
(2)步骤①中获得 的离子方程式为
的离子方程式为_______ 。
(3)步骤②用空气将溴吹出,是因为溴单质_______(填序号)
(4)步骤③中反应的化学方程式为_______ 。
(5)根据上述反应可判断 、
、 、
、 三种物质氧化性由强到弱的顺序
三种物质氧化性由强到弱的顺序_______ 。
III.海带灰中富含以I-形式存在的碘元素。实验室提取 的流程如图所示。
的流程如图所示。
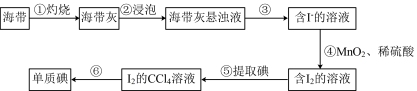
(6)步骤③的实验操作名称为_______ 。
(7)步骤④中反应的离子方程式为_______ 。
(8)检验步骤⑤提取碘后的水溶液中是否含有单质碘,可用的试剂为_______ 。
I.海水的淡化多用蒸馏法,蒸馏法的优点是设备简单、操作简便、淡水质量好,但也有明显缺陷。
(1)海水淡化的方法还有
II.空气吹出法是用于工业规模海水提溴的常用方法。其工艺流程如图。

(2)步骤①中获得
 的离子方程式为
的离子方程式为(3)步骤②用空气将溴吹出,是因为溴单质_______(填序号)
| A.化学性质稳定 | B.沸点低,易挥发 | C.不溶于水 | D.易升华 |
(5)根据上述反应可判断
 、
、 、
、 三种物质氧化性由强到弱的顺序
三种物质氧化性由强到弱的顺序III.海带灰中富含以I-形式存在的碘元素。实验室提取
 的流程如图所示。
的流程如图所示。
(6)步骤③的实验操作名称为
(7)步骤④中反应的离子方程式为
(8)检验步骤⑤提取碘后的水溶液中是否含有单质碘,可用的试剂为
更新时间:2022-06-30 19:13:50
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】当下国际局势紧张,金属钨和单晶硅是重要的军事、科技战略资源。从硫钨矿可以制取金属钨和单晶硅,硫钨矿的主要成分是CaWO4,还包括FeS、SiO2等,某工艺生产流程如图:

已知:常温下,Ksp(CaWO4)=1.0×10-8,Ksp(CaCO3)=1.0×10-9。回答下列问题:
(1)将硫钨矿在空气中高温焙烧,请写出焙烧时FeS发生的化学方程式:_______ 。
(2)写出一种加快焙烧速率的方法:_______ 。
(3)“溶浸”时,_______ (填“能”或“不能”)将纯碱换成烧碱;“操作1”中玻璃棒的作用是_______ 。
(4)滤渣的主要成分是SiO2和将滤渣高温煅烧产生CO2,请从化学反应进行的方向解释由SiO2产生CO2的原因:_______ 。(请用化学方程式及相关文字解释)
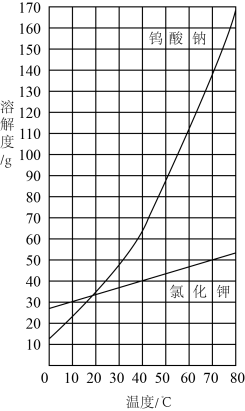
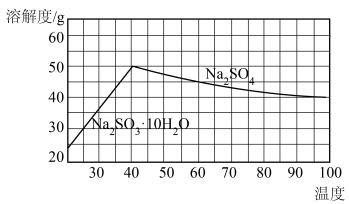
(5)“滤液”是Na2WO4溶液,Na2WO4,在水中的溶解度随温度变化如图所示,“滤液”获得钨酸钠二水合物晶体的操作方法是_______ 、_______ 过滤、洗涤。

已知:常温下,Ksp(CaWO4)=1.0×10-8,Ksp(CaCO3)=1.0×10-9。回答下列问题:
(1)将硫钨矿在空气中高温焙烧,请写出焙烧时FeS发生的化学方程式:
(2)写出一种加快焙烧速率的方法:
(3)“溶浸”时,
(4)滤渣的主要成分是SiO2和将滤渣高温煅烧产生CO2,请从化学反应进行的方向解释由SiO2产生CO2的原因:
(5)“滤液”是Na2WO4溶液,Na2WO4,在水中的溶解度随温度变化如图所示,“滤液”获得钨酸钠二水合物晶体的操作方法是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】合成氨工业产生的钻钼废催化剂(主要成分MoS2、CoO、Fe2O3等)是一种相当宝贵的二次资源。用碱浸法处理钻钼废催化剂的工艺流程如图:
i.氧化钼(MoO3):熔点795℃。易升华(即使在低于熔点情况下,也有显著的升华现象)。
ii.钼酸(H2MoO4):难溶于水和酸的黄色晶体,可通过酸化钼酸盐溶液而制得。
(1)焙烧:
①将废催化剂在空气中焙烧可生成氧化钼,写出反应的化学方程式_______ 。
②解释钼浸取率随焙烧温度变化的原因是_______ 。
碱浸时杂质钴元素以Co(OH)2的形式浸出,加入双氧水可将其氧化为Co(OH)3沉淀。写出反应的化学方程式_______ 。
(3)酸沉:
传统工艺中酸沉多在不锈钢离心机中进行。文献记载,选用浓硝酸比用硫酸和盐酸效果更佳,可避免Mo(VI)还原成低价态,利用了浓硝酸的_______ 性。
(4)从母液中获得无水Na2SO4的操作是_______ 。

i.氧化钼(MoO3):熔点795℃。易升华(即使在低于熔点情况下,也有显著的升华现象)。
ii.钼酸(H2MoO4):难溶于水和酸的黄色晶体,可通过酸化钼酸盐溶液而制得。
(1)焙烧:
①将废催化剂在空气中焙烧可生成氧化钼,写出反应的化学方程式
②解释钼浸取率随焙烧温度变化的原因是
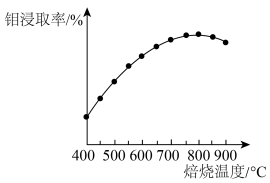
碱浸时杂质钴元素以Co(OH)2的形式浸出,加入双氧水可将其氧化为Co(OH)3沉淀。写出反应的化学方程式
(3)酸沉:
传统工艺中酸沉多在不锈钢离心机中进行。文献记载,选用浓硝酸比用硫酸和盐酸效果更佳,可避免Mo(VI)还原成低价态,利用了浓硝酸的
(4)从母液中获得无水Na2SO4的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】碘化钠可用于医学和摄影.实验室制备 的基本实验步骤为①检查装置气密性;②关闭K,向B中滴入
的基本实验步骤为①检查装置气密性;②关闭K,向B中滴入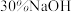 溶液,制得
溶液,制得 ;③打开K,通入
;③打开K,通入 至饱和制得
至饱和制得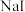 ,同时有黄色沉淀产生;④关闭K,向所得溶液中加入稀硫酸,水浴加热,充分逸出
,同时有黄色沉淀产生;④关闭K,向所得溶液中加入稀硫酸,水浴加热,充分逸出 ;
;
⑤把B中的混合液倒入烧杯,加入足量碳酸钡除去稀硫酸再经过一系列操作得到 成品.
成品.
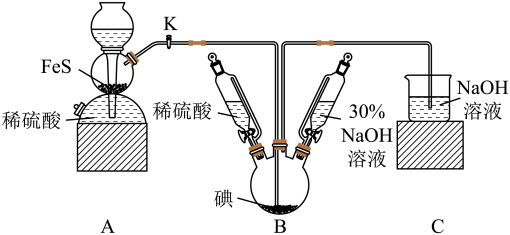
回答下列问题:
(1)盛稀硫酸和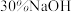 溶液的仪器,若换成分液漏斗,其缺点是
溶液的仪器,若换成分液漏斗,其缺点是_________ .
(2)A装置中发生反应的离子方程式为________ ,C装置的作用为_________ .
(3)步骤②可观察到的现象是_________ .
(4)制得 的离子方程式为
的离子方程式为_________ .通入 至饱和,与
至饱和,与 反应制得
反应制得 的离子方程式为
的离子方程式为________ .
(5)步骤⑤中的“一系列操作”包括过滤、洗涤、合并滤液和洗涤液、________ 等操作.
(6)三颈烧瓶加入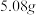 碘单质,若期望反应的产率为88%则最终得到产品的质量为
碘单质,若期望反应的产率为88%则最终得到产品的质量为______ .
 的基本实验步骤为①检查装置气密性;②关闭K,向B中滴入
的基本实验步骤为①检查装置气密性;②关闭K,向B中滴入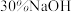 溶液,制得
溶液,制得 ;③打开K,通入
;③打开K,通入 至饱和制得
至饱和制得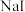 ,同时有黄色沉淀产生;④关闭K,向所得溶液中加入稀硫酸,水浴加热,充分逸出
,同时有黄色沉淀产生;④关闭K,向所得溶液中加入稀硫酸,水浴加热,充分逸出 ;
;⑤把B中的混合液倒入烧杯,加入足量碳酸钡除去稀硫酸再经过一系列操作得到
 成品.
成品.
回答下列问题:
(1)盛稀硫酸和
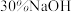 溶液的仪器,若换成分液漏斗,其缺点是
溶液的仪器,若换成分液漏斗,其缺点是(2)A装置中发生反应的离子方程式为
(3)步骤②可观察到的现象是
(4)制得
 的离子方程式为
的离子方程式为 至饱和,与
至饱和,与 反应制得
反应制得 的离子方程式为
的离子方程式为(5)步骤⑤中的“一系列操作”包括过滤、洗涤、合并滤液和洗涤液、
(6)三颈烧瓶加入
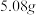 碘单质,若期望反应的产率为88%则最终得到产品的质量为
碘单质,若期望反应的产率为88%则最终得到产品的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯化钾样品中含有少量氯化镁、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
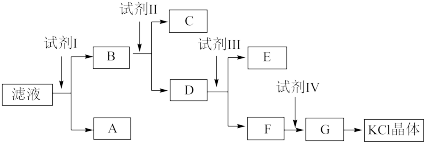
(1)已知步骤①②③④中加入的试剂均为过量,所得物质A是一种难溶于酸的沉淀,物质C属于碱,则试剂I的化学式为_________ ,试剂Ⅱ的化学式为__________ ,物质E的化学式为__________ ,试剂Ⅳ的化学式为__________ 。
(2)步骤①②③④中均采用了相同的分离提纯操作为_________ ,检验提纯后的KCl溶液中是否还含有 的方法是:
的方法是:_____________________________________ 。

(1)已知步骤①②③④中加入的试剂均为过量,所得物质A是一种难溶于酸的沉淀,物质C属于碱,则试剂I的化学式为
(2)步骤①②③④中均采用了相同的分离提纯操作为
 的方法是:
的方法是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】碳酸锰主要用于制备软磁铁氧体,工业上以软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)为主要原料制备碳酸锰(MnCO3难溶,分解温度较高)的一种工艺流程如下:
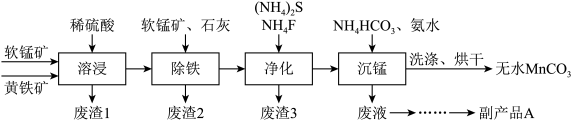
已知:几种金属离子沉淀的pH如下表:
回答下列问题:
(1)为了提高溶浸工序中原料的浸出效率,可以采取的措施有___________ (至少2条)。
(2)请写出“溶浸”过程中反应的离子方程式:___________ 。
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。请写出除去Cu2+的离子方程式:___________ 。若测得滤液中c(Fˉ)=0.01mol·Lˉ1,则滤液中残留c(Ca2+)=___________ mol·Lˉ1.[已知:Ksp(CaF2)=1.5×10ˉ10]
(4)除铁工序中,先加入适量的软锰矿,其作用是___________ ,再加入石灰调节溶液的pH的范围为___________ 。
(5)副产品A的主要成分是___________ 。

已知:几种金属离子沉淀的pH如下表:
| Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 7.8 | 10.4 |
(1)为了提高溶浸工序中原料的浸出效率,可以采取的措施有
(2)请写出“溶浸”过程中反应的离子方程式:
(3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。请写出除去Cu2+的离子方程式:
(4)除铁工序中,先加入适量的软锰矿,其作用是
(5)副产品A的主要成分是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用。
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O="6Cu+" SO2
在③中被氧化与被还原元素原子的物质的量之比为____________ ;若由3mol CuFeS2生成3molCu,理论上消耗O2的物质的量为______________ 。
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式________________ 。
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:
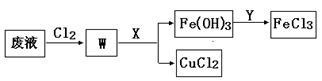
①试剂Y的名称___________ ;物质X最好是__________ (填化学式)。
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5mol·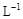 , 则加入Cl2气和物质X使溶液的pH在
, 则加入Cl2气和物质X使溶液的pH在________________ 范围时(设溶液体积保持不变),铁元素完全转化为Fe(OH)3,而CuCl2不产生沉淀。( KSP [Fe(OH)3]=1.0×10—38、 KSP[Cu(OH)2]=2.0×10—20 、 lg5=0.7)
(1)工业上可以用黄铜矿(主要成分CuFeS2)为原料冶炼铜。主要反应如下:
① 2CuFeS2+4O2=Cu2S+3SO2+2FeO ② 2Cu2S + 3O2=2SO2+2Cu2O③ Cu2S+ 2Cu2O="6Cu+" SO2
在③中被氧化与被还原元素原子的物质的量之比为
(2)常温下Cu2O能溶于稀硫酸,得到蓝色溶液和红色固体,可以利用该性质检验工业上冶炼铜得到的粗铜中是否含有Cu2O,写出此反应的离子方程式
(3)刻蚀印刷电路的废液中含有大量的CuCl2、FeCl2、FeCl3,任意排放将导致环境污染和资源的浪费, 为了使FeCl3循环利用和回收CuCl2,现设计如下生产过程:

①试剂Y的名称
②若常温下1L废液中含CuCl2、FeCl2、FeCl3的物质的量浓度均为0.5mol·
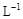 , 则加入Cl2气和物质X使溶液的pH在
, 则加入Cl2气和物质X使溶液的pH在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得一些重要的化工产品。
Ⅰ.从海水提溴工艺流程如下图所示:
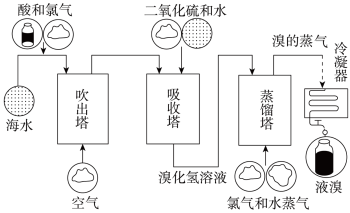
(1)向酸化后的海水中通入氯气,发生的离子方程式是:_______ ,若通入22.4 L Cl2(标准状况),理论上可得Br2_______ g。
(2)在吹出塔中,通入热空气吹出Br2,利用了溴的_______ (填序号)。
①腐蚀性 ②氧化性 ③还原性 ④挥发性
(3)将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生反应以达到富集的目的,该反应中的还原剂是_______ (填化学式)。
(4)蒸馏塔溶液中Br2的浓度比吹出塔溶液中Br2的浓度_______ (填“高”“相等”或“低”)。
(5)蒸馏塔在蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因_______ 。
Ⅱ.从海水中提取镁的方法如下:

(6)该工艺流程中涉及到的基本反应类型有_______ (填反应类型名称)。
(7)电解无水MgCl2所得的镁蒸气可以在下列_______气体中冷却(填序号)。
Ⅰ.从海水提溴工艺流程如下图所示:

(1)向酸化后的海水中通入氯气,发生的离子方程式是:
(2)在吹出塔中,通入热空气吹出Br2,利用了溴的
①腐蚀性 ②氧化性 ③还原性 ④挥发性
(3)将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生反应以达到富集的目的,该反应中的还原剂是
(4)蒸馏塔溶液中Br2的浓度比吹出塔溶液中Br2的浓度
(5)蒸馏塔在蒸馏过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因
Ⅱ.从海水中提取镁的方法如下:

(6)该工艺流程中涉及到的基本反应类型有
(7)电解无水MgCl2所得的镁蒸气可以在下列_______气体中冷却(填序号)。
| A.N2 | B.CO2 | C.Ar | D.O2 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
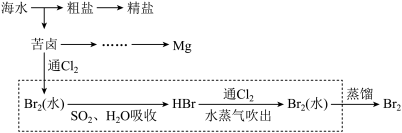
【推荐2】我国地大物博,资源非常丰富,从海水资源获取某些物质的流程示意图如下。
①粗盐中还含有泥沙、 、
、 以及可溶性硫酸盐等杂质,可以依次通过溶解、过滤、
以及可溶性硫酸盐等杂质,可以依次通过溶解、过滤、___________ (选填字母序号;所加试剂均过量)、结晶等一系列流程得到精盐。
a.加入 溶液→加入NaOH溶液→加入
溶液→加入NaOH溶液→加入 溶液→过滤→加入稀盐酸
溶液→过滤→加入稀盐酸
b.加入NaOH溶液→加入 溶液→加入
溶液→加入 溶液→加入稀盐酸→过滤
溶液→加入稀盐酸→过滤
c.加入 溶液→加入
溶液→加入 溶液→加入NaOH溶液→过滤→加入稀盐酸
溶液→加入NaOH溶液→过滤→加入稀盐酸
②检验精盐中镁离子是否除尽的方法是___________ (简述操作、现象及结论)。
③得到的精盐可用于冶炼金属钠,该反应的化学方程式是___________ 。
(2)工业上常用的一种海水提溴技术称为“吹出法”。
①图中虚线框内流程的主要目的是___________ 。
②图中虚线框内流程也可用低浓度
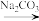 溶液Ⅰ
溶液Ⅰ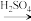
 替代,溶液Ⅰ中含有
替代,溶液Ⅰ中含有 ,请写出
,请写出 与
与 反应的化学方程式
反应的化学方程式___________ ,向溶液Ⅰ中再加入稀硫酸之后可制得溴单质,请写出这步的离子反应方程式___________ 。
(3)已知苦卤的主要成分如下:
理论上,1L苦卤最多可得到 的质量为
的质量为___________ g。
①粗盐中还含有泥沙、
 、
、 以及可溶性硫酸盐等杂质,可以依次通过溶解、过滤、
以及可溶性硫酸盐等杂质,可以依次通过溶解、过滤、a.加入
 溶液→加入NaOH溶液→加入
溶液→加入NaOH溶液→加入 溶液→过滤→加入稀盐酸
溶液→过滤→加入稀盐酸b.加入NaOH溶液→加入
 溶液→加入
溶液→加入 溶液→加入稀盐酸→过滤
溶液→加入稀盐酸→过滤c.加入
 溶液→加入
溶液→加入 溶液→加入NaOH溶液→过滤→加入稀盐酸
溶液→加入NaOH溶液→过滤→加入稀盐酸②检验精盐中镁离子是否除尽的方法是
③得到的精盐可用于冶炼金属钠,该反应的化学方程式是
(2)工业上常用的一种海水提溴技术称为“吹出法”。
①图中虚线框内流程的主要目的是
②图中虚线框内流程也可用低浓度

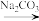 溶液Ⅰ
溶液Ⅰ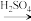
 替代,溶液Ⅰ中含有
替代,溶液Ⅰ中含有 ,请写出
,请写出 与
与 反应的化学方程式
反应的化学方程式(3)已知苦卤的主要成分如下:
| 离子 |  |  |  |  |
浓度/( ) ) | 63.7 | 28.8 | 144.6 | 46.4 |
 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

(1)步骤①反应的离子方程式是____________________________________________ 。
(2)步骤③反应的化学方程式是____________________________________________ 。
(3)Br的原子序数是_________ ,在周期表中位于__________ 周期__________ 族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴_____ ?

(1)步骤①反应的离子方程式是
(2)步骤③反应的化学方程式是
(3)Br的原子序数是
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水资源的利用具有非常广阔的前景。下面是海水综合利用联合工业体系的简图:

回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法有_______ 。(写出一种即可)
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是_______ ;
(3)粗盐中可溶性的杂质离子主要有 、
、 、
、 。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、
。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、 溶液、
溶液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是_______ 。
Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为_______ ;从理论上考虑下列也能吸收 的是
的是_______ 。
A.NaCl B. C.
C. D.
D.
(5)经过步骤①②已获得 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“空气吹出、
的海水进行蒸馏得到液溴,而要经过“空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是_______ ;
Ⅳ.海水提镁
(6)该工业生产过程中,为了使 转化为
转化为 ,应加入的试剂为
,应加入的试剂为_______ ;
(7)写出电解 冶炼金属Mg的化学方程式
冶炼金属Mg的化学方程式_______ 。

回答下列问题:
Ⅰ.海水淡化
(1)人类可以从海水中获得淡水,以解决水资源危机。海水淡化的方法有
Ⅱ.海水制盐
(2)过程Ⅰ采用的操作是
(3)粗盐中可溶性的杂质离子主要有
 、
、 、
、 。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、
。要除去这些杂质离子得到精盐水,过程Ⅱ依次加入了试剂NaOH溶液、 溶液、
溶液、 溶液、盐酸,其中
溶液、盐酸,其中 溶液的作用是
溶液的作用是Ⅲ.海水提溴
(4)工业上从海水中提取溴单质的流程图中,步骤④的离子方程式为
 的是
的是A.NaCl B.
 C.
C. D.
D.
(5)经过步骤①②已获得
 ,不直接用含
,不直接用含 的海水进行蒸馏得到液溴,而要经过“空气吹出、
的海水进行蒸馏得到液溴,而要经过“空气吹出、 吸收、通入氯气”后再蒸馏,其目的是
吸收、通入氯气”后再蒸馏,其目的是Ⅳ.海水提镁
(6)该工业生产过程中,为了使
 转化为
转化为 ,应加入的试剂为
,应加入的试剂为(7)写出电解
 冶炼金属Mg的化学方程式
冶炼金属Mg的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。如图是某工厂海水综合利用的流程图。
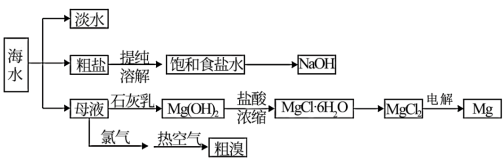
请根据以上信息回答下列问题:
(1)请列举一种海水淡化的方法__ 。
(2)粗盐中含有Ca2+、Mg2+、SO 等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是
等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是__ (填字母)。
A.②③④① B.③④②① C.④③②① D.③②①④
(3)以电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式___ 。
(4)请写出提取镁过程中Mg(OH)2与盐酸反应的离子方程式___ 。
(5)将氯气通入母液中,可将溶液中的溴离子转化为溴单质,请写出该反应的离子方程式__ 。以下是为该工厂氯气寻找货源的设想,其中较合理的是__ (填字母)。
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环

请根据以上信息回答下列问题:
(1)请列举一种海水淡化的方法
(2)粗盐中含有Ca2+、Mg2+、SO
 等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是
等杂质,精制时所用试剂为①盐酸②氯化钡溶液③氢氧化钠溶液④碳酸钠溶液,添加以上试剂合理的顺序是A.②③④① B.③④②① C.④③②① D.③②①④
(3)以电解饱和食盐水为基础制取氯气、烧碱等产品的工业称为氯碱工业,请写出该反应的化学方程式
(4)请写出提取镁过程中Mg(OH)2与盐酸反应的离子方程式
(5)将氯气通入母液中,可将溶液中的溴离子转化为溴单质,请写出该反应的离子方程式
A.从外地购买
B.在当地新建生产厂
C.从本厂生产烧碱处循环
D.从本厂生产镁单质处循环
您最近一年使用:0次
【推荐3】海水水资源和海水化学资源的开发利用具有非常广阔的前景。
Ⅰ.海水淡化
海水淡化的主要方法有蒸馏法、电渗析法、离子交换法。如图是海水蒸馏的原理示意图。

(1)仪器A的名称是_______ 。
(2)实验时按图示装置组装好仪器,检查气密性,装入海水后,先_______ 再_______ (填操作)。冷却水从_______ (填“a”或“b”)端通入。
Ⅱ.从海水中提取溴
从海水中提取溴单质的工艺流程如图:
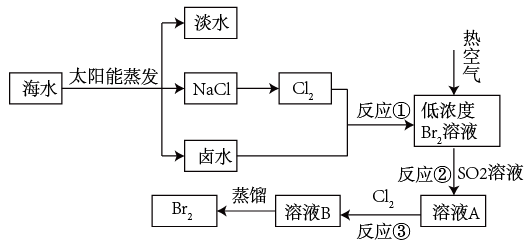
(3)流程中经历反应①到③的主要目的是_______ ,反应②的离子方程式为_______ 。
(4)反应③后所得含 溶液也可以先用萃取剂将
溶液也可以先用萃取剂将 萃取出来后再蒸馏,下列物质可作为萃取剂的是
萃取出来后再蒸馏,下列物质可作为萃取剂的是_______ (填正确答案标号)。
A.乙醇 B. C.环己烷 D.环己烯(
C.环己烷 D.环己烯(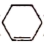 )
)
Ⅰ.海水淡化
海水淡化的主要方法有蒸馏法、电渗析法、离子交换法。如图是海水蒸馏的原理示意图。

(1)仪器A的名称是
(2)实验时按图示装置组装好仪器,检查气密性,装入海水后,先
Ⅱ.从海水中提取溴
从海水中提取溴单质的工艺流程如图:

(3)流程中经历反应①到③的主要目的是
(4)反应③后所得含
 溶液也可以先用萃取剂将
溶液也可以先用萃取剂将 萃取出来后再蒸馏,下列物质可作为萃取剂的是
萃取出来后再蒸馏,下列物质可作为萃取剂的是A.乙醇 B.
 C.环己烷 D.环己烯(
C.环己烷 D.环己烯( )
)
您最近一年使用:0次



