“价—类”二维图是元素化合物知识结构化的良好工具,有利于变化观念的形成。下图是氮元素的“价—类”二维图。请回答下列问题:

(1)C的化学式是_____ ,肼( )可用作火箭的燃料,其在上图中的字母标号为
)可用作火箭的燃料,其在上图中的字母标号为_____ 。
(2)检验A可使用_______ 试纸。A是重要的化工原料,可以合成多种物质,请写出其在工业上制取D的第1步反应方程式_______ 。
(3)铜和足量的D的稀溶液的反应为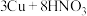 (稀)
(稀)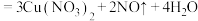 ,当生成11.2L
,当生成11.2L (标准状况)时,转移的电子数目为
(标准状况)时,转移的电子数目为_______ 。反应中D表现的性质为_______ (填标号)。
A.只有还原性 B.还原性和酸性 C.只有强氧化性 D.强氧化性和酸性
(4)一定条件下D分解产生 和另一种气体,写出D分解的化学方程式
和另一种气体,写出D分解的化学方程式_______ 。
(5)若E为硫酸铵,写出以氮气为起始原料制备E的两步制备路线,其它无机试剂任选。_______ (制备路线示例: )
)

(1)C的化学式是
 )可用作火箭的燃料,其在上图中的字母标号为
)可用作火箭的燃料,其在上图中的字母标号为(2)检验A可使用
(3)铜和足量的D的稀溶液的反应为
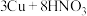 (稀)
(稀)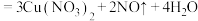 ,当生成11.2L
,当生成11.2L (标准状况)时,转移的电子数目为
(标准状况)时,转移的电子数目为A.只有还原性 B.还原性和酸性 C.只有强氧化性 D.强氧化性和酸性
(4)一定条件下D分解产生
 和另一种气体,写出D分解的化学方程式
和另一种气体,写出D分解的化学方程式(5)若E为硫酸铵,写出以氮气为起始原料制备E的两步制备路线,其它无机试剂任选。
 )
)
更新时间:2022-06-11 17:39:23
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】实验室用废金属矿渣(主要成分是Al、Al2O3、Fe2O3、Fe3O4)为原料制备净水剂高铁酸钾(K2FeO4),流程如下:

(1)试剂a为___________ ,写出加入试剂a后Al发生的化学反应方程式___________ 。
(2)试剂b可以选择下列试剂___________ 。
①氨水②KI③H2O2④铁粉
并写出使用试剂b时,溶液中发生的离子反应方程式___________ 。证明溶液中试剂b加入的量不足的方法是___________ 。
(3)Fe(OH)3与KClO在强碱性条件下反应可制取K2FeO4,KClO转化为KCl,制备过程中氧化剂与还原剂的物质的量之比为___________ 。
(4)实验室可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,制备1molNa2FeO4,反应转移的电子数目为___________ 。

(1)试剂a为
(2)试剂b可以选择下列试剂
①氨水②KI③H2O2④铁粉
并写出使用试剂b时,溶液中发生的离子反应方程式
(3)Fe(OH)3与KClO在强碱性条件下反应可制取K2FeO4,KClO转化为KCl,制备过程中氧化剂与还原剂的物质的量之比为
(4)实验室可用干法制备高铁酸钠,主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,制备1molNa2FeO4,反应转移的电子数目为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】氮在自然界中的部分循环如图。
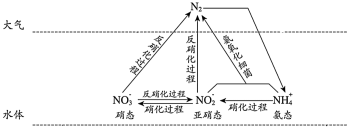
(1)如图所示氮循环中,属于氮的固定的有______ (填字母序号)。
a. 转化为铵态氮 b.硝化过程 c.反硝化过程
转化为铵态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中铵态氮的主要来源之一。
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为______ 。
②检验铵态氮肥中 的实验方案是
的实验方案是______ 。
(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为______ mol。
(4)常温下氨气能被氯气氧化生成 ,化工厂常用此法检验管道是否泄漏氯气,某研究小组用下面装置进行氨气的制备并验证氨气与氯气反应。
,化工厂常用此法检验管道是否泄漏氯气,某研究小组用下面装置进行氨气的制备并验证氨气与氯气反应。
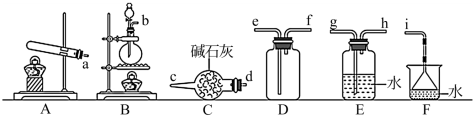
Ⅰ.氨气的制备。欲制备和收集一瓶干燥的氨气可以选择图中的装置______ (填大写字母)。
Ⅱ.氯气与氨气的反应(已知:实验前 、
、 关闭)。
关闭)。
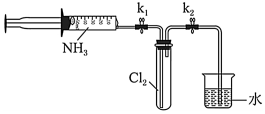
①打开 ,缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭
,缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭 ,恢复至室温。试管中可观察到的现象是
,恢复至室温。试管中可观察到的现象是______ 。发生反应的化学方程式______ 。
②再打开 ,可观察到的现象是
,可观察到的现象是______ 。

(1)如图所示氮循环中,属于氮的固定的有
a.
 转化为铵态氮 b.硝化过程 c.反硝化过程
转化为铵态氮 b.硝化过程 c.反硝化过程(2)氮肥是水体中铵态氮的主要来源之一。
①氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
②检验铵态氮肥中
 的实验方案是
的实验方案是(3)铵态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)常温下氨气能被氯气氧化生成
 ,化工厂常用此法检验管道是否泄漏氯气,某研究小组用下面装置进行氨气的制备并验证氨气与氯气反应。
,化工厂常用此法检验管道是否泄漏氯气,某研究小组用下面装置进行氨气的制备并验证氨气与氯气反应。
Ⅰ.氨气的制备。欲制备和收集一瓶干燥的氨气可以选择图中的装置
Ⅱ.氯气与氨气的反应(已知:实验前
 、
、 关闭)。
关闭)。
①打开
 ,缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭
,缓缓推动注射器活塞,向试管中注入约3倍于氯气体积的氨气,关闭 ,恢复至室温。试管中可观察到的现象是
,恢复至室温。试管中可观察到的现象是②再打开
 ,可观察到的现象是
,可观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】实验室制备并收集干燥、纯净氯气的装置如图所示:

(1)写出实验室制备Cl2的化学方程式:_______ 。
(2)写出指定试剂的名称:D_______ 。
(3)C的作用是_______ 。F的作用是_______ 。
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是_______ ,若反应产生0.5molCl2,则消耗的氧化剂的物质的量为_______ mol,反应转移的电子数是_______ 。

(1)写出实验室制备Cl2的化学方程式:
(2)写出指定试剂的名称:D
(3)C的作用是
(4)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中HCl的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如图变化关系:

(1)A的名称是___ ;D的化学式是___ 。
(2)B→D反应的化学方程式___ 。
(3)A与水反应的化学方程式___ 。

(1)A的名称是
(2)B→D反应的化学方程式
(3)A与水反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】NH3具有广泛的用途。实验室常用如图所示装置制取并收集NH3。______ 。
(2)干燥NH3应选用的干燥剂是______ 。
(3)图1中方框内收集NH3的装置可选用图2中的______ (填序号)。
(4)尾气处理装置中使用倒置漏斗的作用是______ 。

(2)干燥NH3应选用的干燥剂是
(3)图1中方框内收集NH3的装置可选用图2中的
(4)尾气处理装置中使用倒置漏斗的作用是
您最近一年使用:0次
【推荐3】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用如图装置制备氨气并探究相关性质。
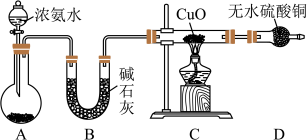
(1)装置A 中,盛有浓氨水的仪器名称为_____ 。装置B 的作用是_____ 。
(2)连接好装置并检验装置的气密性后,装入药品,然后应先_____ (填 I 或Ⅱ)。
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C 中 CuO 粉末变红,D 中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为_____ ,该反应证明氨气具有还原性;氨与氧气的在催化剂作用下的反应也体现了这一性质,该反应化学方程式为_____ 。
(4)该实验缺少尾气吸收装置,如图中能用来吸收尾气的装置是_____ (填装置序号)。

(5)实验室还可用如图所示装置制备氨气,化学反应方程式为_____ 。
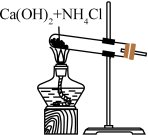
(6)现将 1.92gCu 投入到一定量的浓HNO3 中,Cu 完全溶解,生成气体颜色越来越浅,共收集到标准状况下 672mL 的NOX 混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的 O2 的体积为_____ 。

(1)装置A 中,盛有浓氨水的仪器名称为
(2)连接好装置并检验装置的气密性后,装入药品,然后应先
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(3)实验中观察到C 中 CuO 粉末变红,D 中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
(4)该实验缺少尾气吸收装置,如图中能用来吸收尾气的装置是

(5)实验室还可用如图所示装置制备氨气,化学反应方程式为

(6)现将 1.92gCu 投入到一定量的浓HNO3 中,Cu 完全溶解,生成气体颜色越来越浅,共收集到标准状况下 672mL 的NOX 混合气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入标准状况下的 O2 的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】同学们在实验室中进行了如图所示的实验。(夹持仪器已省略)

(1)具支试管中发生反应的化学方程式是_____ ,该反应中硝酸表现出的化学性质是____ 。
(2)实验中观察到具支试管内的现象是_______ ,溶液上方的气体略有红棕色,该红棕色气体是_______ ,产生的原因是_______ (用化学方程式表示)。
(3) 溶液的作用是
溶液的作用是_______ 。
(4)使实验停止的操作是_______ 。

(1)具支试管中发生反应的化学方程式是
(2)实验中观察到具支试管内的现象是
(3)
 溶液的作用是
溶液的作用是(4)使实验停止的操作是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】(Ⅰ)已知氯水有漂白性,是因为含有_________ (化学式),能与AgNO3反应生成_________ 色沉淀,是因为含有_______________ (名称)离子;
(Ⅱ)在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)实验室制取A的化学方程式__________
(2)反应①的化学方程式为___________ 。当有1molA参加反应时,转移______ mol电子。
(3)反应②的化学方程式为________________________ 。
(4)反应③的离子方程式为_____________________
(Ⅱ)在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)实验室制取A的化学方程式
(2)反应①的化学方程式为
(3)反应②的化学方程式为
(4)反应③的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】课外小组的同学利用下图装置研究铜与稀硝酸的反应。
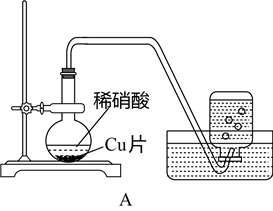
(1)铜与稀硝酸反应的离子方程式________________________________________ 。
(2)实验过程中水槽中的集气瓶收集到无色气体,甲同学由此认为铜与稀硝酸反应生成了NO。乙同学认为上述理由不完备,原因是________________________________________ (用化学方程式表示)。
(3)同学们经过讨论,决定改用装置B进行反应,实验步骤①~③如下图所示。

步骤③拔去注射器的橡胶帽,拉动活塞吸入少量的空气后,迅速盖上橡胶帽。如果观察到____________________ 的现象,就能证明铜与稀硝酸反应生成了NO。

(1)铜与稀硝酸反应的离子方程式
(2)实验过程中水槽中的集气瓶收集到无色气体,甲同学由此认为铜与稀硝酸反应生成了NO。乙同学认为上述理由不完备,原因是
(3)同学们经过讨论,决定改用装置B进行反应,实验步骤①~③如下图所示。

步骤③拔去注射器的橡胶帽,拉动活塞吸入少量的空气后,迅速盖上橡胶帽。如果观察到
您最近一年使用:0次
【推荐1】铁红(Fe2O3)是一种常见颜料,用废铁屑(主要含铁,还含有少量Fe2O3)制取铁红的工艺如下:
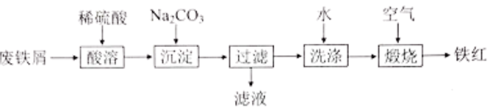
(1)写出废铁屑中的Fe2O3和稀硫酸反应的离子方程式:___________ 。
(2)“酸溶”一段时间后,溶液中检测不到Fe3+的原因是___________ 。
(3)“沉淀”所得固体为FeCO3,检验FeCO3“洗涤”是否完全的方法是___________ 。
(4)“煅烧”时FeCO3与O2反应的物质的量之比为___________ 。

(1)写出废铁屑中的Fe2O3和稀硫酸反应的离子方程式:
(2)“酸溶”一段时间后,溶液中检测不到Fe3+的原因是
(3)“沉淀”所得固体为FeCO3,检验FeCO3“洗涤”是否完全的方法是
(4)“煅烧”时FeCO3与O2反应的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】I.探究浓硫酸与木炭粉反应的产物,把生成物通过如图所示连接装置。

(1)发生装置中盛放浓硫酸和木碳粉的仪器名称分别是________ 、________ 。发生反应的化学方程式是________ ;其中体现浓硫酸的________ 性。
(2)A中的实验现象是________ ,说明产物中有________ 。
(3)B实验中观察到的现象是________ ;证明生成的气体具有________ 性。
(4)装置C的作用是________ ;装置D的作用是________ 。
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。

(5)设备1、2中发生反应的化学方程式分别是_________ 、________ 。
(6)设备2中通入的物质A是_________ 。

(1)发生装置中盛放浓硫酸和木碳粉的仪器名称分别是
(2)A中的实验现象是
(3)B实验中观察到的现象是
(4)装置C的作用是
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示。

(5)设备1、2中发生反应的化学方程式分别是
(6)设备2中通入的物质A是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】高铁酸钾( )是一种暗紫色固体,在低温碱性条件下比较稳定,微溶于KOH浓溶液。工业上湿法制备
)是一种暗紫色固体,在低温碱性条件下比较稳定,微溶于KOH浓溶液。工业上湿法制备 的流程如图:
的流程如图:
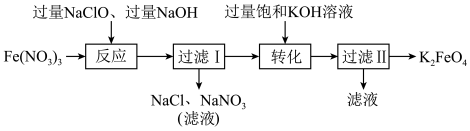
(1)基态Fe原子的价层电子的运动状态有_______ 种。
(2)请比较工业上湿法制备 的条件下
的条件下 和
和 的溶解度大小:
的溶解度大小:
_______ (填“>”、“<”或“=”) 。
。
(3)将 粗品[含有
粗品[含有 、NaCl等杂质]转化为
、NaCl等杂质]转化为 的实验方案为:
的实验方案为:
a.在不断搅拌下,将 粗品溶于冷的3
粗品溶于冷的3  KOH溶液中,快速过滤除去
KOH溶液中,快速过滤除去 等难溶的物质。
等难溶的物质。
b.将滤液置于_______ 中,向滤液中加入_______ ,过滤。
c.对产品进行洗涤时使用乙醇,其目的是_______ (答两点)。
(4)测定高铁酸钾样品的纯度:
①称取0.5000 g高铁酸钾样品,完全溶解于KOH浓溶液中,再加入足量亚铬酸钾{ }反应后配成100.00 mL溶液。
}反应后配成100.00 mL溶液。
②取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至 ,用0.1000
,用0.1000  的硫酸亚铁铵
的硫酸亚铁铵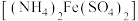 滴定,消耗标准硫酸亚铁铵溶液12.00 mL。
滴定,消耗标准硫酸亚铁铵溶液12.00 mL。
已知测定过程中发生如下反应: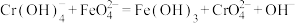 ,
,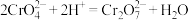 ,
, 。计算样品中
。计算样品中 的质量分数:
的质量分数:_______ 。
(5)高铁酸盐具有强氧化性,溶液pH越小氧化性越强,可用于除去废水中的氨、重金属等。 的浓度与pH关系如图1所示;用
的浓度与pH关系如图1所示;用 除去某氨氮(
除去某氨氮(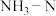 )废水,氨氮去除率与pH关系如图2所示;用
)废水,氨氮去除率与pH关系如图2所示;用 处理
处理 浓度为0.12
浓度为0.12  的含锌废水{
的含锌废水{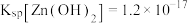 },锌残留量与pH关系如图3所示。[已知:
},锌残留量与pH关系如图3所示。[已知: 与
与 反应生成
反应生成 的过程中,可以捕集某些难溶金属的氢氧化物形成共沉淀]
的过程中,可以捕集某些难溶金属的氢氧化物形成共沉淀]

①图2中,pH越大氨氮的去除率越大,其原因可能是_______ 。
②图3中, 时锌的去除率比
时锌的去除率比 时大得多,其原因是
时大得多,其原因是_______ 。(从锌元素的存在形态角度说明)
 )是一种暗紫色固体,在低温碱性条件下比较稳定,微溶于KOH浓溶液。工业上湿法制备
)是一种暗紫色固体,在低温碱性条件下比较稳定,微溶于KOH浓溶液。工业上湿法制备 的流程如图:
的流程如图:
(1)基态Fe原子的价层电子的运动状态有
(2)请比较工业上湿法制备
 的条件下
的条件下 和
和 的溶解度大小:
的溶解度大小:
 。
。(3)将
 粗品[含有
粗品[含有 、NaCl等杂质]转化为
、NaCl等杂质]转化为 的实验方案为:
的实验方案为:a.在不断搅拌下,将
 粗品溶于冷的3
粗品溶于冷的3  KOH溶液中,快速过滤除去
KOH溶液中,快速过滤除去 等难溶的物质。
等难溶的物质。b.将滤液置于
c.对产品进行洗涤时使用乙醇,其目的是
(4)测定高铁酸钾样品的纯度:
①称取0.5000 g高铁酸钾样品,完全溶解于KOH浓溶液中,再加入足量亚铬酸钾{
 }反应后配成100.00 mL溶液。
}反应后配成100.00 mL溶液。②取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至
 ,用0.1000
,用0.1000  的硫酸亚铁铵
的硫酸亚铁铵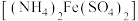 滴定,消耗标准硫酸亚铁铵溶液12.00 mL。
滴定,消耗标准硫酸亚铁铵溶液12.00 mL。已知测定过程中发生如下反应:
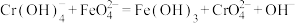 ,
,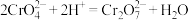 ,
, 。计算样品中
。计算样品中 的质量分数:
的质量分数:(5)高铁酸盐具有强氧化性,溶液pH越小氧化性越强,可用于除去废水中的氨、重金属等。
 的浓度与pH关系如图1所示;用
的浓度与pH关系如图1所示;用 除去某氨氮(
除去某氨氮(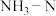 )废水,氨氮去除率与pH关系如图2所示;用
)废水,氨氮去除率与pH关系如图2所示;用 处理
处理 浓度为0.12
浓度为0.12  的含锌废水{
的含锌废水{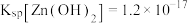 },锌残留量与pH关系如图3所示。[已知:
},锌残留量与pH关系如图3所示。[已知: 与
与 反应生成
反应生成 的过程中,可以捕集某些难溶金属的氢氧化物形成共沉淀]
的过程中,可以捕集某些难溶金属的氢氧化物形成共沉淀]
①图2中,pH越大氨氮的去除率越大,其原因可能是
②图3中,
 时锌的去除率比
时锌的去除率比 时大得多,其原因是
时大得多,其原因是
您最近一年使用:0次



