海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
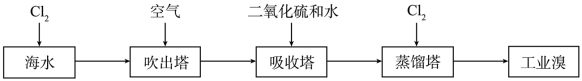
(1)溴元素在元素周期表中的位置为_______ 。
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:_______ 。
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______ 。
Ⅱ.海水提镁
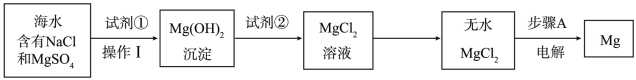
(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(5)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______ 。
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收Br2的离子反应方程式:
(3)蒸馏塔的蒸馏温度应控制在80-90°C最有利于生产,原因可能为:温度过高,
Ⅱ.海水提镁

(4)工业上常用于沉淀Mg2+的廉价试剂①的俗名是
(5)步骤A的化学方程式为
Ⅲ.海带提碘

(6)步骤B需搅拌、加热煮沸的目的是
更新时间:2022-07-10 17:45:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Al、Mg及其化合物在生产、生活中有着广泛的应用,请按要求回答下列问题。
I.用废铝渣制备Al(OH)3的流程如下图所示,假设反应①杂质不反应。
(1)Al在元素周期表中的位置为______ ,试剂X的名称______ 。
(2)溶液A显酸性的原因可能是(可用离子方程式表示) a.盐酸过量;b.____________ 。
II.用镁硅酸盐矿石制备高纯度Mg(OH)2的流程如下图所示:

已知:①溶液M中除含Mg2+、SO42-外,还含少量Fe3+、 Al3+、Fe2+等离子;
②Mg2+与氨水的反应为吸热反应。
(1)向溶液M中先加入的试剂是_______ ;产生的沉淀有_____ 。
(2)H2O2参与反应的离子方程式是____________________ 。
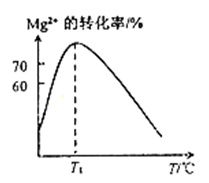
(2)溶液N中Mg2+的装化率随温度T的变化情况如图所示。T1之后,Mg,2+的转化率减小的原因是_________ 。
I.用废铝渣制备Al(OH)3的流程如下图所示,假设反应①杂质不反应。

(1)Al在元素周期表中的位置为
(2)溶液A显酸性的原因可能是(可用离子方程式表示) a.盐酸过量;b.
II.用镁硅酸盐矿石制备高纯度Mg(OH)2的流程如下图所示:

已知:①溶液M中除含Mg2+、SO42-外,还含少量Fe3+、 Al3+、Fe2+等离子;
②Mg2+与氨水的反应为吸热反应。
(1)向溶液M中先加入的试剂是
(2)H2O2参与反应的离子方程式是
(2)溶液N中Mg2+的装化率随温度T的变化情况如图所示。T1之后,Mg,2+的转化率减小的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】推断题。
(1)A、B、C、D、E分别是铁或铁的化合物。E常用作制油漆、涂料的颜料。其相互反应关系如图所示:
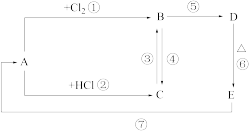
根据如图所示变化,按要求回答下列问题:
①写出D的化学式___________ ;
②向C的酸性溶液中加入 生成B的离子方程式:
生成B的离子方程式:___________ ;
③E→A的化学方程式:___________ ;
④C中加入 溶液,看到的现象是
溶液,看到的现象是___________ ;该过程中发生的氧化还原反应的化学方程式:___________ ;
(2)利用黄铜矿粉(主要成分为 )制取绿矾
)制取绿矾
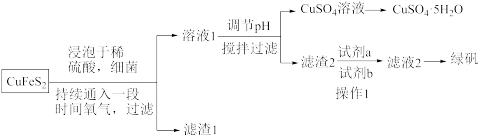
①有一种细菌在有氧气存在的稀硫酸中,可以将 氧化成硫酸盐,写出该反应的化学方程式:
氧化成硫酸盐,写出该反应的化学方程式:___________ 。
②若先加试剂a再加试剂b,则试剂a、b的化学式分别是___________ ;操作I需要用到的玻璃仪器名称是___________ 。
(1)A、B、C、D、E分别是铁或铁的化合物。E常用作制油漆、涂料的颜料。其相互反应关系如图所示:

根据如图所示变化,按要求回答下列问题:
①写出D的化学式
②向C的酸性溶液中加入
 生成B的离子方程式:
生成B的离子方程式:③E→A的化学方程式:
④C中加入
 溶液,看到的现象是
溶液,看到的现象是(2)利用黄铜矿粉(主要成分为
 )制取绿矾
)制取绿矾
①有一种细菌在有氧气存在的稀硫酸中,可以将
 氧化成硫酸盐,写出该反应的化学方程式:
氧化成硫酸盐,写出该反应的化学方程式:②若先加试剂a再加试剂b,则试剂a、b的化学式分别是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】分已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质.
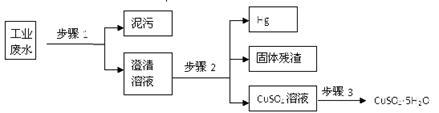
(1)步骤1的主要操作需用到的玻璃仪器除烧杯外有_____________ .
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)________________ ,固体残渣的成分是___________ (填化学式)
(3)步骤3中涉及的操作是:____________ 、____________ 、过滤、烘干。
(4)步骤2应该在通风橱中进行,原因是______________________

(1)步骤1的主要操作需用到的玻璃仪器除烧杯外有
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
(3)步骤3中涉及的操作是:
(4)步骤2应该在通风橱中进行,原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋中有丰富的资源,从中可以制取氯溴碘的单质及其化合物
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是___________________________ ,在空气中漂白粉长期存放会变质而失效的原理是(用化学方程式说明)________ 、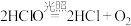 。
。
Ⅱ海水中溴元素以 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:

请回答下列问题。
(1)将海水浓缩的方法是________ 。
(2)步骤①反应的化学方程式是________________________________ 。
(3)步骤②通入热空气吹出 ,利用了
,利用了 的
的________ (填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。
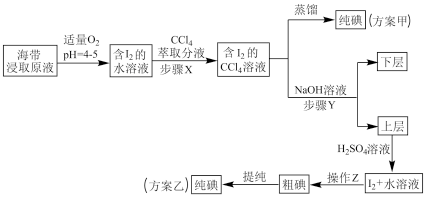
已知: 。
。
(1)步骤X中,萃取后分液漏斗内观察到的现象是__________________ 。
(2)下列有关步骤Y的说法中正确的是_______ (填字母)。
A.应控制 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
C.主要是除去海带浸取原液中的有机杂质 D. 溶液可以用乙醇代替
溶液可以用乙醇代替
(3)向上层清液中加入 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为_______________________ ,由于碘单质在水中的溶解度较小,且通过富集后得到的碘单质浓度较大,操作Z的名称为___________ 。
Ⅰ氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上利用氯气和石灰乳生产漂白粉的主要化学方程式是
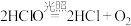 。
。Ⅱ海水中溴元素以
 形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图:
请回答下列问题。
(1)将海水浓缩的方法是
(2)步骤①反应的化学方程式是
(3)步骤②通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性 D.腐蚀性
Ⅲ碘及其化合物在科研、生活等方面有广泛用途。如图所示为从海带中制取碘的工艺流程。

已知:
 。
。(1)步骤X中,萃取后分液漏斗内观察到的现象是
(2)下列有关步骤Y的说法中正确的是
A.应控制
 溶液的浓度和体积 B.将碘单质转化成碘离子进入水层
溶液的浓度和体积 B.将碘单质转化成碘离子进入水层C.主要是除去海带浸取原液中的有机杂质 D.
 溶液可以用乙醇代替
溶液可以用乙醇代替(3)向上层清液中加入
 溶液,发生反应的化学方程式为
溶液,发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海水中化学资源的综合开发利用,已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,如图为提取它们的主要步骤:

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是________________ 。
(2)吸收塔中反应的离子方程式是___________ 。
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用______ (写化学式)。
(2)加入试剂②后反应的离子方程式是_______________ 。
(3)步骤①包括加热、蒸发、冷却、结晶、____________ 。
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是_______________ 。
Ⅲ.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸。生产方法是:
①将氯化镁晶体(MgCl2•6H2O)加热到523℃以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体。
②将两种气体冷却至室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸.
(1)MgCl2•6H2O在523℃以上分解的化学方程式是___________ 。
(2)现用1molMgCl2•6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水_______ g(精确到0.1),该盐酸中溶质的物质的量浓度是_________ mol/L(精确到0.1)。

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时第一次通入Cl2时发生反应的离子方程式是
(2)吸收塔中反应的离子方程式是
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
(2)加入试剂②后反应的离子方程式是
(3)步骤①包括加热、蒸发、冷却、结晶、
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
Ⅲ.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸。生产方法是:
①将氯化镁晶体(MgCl2•6H2O)加热到523℃以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体。
②将两种气体冷却至室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸.
(1)MgCl2•6H2O在523℃以上分解的化学方程式是
(2)现用1molMgCl2•6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】海水是巨大的化学资源宝库,利用海水可以提取很多物质。
利用1:提溴工业
用海水晒盐之后的盐卤可提取溴,提取流程如图:

(1)吹出塔中热空气能将溴单质吹出的原因是_____ 。蒸馏塔中通入水蒸气进行加热,需要控制温度在90℃左右的原因是______ 。
利用2:提镁工业
从海水提取食盐和Br2之后的盐卤中除含有Mg2+、C1-外,还含有少量Na+、Fe2+、Fe3+、SO42-和CO(NH2)2等,还可以用来提取MgCl2、MgO、Mg(OH)2等物质,流程如图所示:
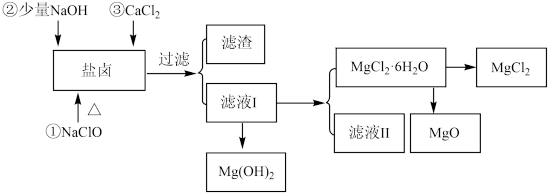
(2)用NaClO除去尿素CO(NH2)2时,生成物除盐外,还有能参与大气循环的无毒物质,则该反应的化学方程式为_______ ;加入NaClO的另一个作用是________ 。
利用3:淡化工业
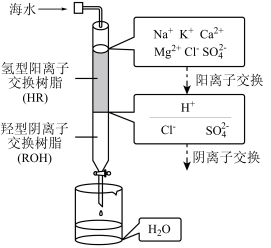
(3)海水淡化的方法主要有闪蒸法、离子交换法、电渗析法等。离子交换法淡化海水模拟过程如图所示。氢型阳离子交换原理可表示为:HR+Na+=NaR+H+;……。羟型阴离子交换树脂填充部分存在的反应有:ROH+C1-=RC1+OH-;______ ;________ 。
(4)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示:

①图中的海水没有直接通入到阴极室中,其原因是_________ 。
②淡化水在________ 室(填X、Y、Z、M或N)形成后流出。
利用1:提溴工业
用海水晒盐之后的盐卤可提取溴,提取流程如图:

(1)吹出塔中热空气能将溴单质吹出的原因是
利用2:提镁工业
从海水提取食盐和Br2之后的盐卤中除含有Mg2+、C1-外,还含有少量Na+、Fe2+、Fe3+、SO42-和CO(NH2)2等,还可以用来提取MgCl2、MgO、Mg(OH)2等物质,流程如图所示:

(2)用NaClO除去尿素CO(NH2)2时,生成物除盐外,还有能参与大气循环的无毒物质,则该反应的化学方程式为
利用3:淡化工业
(3)海水淡化的方法主要有闪蒸法、离子交换法、电渗析法等。离子交换法淡化海水模拟过程如图所示。氢型阳离子交换原理可表示为:HR+Na+=NaR+H+;……。羟型阴离子交换树脂填充部分存在的反应有:ROH+C1-=RC1+OH-;

(4)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示:

①图中的海水没有直接通入到阴极室中,其原因是
②淡化水在
您最近一年使用:0次
【推荐1】海带中含丰富的碘。为了从海带中提碘,某研究性学习小组设计并进行了以下实验:

(1)步骤⑤中,向含碘水溶液中加入苯,充分振荡静置后看到的现象是________
(2)有关上述实验方案说法正确的是_____
(3)步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_______ ,最后碘在_______ (填仪器名称)中得到。
(4)简述检验提取碘后的水溶液中是否还含有单质碘的方法_______ 。
(5)写出步骤④所发生的反应的离子方程式_______ 。

(1)步骤⑤中,向含碘水溶液中加入苯,充分振荡静置后看到的现象是________
| A.液体分为两层,上层紫色,下层无色 |
| B.液体不分层,呈浅棕色 |
| C.液体不分层,呈无色 |
| D.液体分为两层,上是无色,下层紫色 |
| A.步骤①的操作可以在烧瓶中进行 |
| B.步骤②可以适当加热以提升单位时间内的浸取率 |
| C.步骤③⑤的操作分别是过滤、萃取 |
| D.步骤⑤加入的有机溶剂可以更换为四氯化碳 |
(4)简述检验提取碘后的水溶液中是否还含有单质碘的方法
(5)写出步骤④所发生的反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以离子的形式存在。实验中从海藻提取碘的流程如图所示
(1)指出提取碘的过程中有关的实验操作③的名称______________ ;写出过程④中有关反应的离子方程式________________________________________________ 。
(2)提取碘的过程中可提供选择的有机试剂为_________ 。
A.酒精、四氯化碳 B.四氯化碳、苯 C.汽油、醋酸
(3)为使含碘的水溶液转化为碘的有机溶液,操作⑤所用的仪器有铁架台(带铁圈),烧杯和__________________ 。
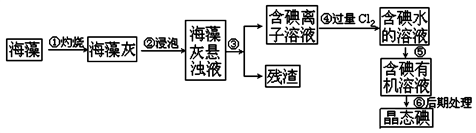
(1)指出提取碘的过程中有关的实验操作③的名称
(2)提取碘的过程中可提供选择的有机试剂为
A.酒精、四氯化碳 B.四氯化碳、苯 C.汽油、醋酸
(3)为使含碘的水溶液转化为碘的有机溶液,操作⑤所用的仪器有铁架台(带铁圈),烧杯和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】碘是人体必需的元素之一,海带中含有丰富的碘元素。灼烧海带获取的海带灰中,碘元素主要以I-形式存在。在实验室中,从海带灰中提取碘的流程如下:
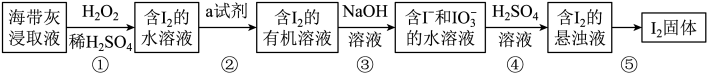
回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、_______ 等
(2)下列关于卤族元素单质储存的说法错误的是_______;(填字母)
(3)写出步骤①中发生反应的离子方程式:_______ ;
(4)步骤②中提取碘的过程中,可选择的有机试剂是_______;(填字母)
(5)下列有关萃取、分液的说法错误的是
(6)写出步骤③中发生反应的离子方程式:_______ ;在此反应中,每消耗3.81gI2转移_______ mol电子;
(7)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是_______ 。

回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、
(2)下列关于卤族元素单质储存的说法错误的是_______;(填字母)
| A.将氟气压缩成液氟储存在钢瓶中 |
| B.将氯气压缩成液氯储存在钢瓶中 |
| C.溴单质保存在棕色瓶中,不需要加水封存 |
| D.碘单质保存在棕色广口瓶中 |
(4)步骤②中提取碘的过程中,可选择的有机试剂是_______;(填字母)
| A.酒精 | B.醋酸 | C.四氯化碳 | D.苯 |
| A.萃取剂可以循环利用 |
| B.萃取振荡时,分液漏斗下口应倾斜向上 |
| C.分液时,应先从分液漏斗的下口放出下层液体,然后再从下口放出上层液体 |
| D.从下口放出下层液体前要先取下分液漏斗的塞子 |
(7)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】如图是人类从海水资源获取溴和镁的流程示意图:

回答下列问题::
(1)海水淡化的方法主要有________ (填一种)。
(2)下列物质不需要经过化学变化就能从海水中获得的物质是____________ (填序号)。
A.液溴 B.食盐 C.氢气 D.淡水
(3)操作A是_______ 和过滤(填实验基本操作名称)。
(4)操作B需加入下列试剂中的一种,最合适的是_______ (选填编号)。
a.氢氧化钠溶液 b.石灰乳 c.澄清石灰水 d.碳酸钠溶液
(5)向苦卤中通入Cl2,发生反应的离子方程式是_______ ,用SO2水溶液吸收Br,吸收率可达95%,有关反应的化学方程式为 _______ 。
(6)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式______ 。

回答下列问题::
(1)海水淡化的方法主要有
(2)下列物质不需要经过化学变化就能从海水中获得的物质是
A.液溴 B.食盐 C.氢气 D.淡水
(3)操作A是
(4)操作B需加入下列试剂中的一种,最合适的是
a.氢氧化钠溶液 b.石灰乳 c.澄清石灰水 d.碳酸钠溶液
(5)向苦卤中通入Cl2,发生反应的离子方程式是
(6)无水MgCl2在熔融状态下,通电后会产生Cl2和Mg,写出该反应的化学方程式
您最近一年使用:0次
【推荐2】目前,世界上生产的镁有60%来自海水,其生产流程图如下

(1)贝壳的主要化学成分为________________ (写化学式).
(2)写出反应②的离子方程式:_____________ .
(3)根据流程图可知,可循环利用的物质是________________ .
(4)Mg与CO2反应时,有白色粉末并有黑色固体生成.请写出Mg与CO2反应的化学方程式,并用单线桥标出电子转移的方向与数目.___________________ .
(5)Na比Mg和Al要活泼.将Na投入到Fe2(SO4)3溶液中会发生剧烈的化学反应,其离子方程式为__________________ .

(1)贝壳的主要化学成分为
(2)写出反应②的离子方程式:
(3)根据流程图可知,可循环利用的物质是
(4)Mg与CO2反应时,有白色粉末并有黑色固体生成.请写出Mg与CO2反应的化学方程式,并用单线桥标出电子转移的方向与数目.
(5)Na比Mg和Al要活泼.将Na投入到Fe2(SO4)3溶液中会发生剧烈的化学反应,其离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是某化工厂对海水资源综合利用的示意图:

Ⅰ.(1)写出N的化学式_____ 。
(2)写出反应②的化学方程式__________ 。
Ⅱ.粗盐中含有Ca2+、Mg2+、 等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为______ 。
A.②③④① B.③④②①
C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是______ 。
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是______ 。
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2 乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?______ (填“甲”或“乙),理由是______________ 。

Ⅰ.(1)写出N的化学式
(2)写出反应②的化学方程式
Ⅱ.粗盐中含有Ca2+、Mg2+、
 等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为
等杂质,精制时所用的试剂为:①盐酸 ②氯化钡溶液 ③氢氧化钠溶液 ④碳酸钠溶液,以上试剂添加的顺序可以为A.②③④① B.③④②①
C.④③②① D.③②④①
Ⅲ.提取粗盐后剩余的海水(母液)中,可用来提取Mg和Br2。
(1)若用来提取Mg,根据上述提取Mg的流程,没有涉及到的反应类型是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)若用来提取Br2,反应⑥所用的气态氧化剂的寻找货源的设想,其中合理的是
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
(3)母液用来提取Mg和Br2先后顺序,甲乙两位工程师有不同观点:
甲:母液先提取Mg,后提取Br2 乙:母液先提取Br2,后提取Mg
请你判断哪个更合适?
您最近一年使用:0次



