掺杂了硒(Se)、 碲(Te) 固溶物的Ag2S是一种具有良好塑性和热电性能的柔性半导体材料,该材料能用于可穿戴式、植入式电子设备的制备。
回答下列问题:
(1)Ag的核外电子排布式是[Kr] 4d105s1,则Ag在元素周期表中的位置是_______ 。下列属于基态Ag+的电子排布式的是_______ (填标号)。
A. [Kr] 4d95s2 B. [Kr] 4dl0 C. [Kr] 4d95s1
(2)S、As、Se、Br在元素周期表中的位置关系如图所示,则As、Se、Br的第一电离能由大到小的顺序为_______ , 的空间构型为
的空间构型为_______ 。
(3)金属Ge也是一种良好的半导体,利用离子液体[EMIM] [AlCl4]可电沉积还原金属Ge,该离子液体的熔点只有7℃,其中EMIM+结构如图所示。
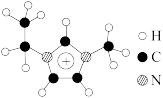
①EMIM+中C原子的杂化类型是_______ 。
②EMIM+中σ键数: π键数=_______ 。
③该离子液体的熔点比较低的原因是_______ 。
(4)ZnS的立方晶胞结构如下图所示:

①ZnS晶体中,与S2-距离最近且等距的Zn2+的个数是_______ 。
②ZnS的晶胞边长为a pm,则晶体的密度为_______ g·cm-3(用含a、NA的代数式表示,NA为阿伏加德罗常数的值)。
回答下列问题:
(1)Ag的核外电子排布式是[Kr] 4d105s1,则Ag在元素周期表中的位置是
A. [Kr] 4d95s2 B. [Kr] 4dl0 C. [Kr] 4d95s1
(2)S、As、Se、Br在元素周期表中的位置关系如图所示,则As、Se、Br的第一电离能由大到小的顺序为
 的空间构型为
的空间构型为| S | ||
| As | Se | Br |

①EMIM+中C原子的杂化类型是
②EMIM+中σ键数: π键数=
③该离子液体的熔点比较低的原因是
(4)ZnS的立方晶胞结构如下图所示:

①ZnS晶体中,与S2-距离最近且等距的Zn2+的个数是
②ZnS的晶胞边长为a pm,则晶体的密度为
更新时间:2022-07-13 12:34:53
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】某市售照明材料LED晶片是一种发光二极管。材质组成为:GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、GaInN(氮化镓铟)等。请回答下列问题:
(1)砷基态原子的核外电子排布式为______________________ 。
(2)上述非金属元素氢化物的沸点从高到低的顺序为___________ 。
(3)下列说法正确的是___________
a.电负性:As<Ga b.Sic与GaAs互为等电子体 c.第一电离能:As>Se>Ga
(4)如图所示为GaAs的晶胞结构,晶体熔点为1237℃。
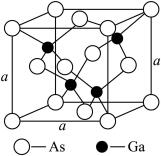
①晶胞中砷与镓原子间的化学键类型有___________ 。
②一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是___________ 。
③一个晶胞的组成为___________ 。
④已知晶胞棱长a=5.64×10-10m,相对原子质量Ga∶70,As∶75,则该晶胞密度为ρ=___________ 。
(1)砷基态原子的核外电子排布式为
(2)上述非金属元素氢化物的沸点从高到低的顺序为
(3)下列说法正确的是
a.电负性:As<Ga b.Sic与GaAs互为等电子体 c.第一电离能:As>Se>Ga
(4)如图所示为GaAs的晶胞结构,晶体熔点为1237℃。

①晶胞中砷与镓原子间的化学键类型有
②一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是
③一个晶胞的组成为
④已知晶胞棱长a=5.64×10-10m,相对原子质量Ga∶70,As∶75,则该晶胞密度为ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++
2CuCl+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为_______ ,H、N、O三种元素的电负性由大到小的顺序是_______ ;
(2)SO2分子的空间构型为_______ ;
(3)乙二胺分子中氮原子轨道的杂化类型为_______ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______ 。
(4)配离子[Cu(En)2]2+的配位数为_______ ;
(5)配离子[Cu(En)2]2+含有的微粒间的作用力类型有_______(填字母);
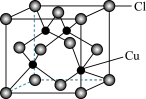
(6)CuCl的晶胞结构如图所示,其中Cl-的配位数(即与Cl- 最近距离的Cu+的个数)为_______ 。
2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++

2CuCl+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N—CH2—CH2—NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写):
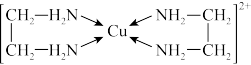
(1)配离子[Cu(En)2]2+的中心原子基态外围电子排布式为
(2)SO2分子的空间构型为
(3)乙二胺分子中氮原子轨道的杂化类型为
(4)配离子[Cu(En)2]2+的配位数为
(5)配离子[Cu(En)2]2+含有的微粒间的作用力类型有_______(填字母);
| A.配位键 | B.极性键 | C.离子键 | D.非极性键 | E.氢键 | F.金属键 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】磷的单质和化合物在科研与生产中有许多重要用途,铜及其合金是人类最早使用的金属材料。请回答下列问题:
(1)白磷是磷的一种单质,其分子结构如图所示,则一个分子中有____ 对成键电子对和____ 对孤电子对。
(2)N和P都有+5价,PCl5能形成离子型晶体,晶格中含有[PCl4]+和[PCl6]-,则[PCl4]+空间构型为______ 。
(3)电负性比较:P_____ S(填“>”“=”“<”);而P的第一电离能比S大的原因是______ 。
(4)铜及其合金是人类最早使用的金属材料,Cu2+能与NH3形成配位数为4的配合物[Cu(NH3)4]SO4。
①铜元素在周期表中的位置是__________ ,1mol[Cu(NH3)4]SO4 有___ mol配位键 ;②[Cu(NH3)4]SO4中,存在的化学键的类型有_____ (填标号)。
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)磷化镓(GaP)材料是研制微电子器件、光电子器件的新型半导体材料。GaP的晶体结构是闪锌矿型结构(如图所示),晶胞参数apm。
①与Ga紧邻的P个数为________ 。
②GaP晶体的密度为(列出计算式)______ g·cm-3(NA为阿伏伽德罗常数)。
(1)白磷是磷的一种单质,其分子结构如图所示,则一个分子中有

(2)N和P都有+5价,PCl5能形成离子型晶体,晶格中含有[PCl4]+和[PCl6]-,则[PCl4]+空间构型为
(3)电负性比较:P
(4)铜及其合金是人类最早使用的金属材料,Cu2+能与NH3形成配位数为4的配合物[Cu(NH3)4]SO4。
①铜元素在周期表中的位置是
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)磷化镓(GaP)材料是研制微电子器件、光电子器件的新型半导体材料。GaP的晶体结构是闪锌矿型结构(如图所示),晶胞参数apm。

①与Ga紧邻的P个数为
②GaP晶体的密度为(列出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铁在人类物质文明的发展进程中起到重要的作用。回答下列问题:
(1)人体血液中含有铁元素,其存在形式的基态电子排布式为_______ 。
(2)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在,其中Fe采取的杂化类型为_______ ,固态FeCl3的晶体类型为_______ 。
(3)Fe能与CO形成配合物Fe(CO)5。该配合物分子中有_______ 个σ键和_______ 个π键,所含三种元素原子的第一电离能从大到小的顺序为:_______ ,CH4的键角比H2O大的原因是:_______ 。
(4)Fe3+离子和K4[Fe(CN)6]反应生成蓝色沉淀,被称为普鲁士蓝,普鲁士蓝颜色很深,原因是_______ ,其晶体部分结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),Fe3+在晶体中的配位数是_______ ,已知图示立方体边长为a pm,则该晶体密度为_______ g·cm-3(写出表达式,用NA表示阿伏加德罗常数的值)。
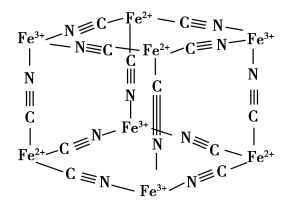
(1)人体血液中含有铁元素,其存在形式的基态电子排布式为
(2)FeCl3中的化学键具有明显的共价性,蒸气状态下以双聚分子存在,其中Fe采取的杂化类型为
(3)Fe能与CO形成配合物Fe(CO)5。该配合物分子中有
(4)Fe3+离子和K4[Fe(CN)6]反应生成蓝色沉淀,被称为普鲁士蓝,普鲁士蓝颜色很深,原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
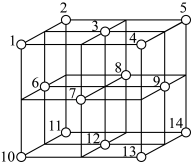
【推荐2】有A、B、C、D、E五种元素。其相关信息如表:
请回答下列问题:
(1)写出E元素原子基态时的电子排布式________ 。
(2)C元素的第一电离能比氧元素的第一电离能_______ (填“大”或“小”)。
(3)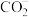 离子中C原子的杂化轨道类型是
离子中C原子的杂化轨道类型是_______ , 分子的空间构型是
分子的空间构型是_________ 。
(4)A、C、E三种元素可形成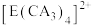 配离子,其中存在的化学键类型有
配离子,其中存在的化学键类型有________ (填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
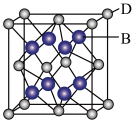
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为_______ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式
(2)C元素的第一电离能比氧元素的第一电离能
(3)
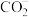 离子中C原子的杂化轨道类型是
离子中C原子的杂化轨道类型是 分子的空间构型是
分子的空间构型是(4)A、C、E三种元素可形成
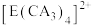 配离子,其中存在的化学键类型有
配离子,其中存在的化学键类型有①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为

您最近一年使用:0次
【推荐1】非金属和金属单质以及相关化合物有着广泛的应用,回答下列相关问题:
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是______ (填字母)。
a. 电子从基态跃迁到较高的激发态 b. 电子从较高的激发态跃迁到基态
c. 焰色反应的光谱属于吸收光谱 d. 焰色反应的光谱属于发射光谱
(2)In元素基态原子的价电子排布式为________ 。与Cu元素同周期,且基态原子有2个未成对电子的过渡元素是____ (填元素符号)。
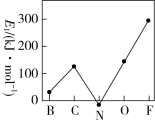
(3)第一电子亲和能(E1)是元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量。第二周期部分元素的E1变化趋势如图所示。试分析碳元素的E1较大的原因:______________ 。
(4)[PtCl4(NH3)2]中H-N-H键之间的夹角____ (填“>”“<”或“=”)NH3分子中H-N-H键之间的夹角,原因是________________ 。
(5)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4。1个Fe(CO)5分子中含有σ键数目为____ ;已知Ni(CO)4分子为正四面体构型,下列溶剂能够溶解Ni(CO)4的是____ (填字母)。
A. 四氯化碳 B.苯 C.水 D.液氨
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和由3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为____ 。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18 g·cm-3,则该晶胞参数a=_____ cm(写出计算表达式即可)。
(1)铜或铜盐的焰色反应为绿色,下列有关原理分析的叙述正确的是
a. 电子从基态跃迁到较高的激发态 b. 电子从较高的激发态跃迁到基态
c. 焰色反应的光谱属于吸收光谱 d. 焰色反应的光谱属于发射光谱
(2)In元素基态原子的价电子排布式为
(3)第一电子亲和能(E1)是元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量。第二周期部分元素的E1变化趋势如图所示。试分析碳元素的E1较大的原因:

(4)[PtCl4(NH3)2]中H-N-H键之间的夹角
(5)铁、镍易与CO作用形成羰基配合物Fe(CO)5、Ni(CO)4。1个Fe(CO)5分子中含有σ键数目为
A. 四氯化碳 B.苯 C.水 D.液氨
(6)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2-围成的正四面体空隙和由3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2-数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其化合物在生产、生活中应用广泛。回答下列问题:
(1)基态Fe原子核外电子排布式为___________ 。
(2) 可与
可与 形成配离子
形成配离子 ,
, 可与NO形成配离子
可与NO形成配离子 。
。
①S、N、O三种元素第一电离能由大到小的顺序为___________ 。
②每个 中含有σ键的数目是
中含有σ键的数目是___________ 。
(3) 的结构如图1所示。
的结构如图1所示。___________
②H2O中H-O-H键角___________ (填“>”“<”或“=”) 中O-S-O键角。
中O-S-O键角。
(4)由铁铜硫形成的某化合物的晶胞结构如图2所示。___________ 。
②若该晶体的密度为ρ g⋅cm ,则该晶胞的底面边长a=
,则该晶胞的底面边长a=___________ pm( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态Fe原子核外电子排布式为
(2)
 可与
可与 形成配离子
形成配离子 ,
, 可与NO形成配离子
可与NO形成配离子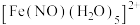 。
。①S、N、O三种元素第一电离能由大到小的顺序为
②每个
 中含有σ键的数目是
中含有σ键的数目是(3)
 的结构如图1所示。
的结构如图1所示。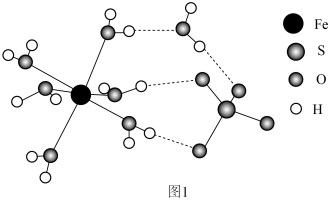
②H2O中H-O-H键角
 中O-S-O键角。
中O-S-O键角。(4)由铁铜硫形成的某化合物的晶胞结构如图2所示。
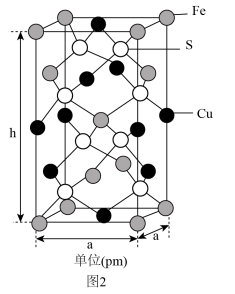
②若该晶体的密度为ρ g⋅cm
 ,则该晶胞的底面边长a=
,则该晶胞的底面边长a= 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Ni2+在氨性溶液中和镍试剂(丁二酮肟)反应生成鲜红色的螯合物沉淀,在定性分析中用于鉴定 。该反应可表示为
。该反应可表示为

(1)Ni在元素周期表中的位置是_______ ,其基态原子的未成对电子数是_______ 。
(2)与Ni同周期,基态原子最外层电子数为1的元素有________ (填元素符号)。其中原子序数最大的元素,其基态原子核外电子排布不符合________ (填选项字母)。
A.构造原理 B.泡利不相容原理 C.洪特规则
(3)已知丁二酮肟(物质A)通常情况下是白色粉末,熔点238~240℃,溶于乙醇、乙醚,几乎不溶于水。则丁二酮肟的晶体类型是________ 。
(4)丁二酮肟的组成元素电负性由大到小的顺序是________ 。
(5)物质B中含有的微粒间作用力类型有________ 。
A.离子键 B.共价键 C.氢键 D.配位键
(6)物质B中C原子的杂化方式是________ 。
(7)氧化镍(NiO)的晶体结构为立方晶系,其晶胞结构与氯化钠相似。氧化镍晶胞中,与一个Ni2+紧邻且距离相等的O2-以线段相连,构成的几何图形为________ 。
(8)某种氧化镍晶体中存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+取代,晶体仍显电中性。实验测得该氧化镍晶体的化学式为Ni0.90O,其晶胞参数为acm,NA代表阿伏加 德罗常数的值,则该晶体的密度为________ (用含a和NA的代数式表示)。
 。该反应可表示为
。该反应可表示为
(1)Ni在元素周期表中的位置是
(2)与Ni同周期,基态原子最外层电子数为1的元素有
A.构造原理 B.泡利不相容原理 C.洪特规则
(3)已知丁二酮肟(物质A)通常情况下是白色粉末,熔点238~240℃,溶于乙醇、乙醚,几乎不溶于水。则丁二酮肟的晶体类型是
(4)丁二酮肟的组成元素电负性由大到小的顺序是
(5)物质B中含有的微粒间作用力类型有
A.离子键 B.共价键 C.氢键 D.配位键
(6)物质B中C原子的杂化方式是
(7)氧化镍(NiO)的晶体结构为立方晶系,其晶胞结构与氯化钠相似。氧化镍晶胞中,与一个Ni2+紧邻且距离相等的O2-以线段相连,构成的几何图形为
(8)某种氧化镍晶体中存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+取代,晶体仍显电中性。实验测得该氧化镍晶体的化学式为Ni0.90O,其晶胞参数为acm,NA代表阿伏加 德罗常数的值,则该晶体的密度为
您最近一年使用:0次

 磷酸氧铜电池正极的活性物质是
磷酸氧铜电池正极的活性物质是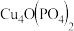 ,可通过下列反应制备:
,可通过下列反应制备: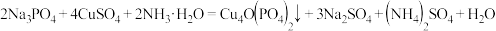
 、O、P元素的电负性由小到大的顺序是
、O、P元素的电负性由小到大的顺序是 原子的价电子排布式为
原子的价电子排布式为 中含有化学键的类型为
中含有化学键的类型为 空间结构名称为
空间结构名称为 ,结构式为
,结构式为 ,分子中
,分子中 键与
键与 键的个数之比为
键的个数之比为

