《石雅》云:“青金石色相如天,或复金屑散乱,光辉灿烂,若众星丽于天也”。青金石的化学组成可表示为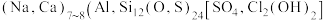 。回答下列问题:
。回答下列问题:
(1)硅在元素周期表中的位置是_______ ;铝离子的结构示意图为_______ 。
(2) 的电子式为
的电子式为_______ , 的结构式为
的结构式为_______ 。写出一种由青金石中非金属元素组成的既含有极性键又含有非极性键的物质的分子式_______ 。
(3)青金石所含的短周期元素中,金属性最强的是_______ ,非金属元素原子半径由大到小的顺序为_______ 。
(4)Be与Al的化学性质相似,则Be与NaOH溶液反应的化学方程式是_______ 。
(5)下列不能说明氯元素的非金属性比硫元素强的是_______(填字母)。
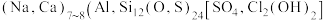 。回答下列问题:
。回答下列问题:(1)硅在元素周期表中的位置是
(2)
 的电子式为
的电子式为 的结构式为
的结构式为(3)青金石所含的短周期元素中,金属性最强的是
(4)Be与Al的化学性质相似,则Be与NaOH溶液反应的化学方程式是
(5)下列不能说明氯元素的非金属性比硫元素强的是_______(填字母)。
| A.氯、硫的最低负价分别为-1、-2 |
| B.硫化氢在300℃时开始分解,HCl在1500℃时开始缓慢分解 |
C. 的酸性比 的酸性比 的强 的强 |
D.向 水溶液中通入 水溶液中通入 有淡黄色沉淀生成 有淡黄色沉淀生成 |
更新时间:2022-07-16 08:24:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】以下是丁醇的四种同分异构体:
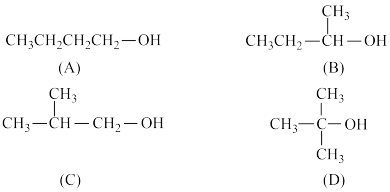
请根据乙醇在消去反应、催化氧化反应中变化的结构特点,回答以下问题(以下各问只需填写编号):
(1)在消去反应中能够得到两种消去产物的结构有_______________________________ 。
(2)只得到一种消去产物的结构是_____________________________________________ 。
(3)能被氧化为含相同碳原子数的醛的结构是____________________________ 。
(4)不能被灼热的CuO氧化的醇的结构是______________________________ 。

请根据乙醇在消去反应、催化氧化反应中变化的结构特点,回答以下问题(以下各问只需填写编号):
(1)在消去反应中能够得到两种消去产物的结构有
(2)只得到一种消去产物的结构是
(3)能被氧化为含相同碳原子数的醛的结构是
(4)不能被灼热的CuO氧化的醇的结构是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)得电子能力最强的原子是___________ ;
(2)化学性质最不活泼的单质是___________ ﹔
(3)F与Cl相比,原子半径较大的是___________ ;
(4) 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是___________ ﹔
(5)原子最外层电子数与最内层电子数相等的元素是___________ ﹔
(6)某阴离子的结构示意图为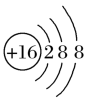 ,其离子符号是
,其离子符号是___________ ;
(7) 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是___________ ﹔
(8)第三周期元素中能与冷水剧烈反应的金属单质是___________ ,写出该反应的化学方程式:___________ ;
(9)碳的一种氢化物结构式为 ,其分子式是
,其分子式是___________ ,其中碳元素与氢元素的质量比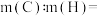
___________ ;(相对原子质量:C-12,H-1)
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填标号 )。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Mg | Al | S | Cl |
(1)得电子能力最强的原子是
(2)化学性质最不活泼的单质是
(3)F与Cl相比,原子半径较大的是
(4)
 与
与 相比,热稳定性较强的是
相比,热稳定性较强的是(5)原子最外层电子数与最内层电子数相等的元素是
(6)某阴离子的结构示意图为
 ,其离子符号是
,其离子符号是(7)
 与
与 中,能与
中,能与 溶液反应的是
溶液反应的是(8)第三周期元素中能与冷水剧烈反应的金属单质是
(9)碳的一种氢化物结构式为
 ,其分子式是
,其分子式是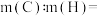
(10)下列各项性质的比较,符合相关性质递变规律的是___________(填
A.还原性: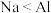 | B.非金属性: |
C.酸性: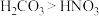 | D.碱性: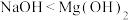 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】卤族元素包含F(氟)、Cl(氯)、Br(溴)和I(碘)等元素,卤族元素的单质及其化合物在生产生活中有着重要的应用,人们从自然界中获得卤族单质及基化合物的过程,体现了化学科学在利用自然资源创造新物质中的独特作用,根据所学知识及所给信息,回答下列问题:
(1)写出 的离子结构示意图
的离子结构示意图_______ 。
(2)氯元素存在 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有_______ 种。
(3)将氯气通入紫色石蕊溶液中,实验的现象是_______ ,结合离子方程式加上必要的文字解释原因_______ 。
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是 。干海带
。干海带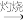 海带灰
海带灰 悬浊液
悬浊液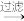 滤液
滤液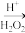 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有_______ 。
①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入 和
和 发生的离子方程式为
发生的离子方程式为_______ ;检验提取的碘水中含有 的试剂是
的试剂是_______ 。
(5)从海水晒盐后的盐卤(主要含 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:

从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是_______ 反应。工业上从盐卤中获取 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是_______ 。写出 与盐酸反应的离子方程式
与盐酸反应的离子方程式_______ 。
(1)写出
 的离子结构示意图
的离子结构示意图(2)氯元素存在
 、
、 两种核素,由这两种
两种核素,由这两种 、
、 核素构成的氯气单质有
核素构成的氯气单质有(3)将氯气通入紫色石蕊溶液中,实验的现象是
(4)从海带中提取碘单质的工艺流程如下,其中海带灰溶于水后碘的存在形成是
 。干海带
。干海带 海带灰
海带灰 悬浊液
悬浊液 滤液
滤液 碘水。工艺流程中不会用到的实验仪器有
碘水。工艺流程中不会用到的实验仪器有①酒精灯 ②三脚架 ③泥三角 ④分液漏斗 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒 ⑧量筒 ⑨漏斗
向“滤液”中加入
 和
和 发生的离子方程式为
发生的离子方程式为 的试剂是
的试剂是(5)从海水晒盐后的盐卤(主要含
 、
、 、
、 、
、 等)中模拟工业生产来提取镁,主要流程如图:
等)中模拟工业生产来提取镁,主要流程如图:
从流程提取镁的反应①~⑥中,没有涉及到的四种基本反应类型的是
 用石灰乳而不用NaOH溶液的原因是
用石灰乳而不用NaOH溶液的原因是 与盐酸反应的离子方程式
与盐酸反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1)NH3的电子式是___________ ;钡餐的化学式是___________ 。
(2)红热的碳与浓硫酸反应的化学方程式是___________ 。
(3)足量SO2通入品红溶液,可观察到的现象是___________ 。
(1)NH3的电子式是
(2)红热的碳与浓硫酸反应的化学方程式是
(3)足量SO2通入品红溶液,可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列关于氮族元素的问题:
(1)位于第五周期的元素符号和名称分别为_______ 、_______ 。铋(Bi)的最高正化合价为_______ 。
(2)①热稳定性:NH3_______ PH3(填“>”或“<”)。
②沸点:N2H4_______ P2H4(填“>”或“<”),判断依据是_______ 。
③化合物NH2NH2的电子式为_______ ,其分子内存在的共价键类型有_______
④磷能呈现多种化合价,其中+3价氧化物为10原子分子,该氧化物的分子式为_______ ,+5价简单含氧酸的分子式为_______ 。
(3)PH3与卤化氢的反应和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是_______ (填序号)。
a.能与NaOH反应 b.含离子键、共价键 c.受热可分解
(1)位于第五周期的元素符号和名称分别为
(2)①热稳定性:NH3
②沸点:N2H4
③化合物NH2NH2的电子式为
④磷能呈现多种化合价,其中+3价氧化物为10原子分子,该氧化物的分子式为
(3)PH3与卤化氢的反应和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.能与NaOH反应 b.含离子键、共价键 c.受热可分解
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】双氧水(过氧化氢的水溶液)在工业生产和日常生活中应用广泛。
(1)双氧水的强氧化性使其对大多数病菌和病毒具有消杀功能。用3%医用双氧水对不传染病房喷洒消毒时,地板上有气泡冒出,该气体是__ 。
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。知0.4mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为__ 。
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为__ ,写出该反应的离子方程式__ 。
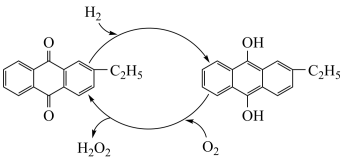
(4)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式___ 。
(5)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式是__ 。
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为__ mol。
(1)双氧水的强氧化性使其对大多数病菌和病毒具有消杀功能。用3%医用双氧水对不传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢。知0.4mol液态肼与足量的液态过氧化氢反应,生成氮气和水蒸气,并放出256.652kJ的热量。该反应的热化学方程式为
(3)双氧水能将碱性废水中的CN-转化成碳酸盐和一种对环境无污染的气体,CN-的电子式为
(4)如图是工业上制备过氧化氢最常见的方法,写出实际发生反应的总方程式

(5)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。

①Ir—Ru惰性电极吸附O2生成H2O2,其电极反应式是
②处理废氨水中溶质(以NH3计)的质量是34g,理论上电路中转移电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业的关键原料之一,可由氨气和氟气反应得到:_______NH3+_______F2→_______NF3+_______NH4F。完成下列填空:
(1)配平上述反应方程式_______ 。
(2)F原子的结构示意图是_______ ,从原子结构角度比较F和N元素的非金属性强弱_______ 。
(3)写出NH4F的电子式_______ ,溶液中NH 的检验方法是
的检验方法是_______ 。
(4)与NH 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是_______ ,该产物的水溶液呈_______ 性,用适当的化学用语解释该溶液酸碱性的原因:_______ 。其稀溶液中存在关系式:c(OH-)-c(H+) =c(HCO ) +
) + _______
(1)配平上述反应方程式
(2)F原子的结构示意图是
(3)写出NH4F的电子式
 的检验方法是
的检验方法是(4)与NH
 具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是
具有相同质子数和电子数的单核微粒,其单质在空气中长期露置后的最终产物是 ) +
) +
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素是组成我们生活的世界中一切物质的“原材料”。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是___________ 。
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:
(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:
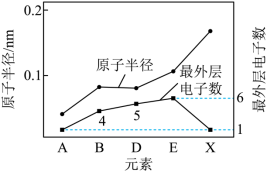
①E在周期表中的位置是___________ 。
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是___________ 。
③用电子式表示化合物XZ的形成过程是:___________ 。
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为___________ 。
⑤下列可以判断X和Y元素原子失电子能力强弱的是___________ (填字母序号)。
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:___________ 。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:

(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:

①E在周期表中的位置是
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是
③用电子式表示化合物XZ的形成过程是:
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为
⑤下列可以判断X和Y元素原子失电子能力强弱的是
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ 。
(2)氨气分子的结构式为_______ ,N2的电子式为_______ 。
(3)CN-中N元素显-3价,说明非金属性N_______ C(填“>”或“<”),请写出一个能比较N和C非金属性强弱的化学事实:_______ 。
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是_______ (用电离方程式解释),常见氮肥种类有_______ (列举两个)。
(1)氮元素在周期表中的位置是
(2)氨气分子的结构式为
(3)CN-中N元素显-3价,说明非金属性N
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)四种元素的原子半径如下表:
由此可推理:决定原子半径大小的因素有_______
(2) 和
和 都是化工生产中的重要物质。
都是化工生产中的重要物质。
① 的沸点(-33.5℃)高于
的沸点(-33.5℃)高于 的沸点(-129℃)的主要原因是
的沸点(-129℃)的主要原因是_______
② 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: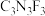 ),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式_______ 。
(1)四种元素的原子半径如下表:
| 元素符号 | Li | Be | Na | S | Cl |
| 原子半径/pm | 152 | 89 | 186 | 102 | 99 |
由此可推理:决定原子半径大小的因素有
(2)
 和
和 都是化工生产中的重要物质。
都是化工生产中的重要物质。①
 的沸点(-33.5℃)高于
的沸点(-33.5℃)高于 的沸点(-129℃)的主要原因是
的沸点(-129℃)的主要原因是②
 的一种下游产品三聚氟氰(分子式为:
的一种下游产品三聚氟氰(分子式为: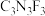 ),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
),分子结构中显示有环状结构,请从价键理论和物质的相对稳定性角度写出三聚氟氰的结构式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A,C同周期,B,C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________ 、B:________ 、C:________ 、D:________ 、E:________ 。
(2)用电子式表示离子化合物A2B的形成过程:______________________ 。
(3)写出下列物质的电子式:
①D元素形成的单质:_______________________________________________ 。
②E与B形成的化合物:_____________________________________________ 。
③A,B,E形成的化合物:___________________________________________ 。
④D与E形成的化合物:______________________________________________ 。
⑤C,D,E形成的离子化合物:________________________________________ 。
(1)写出五种元素的元素符号:A:
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出下列物质的电子式:
①D元素形成的单质:
②E与B形成的化合物:
③A,B,E形成的化合物:
④D与E形成的化合物:
⑤C,D,E形成的离子化合物:
您最近一年使用:0次



