含氯消毒剂和过氧化物消毒剂均可有效灭杀新冠病毒。
Ⅰ.二氧化氯(ClO2) 是目前国际上公认的第四代高效、无毒的广谱消毒剂。制备ClO2常见的方法有:
方法 1: 2NaClO3+2NaCl+2H2SO4 = 2ClO2↑+Cl2↑+2Na2SO4+2H2O
方法2:在酸性条件下,由NaClO3和双氧水反应制备ClO2。
(1)ClO2中氯元素的化合价是_______ ,H2O2的电子式是_______ 。
(2)方法1的反应中,氧化产物与还原产物的物质的量之比是_______ 。
(3)方法2发生反应的离子方程式是_______ 。
(4)和方法2比较,方法1的不足之处是_______ ( 写出一点即可)。
Ⅱ.过碳酸钠(2Na2CO3·3H2O2),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:2Na2CO3 (aq) +3H2O2 (aq) = 2Na2CO3·3H2O2 (aq) ΔH<0。
(5)已知过氧化氢受热易分解,则碳酸钠与过氧化氢的物质的量之比应_______ (填“>”、“<”或“=”)2: 3,且加入Na2CO3溶液速度不能过快,原因是 _______ 。
Ⅰ.二氧化氯(ClO2) 是目前国际上公认的第四代高效、无毒的广谱消毒剂。制备ClO2常见的方法有:
方法 1: 2NaClO3+2NaCl+2H2SO4 = 2ClO2↑+Cl2↑+2Na2SO4+2H2O
方法2:在酸性条件下,由NaClO3和双氧水反应制备ClO2。
(1)ClO2中氯元素的化合价是
(2)方法1的反应中,氧化产物与还原产物的物质的量之比是
(3)方法2发生反应的离子方程式是
(4)和方法2比较,方法1的不足之处是
Ⅱ.过碳酸钠(2Na2CO3·3H2O2),俗名固态双氧水,具有去污杀菌等功效。其制备原理为:2Na2CO3 (aq) +3H2O2 (aq) = 2Na2CO3·3H2O2 (aq) ΔH<0。
(5)已知过氧化氢受热易分解,则碳酸钠与过氧化氢的物质的量之比应
更新时间:2022-07-27 18:00:04
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】完成下列问题。
(1)在元素周期表中位于对角线的元素性质有相似性,如锂和镁。下列关于金属锂的说法不正确的是____ 。
A.金属锂是最轻的金属 B.锂可以和冷水反应放出氢气
C.碳酸锂易溶于水 D.氢氧化钠碱性强于氢氧化锂
(2)下列有关碱金属的说法中,正确的是_______ 。
A.金属锂应保存在煤油中
B.随着核电荷数增加,阳离子的氧化性逐渐减弱
C.它们都能在空气里燃烧生成M2O(M表示碱金属)
D.碱金属单质熔沸点随核电荷数的增大而升高
(3)金属锂是一种重要的储氢材料,吸氢和放氢反应原理如下:
吸氢反应:2Li+H2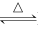 2LiH 放氢反应:LiH+H2O=LiOH+H2↑
2LiH 放氢反应:LiH+H2O=LiOH+H2↑
①放氢反应中的氧化剂是__________ 。
②已知LiH固体密度为0.8g/cm3。用锂吸收112L (标准状况)H2,生成的LiH体积与被吸收的H2体积比为_____ 。由②生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为______ mol。
(1)在元素周期表中位于对角线的元素性质有相似性,如锂和镁。下列关于金属锂的说法不正确的是
A.金属锂是最轻的金属 B.锂可以和冷水反应放出氢气
C.碳酸锂易溶于水 D.氢氧化钠碱性强于氢氧化锂
(2)下列有关碱金属的说法中,正确的是
A.金属锂应保存在煤油中
B.随着核电荷数增加,阳离子的氧化性逐渐减弱
C.它们都能在空气里燃烧生成M2O(M表示碱金属)
D.碱金属单质熔沸点随核电荷数的增大而升高
(3)金属锂是一种重要的储氢材料,吸氢和放氢反应原理如下:
吸氢反应:2Li+H2
 2LiH 放氢反应:LiH+H2O=LiOH+H2↑
2LiH 放氢反应:LiH+H2O=LiOH+H2↑①放氢反应中的氧化剂是
②已知LiH固体密度为0.8g/cm3。用锂吸收112L (标准状况)H2,生成的LiH体积与被吸收的H2体积比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2+2NO↑ + 4H2O。
①反应中还原剂是_______ (填化学式,下同); 被还原的元素是_______ ;氧化产物是_______ 。
②若有 96克 Cu 参与反应时,则生成的NO质量为_______ g。
(2)配平下列方程式,并在所给方程式上用单线桥法标出电子转移的方向和数目_____ 。
_______Al+_______NaNO3+_______NaOH=_______NaAlO2+_______N2↑+_______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 →O2。
①该反应中的氧化剂是_______ 。
②写出该反应的化学方程式_______ 。
(1)已知实验室制备NO的反应为:3Cu + 8HNO3=3Cu(NO3)2+2NO↑ + 4H2O。
①反应中还原剂是
②若有 96克 Cu 参与反应时,则生成的NO质量为
(2)配平下列方程式,并在所给方程式上用单线桥法标出电子转移的方向和数目
_______Al+_______NaNO3+_______NaOH=_______NaAlO2+_______N2↑+_______H2O
(3)某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2 →O2。
①该反应中的氧化剂是
②写出该反应的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】按要求完成。
(1)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为 ,该反应所属基本反应类型是
,该反应所属基本反应类型是___________ ,在反应中铁元素的化合价___________ (填“升高”或“降低”),该元素的原子___________ (填“失去”或“得到”)电子。发生氧化反应的是___________ (填化学式,下同),发生还原反应的是___________ 。
(2)用单线桥表示 的电子转移情况
的电子转移情况___________ 。
(3)在反应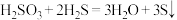 中,被氧化与被还原元素的质量比为
中,被氧化与被还原元素的质量比为___________ ,在反应 中,被还原的硫与被氧化的硫的质量比为
中,被还原的硫与被氧化的硫的质量比为___________ 。
(1)野外焊接铁轨常常采用铝热反应。已知铝热反应的化学方程式为
 ,该反应所属基本反应类型是
,该反应所属基本反应类型是(2)用单线桥表示
 的电子转移情况
的电子转移情况(3)在反应
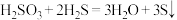 中,被氧化与被还原元素的质量比为
中,被氧化与被还原元素的质量比为 中,被还原的硫与被氧化的硫的质量比为
中,被还原的硫与被氧化的硫的质量比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】以下有十种物质:①氨水 ②稀硫酸 ③氯化氢 ④NaHSO4⑤蔗糖 ⑥二氧化碳 ⑦石墨 ⑧熔融氯化钠 ⑨氢氧化钠 ⑩碳酸钙,请回答下列问题:
(1)属于混合物的是___ ;属于电解质,但熔融状态下不导电的是___ ;属于电解质,且难溶于水的是___ ;属于化合物,但不是电解质的是___ ;不是电解质,但可以导电的是___ ;
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为___ 、_____ 、___ ;
(3)⑦和SiO2在高温下可发生如下反应:3C+SiO2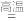 SiC+2CO↑(已知SiC中Si元素为+4价),上述反应中还原产物是
SiC+2CO↑(已知SiC中Si元素为+4价),上述反应中还原产物是___ ;氧化剂与还原剂物质的量之比为___ ;当有1.12L(标准状况下)CO气体产生时,反应过程中转移的电子数是__ 个。
(1)属于混合物的是
(2)上述物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为
(3)⑦和SiO2在高温下可发生如下反应:3C+SiO2
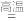 SiC+2CO↑(已知SiC中Si元素为+4价),上述反应中还原产物是
SiC+2CO↑(已知SiC中Si元素为+4价),上述反应中还原产物是
您最近一年使用:0次
【推荐2】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾强,其本身在反应中被还原为Fe3+。已知制取高铁酸钠的化学方程式为:2Fe(NO3)3 + 16NaOH + 3Cl2 = 2Na2FeO4+6NaNO3+ 6NaCl + 8H2O,回答下列问题:
(1)该反应中__________ 得到电子,表现_________ (填“氧化性”或“还原性” ),Na2FeO4为______________ (填“氧化剂”、“还原剂”、“氧化产物”或 “还原产物” )。
(2)若有1 mol Cl2参加反应,则反应中转移电子的物质的量为______________ 。
(1)该反应中
(2)若有1 mol Cl2参加反应,则反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】三氟化氯(ClF3)可用作氟化剂、燃烧剂、推进剂中的氧化剂、高温金属的切割油等。回答下列问题:
(1)ClF3中Cl的化合价为___ 。
(2)ClF3可由Cl2和F2在200~300℃、铜反应器中制得,反应的化学方程式为Cl2+3F2 2ClF3。ClF3能将NH3氧化生成N2,同时产生Cl2和一种能雕刻玻璃的物质。写出该反应的化学方程式:
2ClF3。ClF3能将NH3氧化生成N2,同时产生Cl2和一种能雕刻玻璃的物质。写出该反应的化学方程式:___ ,该反应中氧化剂与还原剂的物质的量之比为___ 。
(3)工业上可用Cl2与石灰乳反应制备漂白粉。相关反应方程式为___ ,其有效成分的名称是___ 。
(1)ClF3中Cl的化合价为
(2)ClF3可由Cl2和F2在200~300℃、铜反应器中制得,反应的化学方程式为Cl2+3F2
 2ClF3。ClF3能将NH3氧化生成N2,同时产生Cl2和一种能雕刻玻璃的物质。写出该反应的化学方程式:
2ClF3。ClF3能将NH3氧化生成N2,同时产生Cl2和一种能雕刻玻璃的物质。写出该反应的化学方程式:(3)工业上可用Cl2与石灰乳反应制备漂白粉。相关反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】配平氧化还原反应方程式
(1)_____Na + _____H2O=_____NaOH +____ H2___________
(2)_____FeCl3+_____SO2+______H2O=___FeCl2+____H2SO4+____HCl___________
(1)_____Na + _____H2O=_____NaOH +____ H2
(2)_____FeCl3+_____SO2+______H2O=___FeCl2+____H2SO4+____HCl
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】根据信息完成下列各空:
(1)氢化钠(NaH)是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。
①氢化钠的电子式为___________ 。
②氢化钠与水反应的化学方程式为___________ ,反应的氧化剂为___________ 。该反应过 程中,被破坏的化学键有___________ (填数字序号,下同),形成的化学键有___________ 。
①离子键 ②极性共价键 ③非极性共价键
(2)MnO2可经过如图所示的转化制取 MnCO3,已知“反应Ⅱ”为复分解反应。
①写出“反应Ⅰ”的化学方程式:___________ 。

②写出“反应Ⅱ”的离子方程式:___________ 。
(1)氢化钠(NaH)是一种离子化合物,遇水后放出氢气并生成一种碱,主要应用在有机合成和储氢材料方面。
①氢化钠的电子式为
②氢化钠与水反应的化学方程式为
①离子键 ②极性共价键 ③非极性共价键
(2)MnO2可经过如图所示的转化制取 MnCO3,已知“反应Ⅱ”为复分解反应。
①写出“反应Ⅰ”的化学方程式:

②写出“反应Ⅱ”的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C可解毒。下列叙述不正确的是__ (填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是__ (填序号)。
A.加入稀盐酸,观察是否有气泡产生
B.加入AgNO3,观察是否有沉淀产生
C.在酸性条件下加入KI-淀粉溶液,观察溶液颜色(I2遇淀粉呈蓝色)
(3)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出反应的离子方程式:__ 。
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C可解毒。下列叙述不正确的是
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.加入稀盐酸,观察是否有气泡产生
B.加入AgNO3,观察是否有沉淀产生
C.在酸性条件下加入KI-淀粉溶液,观察溶液颜色(I2遇淀粉呈蓝色)
(3)某同学把氯气通入到NaNO2溶液中,生成NaNO3和HCl,请写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)下列微粒中,既有氧化性又有还原性的是_____________________ (填字母)。
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中_______ 是还原剂(填“维生素C”或“Fe3+”)。
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成___________ 色,最后变成_________ 色。
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理_____________________________ (用离子方程式表示)。
(1)下列微粒中,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中
(3)向FeSO4溶液中滴加NaOH溶液时的现象是:生成的白色絮状沉淀迅速变成
(4)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”将铜箔腐蚀,反应原理
您最近一年使用:0次

 )十斤,装载入一泥罐内,用煤炭垫盛,发火煅红,罐中炉甘石熔化成团,冷定毁罐取出,即倭铅也。该过程主反应高温为:
)十斤,装载入一泥罐内,用煤炭垫盛,发火煅红,罐中炉甘石熔化成团,冷定毁罐取出,即倭铅也。该过程主反应高温为: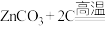
 快速制备氯气,其中氧化剂和还原剂的比是
快速制备氯气,其中氧化剂和还原剂的比是

