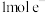是一种优质含氯消毒剂,酸性条件下能将
是一种优质含氯消毒剂,酸性条件下能将 转化为
转化为 。现向
。现向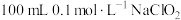 溶液中滴加过量KI溶液,并用硫酸酸化。测得反应后有0.02mol
溶液中滴加过量KI溶液,并用硫酸酸化。测得反应后有0.02mol 生成,则溶液中
生成,则溶液中 将完全转化为
将完全转化为 A. | B. | C. | D. |
21-22高一上·江苏南通·期末 查看更多[4]
江苏省如皋中学2021-2022学年高一上学期期末教学考试化学试题江苏省如皋中学2022-2023学年高一8月综合测试化学试题(已下线)考点05 氧化还原反应方程式的配平与计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型04 氧化还原反应方程式的配平及其计算-学易金卷:备战2023-2024学年高一化学期末真题分类汇编(江苏专用)
更新时间:2022-04-11 10:43:40
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列关于氧化还原反应认识正确的是
| A.氧化剂只具有氧化性 |
| B.还原剂只具有还原性 |
| C.金属单质在化学反应中只能做还原剂 |
| D.还原剂具有还原性,在反应中被氧化,得到还原产物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】Fe2+与酸性K2Cr2O7溶液发生:6Fe2+ + Cr2O + 14H+ =6Fe3+ + 2Cr3+ +7H2O。下列说法正确的是
+ 14H+ =6Fe3+ + 2Cr3+ +7H2O。下列说法正确的是
 + 14H+ =6Fe3+ + 2Cr3+ +7H2O。下列说法正确的是
+ 14H+ =6Fe3+ + 2Cr3+ +7H2O。下列说法正确的是| A.Fe2+被氧化 |
| B.H+是还原剂 |
| C.K2Cr2O7中铬化合价是+5 |
| D.生成1 mol Cr3+时,转移电子数约6×6.02×1023 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:2Fe3++3ClO-+10OH-=2 +3Cl-+5H2O,关于该反应说法错误的是
+3Cl-+5H2O,关于该反应说法错误的是
 +3Cl-+5H2O,关于该反应说法错误的是
+3Cl-+5H2O,关于该反应说法错误的是| A.ClO-中氯元素显+1价 | B.Fe3+被氧化 |
| C.ClO-被还原 | D. 是还原产物 是还原产物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知 与盐酸反应的化学方程式:
与盐酸反应的化学方程式: 。下列说法正确的是
。下列说法正确的是
 与盐酸反应的化学方程式:
与盐酸反应的化学方程式: 。下列说法正确的是
。下列说法正确的是| A.NaCl是还原产物 |
B. 被还原,发生氧化反应 被还原,发生氧化反应 |
| C.还原剂与氧化剂的物质的量比为6∶1 |
D.该反应生成6.72L(标准状况)的 ,转移电子0.5mol ,转移电子0.5mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】多硫化钠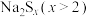 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl,反应中
,而NaClO被还原为NaCl,反应中 与NaClO的物质的量之比为1∶10,则x值为
与NaClO的物质的量之比为1∶10,则x值为
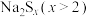 在碱性溶液中可被NaClO氧化为
在碱性溶液中可被NaClO氧化为 ,而NaClO被还原为NaCl,反应中
,而NaClO被还原为NaCl,反应中 与NaClO的物质的量之比为1∶10,则x值为
与NaClO的物质的量之比为1∶10,则x值为| A.6 | B.5 | C.4 | D.3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】与不同密度硝酸溶液反应时,还原产物百分比与硝酸密度的关系如图所示,下列说法错误的是
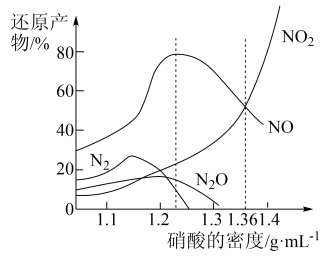

| A.其他条件相同,铁与足量密度为1.23g/mL的硝酸反应,还原产物主要为NO |
B.足量铁与一定量密度为1.36g/mL的硝酸反应,反应的化学方程式始终为: |
C.一定量的铁粉与足量密度为1.36g/mL的 反应,得到气体2.24L(标准状况),则参加反应的硝酸的物质的量为0.3mol 反应,得到气体2.24L(标准状况),则参加反应的硝酸的物质的量为0.3mol |
| D.硝酸的密度越大,其还原产物中高价态的成分所占比例越多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】黄铜矿(CuFeS2)是炼铜的最主要矿物,火法冶炼黄铜矿的过程中,其中一步反应是2Cu2O+Cu2S 6Cu+SO2↑,Cu2O晶胞如图所示。下列说法错误的是
6Cu+SO2↑,Cu2O晶胞如图所示。下列说法错误的是

 6Cu+SO2↑,Cu2O晶胞如图所示。下列说法错误的是
6Cu+SO2↑,Cu2O晶胞如图所示。下列说法错误的是
| A.氧化剂为Cu2O和Cu2S,氧化产物为Cu |
| B.该晶胞中白球代表铜原子、黑球代表氧原子 |
| C.每生成0.5molSO2,转移3mol的电子 |
| D.还原产物与氧化产物的物质的量之比为6∶1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】设NA代表阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,1.8g H2O中含有的电子数为NA |
| B.标准状况下,11.2L NO与11.2L O2混合后的分子数为NA |
| C.常温常压下,22.4L乙烯中含有的碳碳双键数为NA |
| D.5.6g Fe与足量Cl2完全反应转移的电子数为0.2NA |
您最近一年使用:0次

 SiC+2CO↑,有关叙述正确的是(
SiC+2CO↑,有关叙述正确的是( 是氧化剂,C是还原剂
是氧化剂,C是还原剂
 会增大
会增大 不能被F的稀溶液溶解,但可与F浓溶液加热反应生成G,同时生成D
不能被F的稀溶液溶解,但可与F浓溶液加热反应生成G,同时生成D 是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得
是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得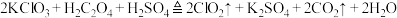 。据此,下列说法不正确的
。据此,下列说法不正确的 发生氧化反应
发生氧化反应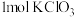 参加反应转移
参加反应转移