回答下列问题
(1)白磷与氧可发生如下反应: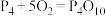 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O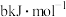 、P=O
、P=O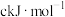 、O=O
、O=O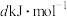 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为_______ 。
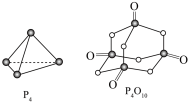
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为_______ 。
(3)氮氧化物能破坏臭氧层: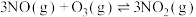

_______ 。
已知:反应Ⅰ: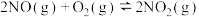
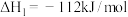
反应Ⅱ: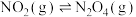
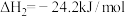
反应Ⅲ: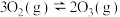
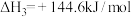
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①

②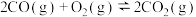

③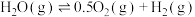

则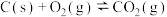

_______ ( 、
、 、
、 表示)。
表示)。
(1)白磷与氧可发生如下反应:
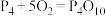 ,已知断裂下列化学键需要吸收的能量分别为:P—P
,已知断裂下列化学键需要吸收的能量分别为:P—P 、P—O
、P—O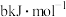 、P=O
、P=O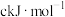 、O=O
、O=O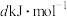 根据图示的分子结构和有关数据计算该反应的反应热为
根据图示的分子结构和有关数据计算该反应的反应热为
(2)写出下列热化学方程式,在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫燃烧热的热化学方程式为
(3)氮氧化物能破坏臭氧层:
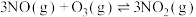

已知:反应Ⅰ:
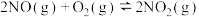
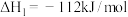
反应Ⅱ:
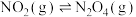
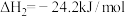
反应Ⅲ:
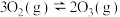
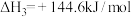
(4)碳氧化物的转化有重大用途,请回答下列问题,已知:
①


②
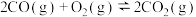

③
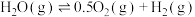

则
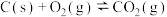

 、
、 、
、 表示)。
表示)。
更新时间:2022-07-21 13:25:56
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.已知下列热化学方程式:①H2(g)+ O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,
②H2(g)+ O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
③C(s)+ O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为___________ ;(填序号)
(2)燃烧1gH2生成气态水,放出的热量为___________ 。
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是___________ (填序号)。
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量___________ (填“大于”“等于”或“小于”)57.3kJ,原因是___________ 。
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能___________ (填“>”“<”或“=”,下同)生成物的总键能,则该反应的反应热∆H ___________ 0。
 O2(g)=H2O(l) ∆H=-285kJ·mol-1,
O2(g)=H2O(l) ∆H=-285kJ·mol-1,②H2(g)+
 O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,
O2(g)=H2O(g) ∆H=-241.8kJ·mol-1,③C(s)+
 O2(g)=CO(g) ∆H=-110.5kJ·mol-1,
O2(g)=CO(g) ∆H=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)C燃烧热的热化学方程式为
(2)燃烧1gH2生成气态水,放出的热量为
Ⅱ.中和热是一类重要的反应热,也是化学研究的重要课题。已知强酸稀溶液与强碱稀溶液发生反应的热化学方程式为H+(aq)+OH-(aq)=H2O(l) ∆H1=-57.3kJ•mol-1。
(1)下列各组试剂混合发生反应的离子方程式为H++OH-=H2O的是
A.盐酸与氢氧化钠溶液
B.稀硫酸与氢氧化钡溶液
C.醋酸与氢氧化钠固体
D.硫酸氢钠溶液与氢氧化钠溶液
E.氢氧化镁溶于稀盐酸
(2)若稀硫酸与氢氧化钠固体反应生成1molH2O(l),则反应放出的热量
Ⅲ.如图所示,某反应在不同条件下的反应历程分别为a、b。

据图可判断出反应物的总键能
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出下列燃烧热的热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式______ 。
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式___________ 。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ的热量。写出CH4的燃烧热化学方程式
(2)在标准状况下,44.8LH2完全燃烧生成液态水放出571.6kJ的热量,求在此条件下H2的燃烧热化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
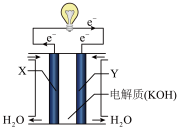
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】CO2是地球上取之不尽用之不竭的碳源,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)CO2加氢制备甲酸(HCOOH,熔点8.4℃沸点100.8℃)是利用化学载体进行H2储存的关键步骤。
已知:H2(g)+CO2(g)⇌HCOOH(l)∆H1=-30.0kJ•mol-1 2H2(g)+O2(g)=2H2O(1)∆H2=-571.6kJ•mol-1;则表示HCOOH燃烧热的热化学方程式为_______ 。
(1)CO2加氢制备甲酸(HCOOH,熔点8.4℃沸点100.8℃)是利用化学载体进行H2储存的关键步骤。
已知:H2(g)+CO2(g)⇌HCOOH(l)∆H1=-30.0kJ•mol-1 2H2(g)+O2(g)=2H2O(1)∆H2=-571.6kJ•mol-1;则表示HCOOH燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)比较下列各组热化学方程式中△H的大小关系:
①S(s)+O2(g)═SO2(g)△H1
S(g)+O2(g)═SO2(g)△H2
△H1__________ △H2(填><或“=”,下同);
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2
△H1_______ △H2;
③4Al(s)+3O2(g)═2Al2O3(s)△H1
4Fe(s)+3O2(g)═2Fe2O2(s)△H2
△H1_________ △H2
(2)已知H2(g)+1/2O2(g)=2H2O(g),反应过程中能量变化如下图:请回答下列问题:
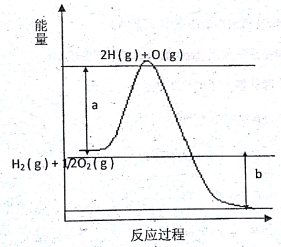
①图中a,b分别代表什么意义?
a.______________ ;b.__________ 。
②该反应是__________ 反应(填“吸热”或“放热”), △H ___________ (填“< 0”或“> 0”)。
①S(s)+O2(g)═SO2(g)△H1
S(g)+O2(g)═SO2(g)△H2
△H1
②CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2
△H1
③4Al(s)+3O2(g)═2Al2O3(s)△H1
4Fe(s)+3O2(g)═2Fe2O2(s)△H2
△H1
(2)已知H2(g)+1/2O2(g)=2H2O(g),反应过程中能量变化如下图:请回答下列问题:

①图中a,b分别代表什么意义?
a.
②该反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在1×105Pa和298K时,将1mol气态AB分子分离成气态A原子和B原子所需要的能量称为键能(kJ•mol﹣1).下面是一些共价键的键能:(已知氨分子中有三个等价的氮氢共价键)
①在1×105Pa、298K时,取一定量的N2和H2放入一密闭容器中,在催化剂存在下进行反应:N2+3H2⇌2NH3,生成2molNH3,该过程中,断键______ (填“释放”或“吸收”)能量_____ kJ,成键______ (填“释放”或“吸收”)能量_____ kJ;据此判断工业合成氨的反应是______ 反应(填“吸热”或“放热”);
②若将1molN2和3molH2放入一密闭容器中在催化剂存在下进行反应,理论上放出或吸收的热量为Q1,而在实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是_______
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2.
| 共价键 | H﹣H | N≡N | N﹣H |
| 键能(kJ•mol﹣1) | 436 | 945 | 391 |
①在1×105Pa、298K时,取一定量的N2和H2放入一密闭容器中,在催化剂存在下进行反应:N2+3H2⇌2NH3,生成2molNH3,该过程中,断键
②若将1molN2和3molH2放入一密闭容器中在催化剂存在下进行反应,理论上放出或吸收的热量为Q1,而在实际生产中,放出或吸收的热量为Q2,Q1与Q2比较,正确的是
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2.
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】按要求完成下列问题。
(1)某反应过程中的能量变化如下图所示:
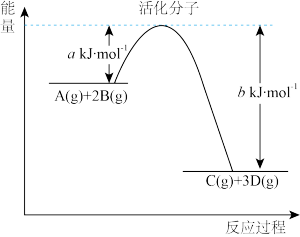
①该反应的ΔH_______ (填“>”或“<”)0。
②加入催化剂,b_______ (填“增大”“减小”或“不变”,下同),ΔH_______ 。
③该反应的热化学方程式为_______ 。
(2)已知: ① 2C(s)+O2(g)=2CO(g) ΔH=-221kJ/mol
② C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
则表示CO的燃烧热的热化学方程式为_______ 。
(1)某反应过程中的能量变化如下图所示:

①该反应的ΔH
②加入催化剂,b
③该反应的热化学方程式为
(2)已知: ① 2C(s)+O2(g)=2CO(g) ΔH=-221kJ/mol
② C(s)+O2(g)=CO2(g) ΔH=-393.5kJ/mol
则表示CO的燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】I.合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g) 2NH3(g)△H,合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
2NH3(g)△H,合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步N2(g)→2N*;H2(g)→2H*(慢反应)
第二步N*+H*=NH*;NH*+H*=NH2*;NH2*+H*=NH3*(快反应)
第三步NH3*=NH3(g)(快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1_____ E2(填“>”“<"或“=")。
II.(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:________ 。

(2)若已知下列数据:
试根据表中及图中数据计算N—H键的键能:___________ kJ·mol-1。
(3)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq)ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=_________________
 2NH3(g)△H,合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
2NH3(g)△H,合成氨反应在催化剂作用下的反应历程为(*表示吸附态):第一步N2(g)→2N*;H2(g)→2H*(慢反应)
第二步N*+H*=NH*;NH*+H*=NH2*;NH2*+H*=NH3*(快反应)
第三步NH3*=NH3(g)(快反应)
比较第一步反应的活化能E1与第二步反应的活化能E2的大小:E1
II.(1)如图是N2(g)和H2(g)反应生成1molNH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:

(2)若已知下列数据:
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
(3)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq)ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=
您最近一年使用:0次



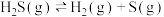
 ;
;
 。
。


