为探究矿物(含三种常见元素)的组成和性质,某兴趣小组设计了如下实验:已知实验中所用试剂均足量,请回答如下问题:
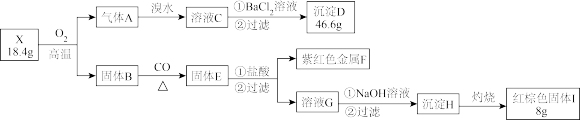
(1)X所含元素的名称为:_______ 。
(2)检验溶液G中的金属阳离子的实验方案:_______ 。
(3)气体A与溴水反应的离子方程式:_______ 。
(4)X在高温下与氧气充分反应的化学方程式:_______ 。

(1)X所含元素的名称为:
(2)检验溶液G中的金属阳离子的实验方案:
(3)气体A与溴水反应的离子方程式:
(4)X在高温下与氧气充分反应的化学方程式:
21-22高一下·浙江金华·期末 查看更多[2]
更新时间:2022-07-28 22:38:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】碘化亚铜(CuI) 是一种白色固体,见光易分解变成棕黄色,不溶于水和乙醇,常用作有机反应催化剂、阳极射线管覆盖物、动物饲料添加剂等。某小组同学以冰铜(Cu2S 和FeS熔体)为原料制备无水CuI的流程如图。

(1)“操作I”和“操作II”相同,所用到的玻璃仪器有_______ 。
(2)“焙烧”过程中Cu被还原,同时有黑色磁性物质生成,熔渣的主要成分为_______ (填化学式)。
(3)“熔渣”酸浸时,用H2O2处理可得到蓝色溶液,用化学方程式解释为_______ ;当加热温度高于40°C时,该过程反应速率减慢,其可能原因是_______ 。

(1)“操作I”和“操作II”相同,所用到的玻璃仪器有
(2)“焙烧”过程中Cu被还原,同时有黑色磁性物质生成,熔渣的主要成分为
(3)“熔渣”酸浸时,用H2O2处理可得到蓝色溶液,用化学方程式解释为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】根据下图各物质的转化关系,回答下列问题。
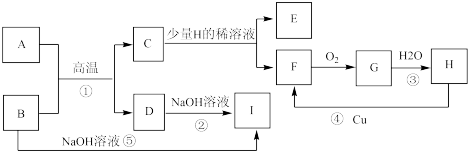
已知:化合物A是红棕色粉末,G是红棕色气体,B、C是常见的金属单质。
(1)向溶液E中滴加氢氧化钠溶液时的现象是_______ 。
(2)反应③中,氧化剂与还原剂的物质的量之比为_______ 。
(3)工业冶炼金属B的方法_______ 。
(4)写出反应④的离子方程式_______ 。
(5)写出反应②的化学方程式_______ 。
(6)向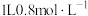 的H的稀溶液中加入足量铜片,反应结束后,再加入足量稀硫酸,又能溶解
的H的稀溶液中加入足量铜片,反应结束后,再加入足量稀硫酸,又能溶解_______ g的铜。

已知:化合物A是红棕色粉末,G是红棕色气体,B、C是常见的金属单质。
(1)向溶液E中滴加氢氧化钠溶液时的现象是
(2)反应③中,氧化剂与还原剂的物质的量之比为
(3)工业冶炼金属B的方法
(4)写出反应④的离子方程式
(5)写出反应②的化学方程式
(6)向
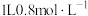 的H的稀溶液中加入足量铜片,反应结束后,再加入足量稀硫酸,又能溶解
的H的稀溶液中加入足量铜片,反应结束后,再加入足量稀硫酸,又能溶解
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】中学化学中几种常见物质的转化关系如下图(有部分产物未画出)。A是一种金属单质,D是一种非金属固体单质。

回答下列问题:
(1)A是_______ G是_______
(2)请写出鉴定B中阳离子的实验方法和现象_______
(3)在酸性条件下,再举出可使B转化为C的两种试剂_______
(4)写出反应C+A→B的离子方程式:_______
(5)写出反应E+H2O2→F的化学方程式:_______

回答下列问题:
(1)A是
(2)请写出鉴定B中阳离子的实验方法和现象
(3)在酸性条件下,再举出可使B转化为C的两种试剂
(4)写出反应C+A→B的离子方程式:
(5)写出反应E+H2O2→F的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
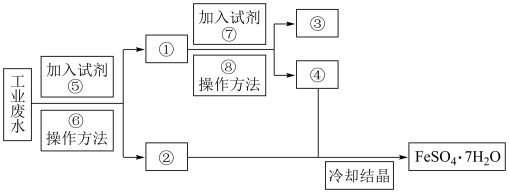
【推荐1】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题。
①___________ ;②___________ ;③___________ ;④___________ ;
⑤___________ ;⑥___________ ;⑦___________ ;⑧___________ ;
(2)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是___________ ,现象依次是___________ ;请写出该鉴别过程中属于氧化还原反应的离子方程式:___________ 。
(3)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,产生的现象是___________ ;此过程涉及反应的化学方程式是___________ 。
①
⑤
(2)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是
(3)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,产生的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
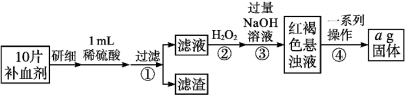
【推荐2】硫酸亚铁晶体(FeSO4·7H2O)在医药上用作补血剂。某课外小组设计实验测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:
(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有金属阳离子是_______ (填离子符号),检验滤液中还存在Fe2+的方法为_______ (说明试剂、现象)。
(2)步骤②加入过量H2O2的目的是_______ 。
(3)步骤③中反应的离子方程式为_______ 。
(4)步骤④中一系列处理的操作步骤包括:过滤、_______ 、干燥、灼烧、冷却、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为_______ g。

请回答下列问题:
(1)向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有金属阳离子是
(2)步骤②加入过量H2O2的目的是
(3)步骤③中反应的离子方程式为
(4)步骤④中一系列处理的操作步骤包括:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铬铁矿的主要成分为FeCr2O4,还含有杂质SiO2及少量难溶于水、碱溶液的物质。以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程如图所示: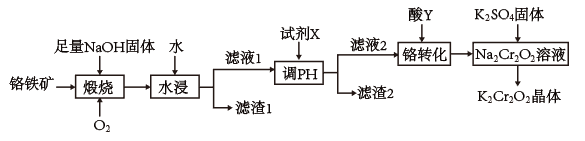
回答下列问题:
(1)煅烧前需将铬铁矿和NaOH固体粉碎后混合,其目的是___________ 。
(2)煅烧后铬铁矿转化为Na2CrO4和NaFeO2,已知NaFeO2遇水强烈水解,“水浸”时NaFeO2水解的离子方程式是___________ ;滤液1中的主要阴离子有CrO 、
、___________ 、___________ 。
(3)酸Y是___________ (填化学式,下同);流程中若去掉“调pH”这一操作,产品中可能含有的较多杂质是___________ 。
(4)为了防止铬对环境的污染,排出的含有Cr2O 的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O
的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O 转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
①室温下Ksp[Cr( OH)3]=___________ mol4•L﹣4。
②分离出的污泥可以加入到流程___________ (填工艺流程中的步骤名称)中,其回收的目的是___________ 。

回答下列问题:
(1)煅烧前需将铬铁矿和NaOH固体粉碎后混合,其目的是
(2)煅烧后铬铁矿转化为Na2CrO4和NaFeO2,已知NaFeO2遇水强烈水解,“水浸”时NaFeO2水解的离子方程式是
 、
、(3)酸Y是
(4)为了防止铬对环境的污染,排出的含有Cr2O
 的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O
的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O 转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。①室温下Ksp[Cr( OH)3]=
②分离出的污泥可以加入到流程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】由四种常见元素组成的化合物X,按如下流程进行实验。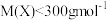 。
。
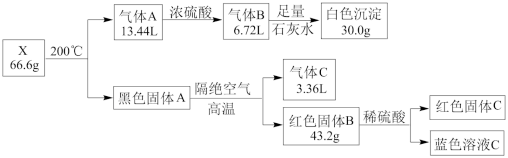
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是___________ (填元素符号)。
(2)化合物X在空气中加热发生反应的化学方程式___________ 。
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:___________ 。
(4)写出红色固体B与稀硫酸反应的离子方程式:___________ 。
(5)某兴趣小组用气体 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:___________ 。
 。
。
已知:固体A、B、C均为纯净物,且C为单质。气体C是单质,且能使带火星的木条复燃。气体体积已折算成标准状况。请回答:
(1)组成X的四种元素是
(2)化合物X在空气中加热发生反应的化学方程式
(3)黑色固体A与乙醇在加热条件下也可以得到红色固体C,该反应的化学方程式:
(4)写出红色固体B与稀硫酸反应的离子方程式:
(5)某兴趣小组用气体
 还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
还原少量黑色固体A,使A完全反应得到红色产物。为确定红色产物的成分,请设计实验方案:
您最近一年使用:0次
【推荐2】实验小组对NaHSO3溶液分别与CuCl2、CuSO4溶液的反应进行探究。
已知:Ⅰ.Cu2+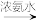 [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)
Ⅱ. Cu+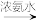 [Cu(NH3)]+(无色溶液)
[Cu(NH3)]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)
(1)推测实验Ⅰ产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到_______ ,反应的离子方程式为_______ 。
(2)对实验Ⅰ产生SO2的原因进行分析,提出假设:
假设a: Cu2+水解使溶液中c(H+)增大;
假设b: Cl-存在时,Cu2+与HSO3-反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设a不合理,实验证据是_______ ;
②实验表明假设b合理,实验I反应的离子方程式有_____ 、H++ HSO3-= SO2↑+H2O。
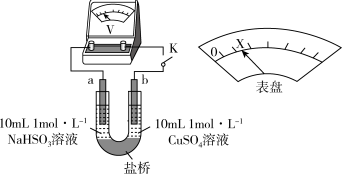
(3)对比实验Ⅰ、Ⅱ,提出假设:Cl-增强了Cu2+的氧化性。
下述实验Ⅲ证实了假设合理,装置如图。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管_______ (补全实验操作及现象)。
(4)将实验Ⅱ的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和SO32−。
①通过实验Ⅳ证实红色沉淀中含有Cu+和Cu2+。
实验Ⅳ: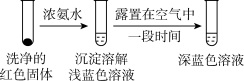
证实红色沉淀中含有Cu+的实验证据是_______ ;
②有同学认为实验Ⅳ不足以证实红色沉淀中含有Cu2+,设计实验Ⅳ的对比实验Ⅴ,证实了Cu2+的存在。实验Ⅴ的方案和现象是:_______ 。
| 实验 | 装置 | 试剂x | 操作及现象 |
| Ⅰ | 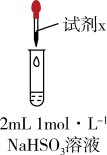 | 1 mol·L−1CuCl2溶液 | 加入2mL CuCl2溶液,得到绿色溶液,30s时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
| Ⅱ | 1 mol·L−1CuSO4溶液 | 加入2mL CuSO4溶液,得到绿色溶液,3分钟未见明显变化。 |
 [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)Ⅱ. Cu+
 [Cu(NH3)]+(无色溶液)
[Cu(NH3)]+(无色溶液) [Cu(NH3)4]2+(深蓝色溶液)
[Cu(NH3)4]2+(深蓝色溶液)(1)推测实验Ⅰ产生的无色气体为SO2,实验证实推测正确:用蘸有碘水的淀粉试纸接近试管口,观察到
(2)对实验Ⅰ产生SO2的原因进行分析,提出假设:
假设a: Cu2+水解使溶液中c(H+)增大;
假设b: Cl-存在时,Cu2+与HSO3-反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设a不合理,实验证据是
②实验表明假设b合理,实验I反应的离子方程式有
(3)对比实验Ⅰ、Ⅱ,提出假设:Cl-增强了Cu2+的氧化性。
下述实验Ⅲ证实了假设合理,装置如图。实验方案:闭合K,电压表的指针偏转至“X”处;向U形管

(4)将实验Ⅱ的溶液静置24小时或加热后,得到红色沉淀。经检验,红色沉淀中含有Cu+、Cu2+和SO32−。
①通过实验Ⅳ证实红色沉淀中含有Cu+和Cu2+。
实验Ⅳ:

证实红色沉淀中含有Cu+的实验证据是
②有同学认为实验Ⅳ不足以证实红色沉淀中含有Cu2+,设计实验Ⅳ的对比实验Ⅴ,证实了Cu2+的存在。实验Ⅴ的方案和现象是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】以铜片(含少量杂质铁)为原料制取Cu(NO3)2溶液的实验流程如图:
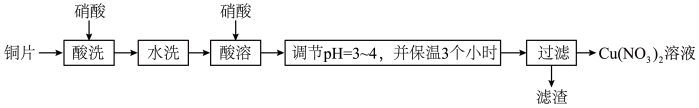
(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:___ 。
(2)“水洗”后检验铜片表面是否洗涤干净的方法是___ 。
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O
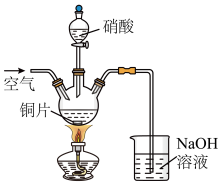
①“酸溶”时为防止反应过于剧烈,可以采取的方法有___ 和___ 。
②通入空气的作用是___ 、___ 。
(4)“调节pH=3~4,并保温3个小时”的目的是___ 。
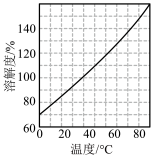
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:___ 。
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

(1)“酸洗”的目的是除去铜片表面难溶的Cu2(OH)2SO4,写出“酸洗”时反应的离子方程式:
(2)“水洗”后检验铜片表面是否洗涤干净的方法是
(3)“酸溶”时的装置如图所示,烧杯内所发生的反应为:
NO+NO2+2OH-=2NO2-+H2O
2NO2+2OH-=NO2-+NO3-+H2O

①“酸溶”时为防止反应过于剧烈,可以采取的方法有
②通入空气的作用是
(4)“调节pH=3~4,并保温3个小时”的目的是
(5)烧杯中所得溶液经多步处理得到NaNO3固体。设计以烧杯中所得溶液为原料,制取NaNO3固体的实验方案:
[已知3NaNO2+2HNO3=3NaNO3+2NO↑+H2O;NaNO3的溶解度随温度变化如图所示。实验中必须使用的试剂:硝酸和NaOH溶液]。

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了探究钠、铁及其化合物的性质,某课外活动小组设计并进行了下列实验。
实验一:按如图所示装置进行实验,E中收集相对纯净的气体。填写相关内容:
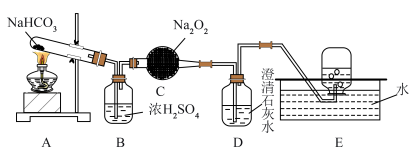
(1)C中发生反应的化学方程式为________ 。
(2)若C中反应不充分,则D(盛有足量澄清石灰水)中的现象是_______ 。
实验二: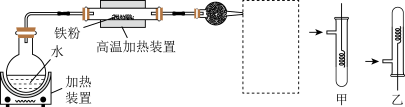
(3)写出在高温加热装置中发生反应的化学方程式_______ 。
(4)虚线框处宜选择的装置是______ (填“甲”或“乙”);实验时应先将螺旋状铜丝加热,变黑后再趁热迅速伸入所制得的纯净气体中,观察到的实验现象是_________ 。
实验三:绿矾(FeSO4∙xH2O)是含有一定量结晶水的硫酸亚铁,为测定绿矾中结晶水的含量,将石英玻璃管(带两端开关K1和K2,设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g,B为干燥管。按图连接好装置进行实验。
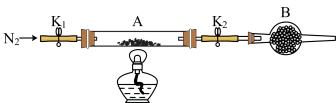
实验步骤如下:①________,②点燃酒精灯,加热,③_______,④_______,⑤_______,⑥称量A,重复上述操作步骤,直至A恒重,记为m3g。
(5)请将下列实验步骤的编号填写在对应步骤的横线上______ 。
a.关闭K1和K2 b.熄灭酒精灯
c.打开K1和K2,缓缓通入N2 d.冷却至室温
(6)已知在上述实验条件下,绿矾受热只是失去结晶水,硫酸亚铁本身不会分解,根据实验记录,计算绿矾化学式中结晶水的数目x=_______ (用含m1、m2、m3的代数式表示)。
实验一:按如图所示装置进行实验,E中收集相对纯净的气体。填写相关内容:

(1)C中发生反应的化学方程式为
(2)若C中反应不充分,则D(盛有足量澄清石灰水)中的现象是
实验二:

(3)写出在高温加热装置中发生反应的化学方程式
(4)虚线框处宜选择的装置是
实验三:绿矾(FeSO4∙xH2O)是含有一定量结晶水的硫酸亚铁,为测定绿矾中结晶水的含量,将石英玻璃管(带两端开关K1和K2,设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g,B为干燥管。按图连接好装置进行实验。

实验步骤如下:①________,②点燃酒精灯,加热,③_______,④_______,⑤_______,⑥称量A,重复上述操作步骤,直至A恒重,记为m3g。
(5)请将下列实验步骤的编号填写在对应步骤的横线上
a.关闭K1和K2 b.熄灭酒精灯
c.打开K1和K2,缓缓通入N2 d.冷却至室温
(6)已知在上述实验条件下,绿矾受热只是失去结晶水,硫酸亚铁本身不会分解,根据实验记录,计算绿矾化学式中结晶水的数目x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
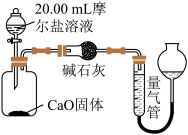
【推荐2】硫酸亚铁铵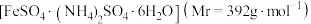 又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
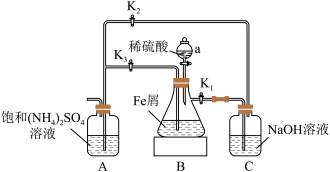
Ⅰ 摩尔盐的制取:
摩尔盐的制取:
(1)仪器a的名称为:_________________
(2)检查装置气密性,加入药品,先关闭 ,打开
,打开 、
、 和仪器a活塞,装置B中有气体产生,该气体的作用是
和仪器a活塞,装置B中有气体产生,该气体的作用是______________ 。反应一段时间后,欲使摩尔盐在装置A中生成的对应操作为___________ 。
Ⅱ 摩尔盐纯度测定:取
摩尔盐纯度测定:取 硫酸亚铁铵样品配制成
硫酸亚铁铵样品配制成 溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
 甲
甲 方案一:取
方案一:取 硫酸亚铁铵溶液用
硫酸亚铁铵溶液用 的酸性
的酸性 溶液进行三次滴定。
溶液进行三次滴定。
 乙
乙 方案二:
方案二: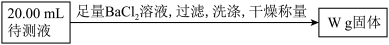
 丙
丙 方案三:实验设计图如图所示:
方案三:实验设计图如图所示:
(3)写出方案一发生反应的离子方程式____________ ,若甲乙两同学实验操作都正确,但方案一的测定结果总是小于方案二,推测可能原因: _________ ;设计实验验证你的推测:_____________ 。
(4)方案三测得 的体积为
的体积为 已折算为标准状况下
已折算为标准状况下 ,计算摩尔盐的纯度
,计算摩尔盐的纯度________ 。 计算结果保留一位小数
计算结果保留一位小数
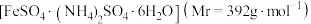 又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
又称摩尔盐,某实验小组利用如图装置制取摩尔盐并测其纯度。
Ⅰ
 摩尔盐的制取:
摩尔盐的制取:(1)仪器a的名称为:
(2)检查装置气密性,加入药品,先关闭
 ,打开
,打开 、
、 和仪器a活塞,装置B中有气体产生,该气体的作用是
和仪器a活塞,装置B中有气体产生,该气体的作用是Ⅱ
 摩尔盐纯度测定:取
摩尔盐纯度测定:取 硫酸亚铁铵样品配制成
硫酸亚铁铵样品配制成 溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答:
溶液,甲、乙、丙三位同学设计了如下三个实验方案,请回答: 甲
甲 方案一:取
方案一:取 硫酸亚铁铵溶液用
硫酸亚铁铵溶液用 的酸性
的酸性 溶液进行三次滴定。
溶液进行三次滴定。 乙
乙 方案二:
方案二: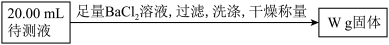
 丙
丙 方案三:实验设计图如图所示:
方案三:实验设计图如图所示:
(3)写出方案一发生反应的离子方程式
(4)方案三测得
 的体积为
的体积为 已折算为标准状况下
已折算为标准状况下 ,计算摩尔盐的纯度
,计算摩尔盐的纯度 计算结果保留一位小数
计算结果保留一位小数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】I-测定的基本原理是将其氧化成I2,再用Na2S2O3标准溶液来滴定。如果样品中仅含有微量I-,必须用“化学放大”反应将碘的量“放大”,然后再进行测定。下面是化学放大反应的实验步骤:
Ⅰ.将含有微量I-的样品溶液调至中性或弱酸性,加入溴水,将I-完全氧化成IO ,煮沸去掉过量的溴;
,煮沸去掉过量的溴;
Ⅱ.取上述溶液,加入过量硫酸酸化的KI溶液,振荡,溶液颜色呈棕黄色;
Ⅲ.将Ⅱ所得溶液中全部的I2萃取至CCl4中;
Ⅳ.向分液后的CCl4溶液中加入肼(N2H4)的水溶液,产生无毒的N2,分去有机层;
Ⅴ.将Ⅳ所得水溶液重复Ⅰ、Ⅱ步骤;
Ⅵ.以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。
已知:反应为I2+2S2O =2I-+S4O
=2I-+S4O ;Na2S2O3和Na2S4O6溶液颜色均为无色。
;Na2S2O3和Na2S4O6溶液颜色均为无色。
(1)Ⅰ中氧化剂和还原剂物质的量之比为_______ 。
(2)Ⅲ中使用的主要玻璃仪器是_______ (填名称)。
(3)Ⅳ中反应的离子方程式是_______ 。
(4)步骤Ⅵ需要在中性或弱酸性环境中进行,pH过大,特别是碱性条件下,Na2S2O3易被I2氧化成Na2SO4,其离子方程式为_______ ;结合离子方程式解释pH不宜过小的原因:_______ 。
Ⅰ.将含有微量I-的样品溶液调至中性或弱酸性,加入溴水,将I-完全氧化成IO
 ,煮沸去掉过量的溴;
,煮沸去掉过量的溴;Ⅱ.取上述溶液,加入过量硫酸酸化的KI溶液,振荡,溶液颜色呈棕黄色;
Ⅲ.将Ⅱ所得溶液中全部的I2萃取至CCl4中;
Ⅳ.向分液后的CCl4溶液中加入肼(N2H4)的水溶液,产生无毒的N2,分去有机层;
Ⅴ.将Ⅳ所得水溶液重复Ⅰ、Ⅱ步骤;
Ⅵ.以淀粉为指示剂,用Na2S2O3标准溶液滴定至终点。
已知:反应为I2+2S2O
 =2I-+S4O
=2I-+S4O ;Na2S2O3和Na2S4O6溶液颜色均为无色。
;Na2S2O3和Na2S4O6溶液颜色均为无色。(1)Ⅰ中氧化剂和还原剂物质的量之比为
(2)Ⅲ中使用的主要玻璃仪器是
(3)Ⅳ中反应的离子方程式是
(4)步骤Ⅵ需要在中性或弱酸性环境中进行,pH过大,特别是碱性条件下,Na2S2O3易被I2氧化成Na2SO4,其离子方程式为
您最近一年使用:0次



