铬铁矿的主要成分为FeCr2O4,还含有杂质SiO2及少量难溶于水、碱溶液的物质。以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程如图所示: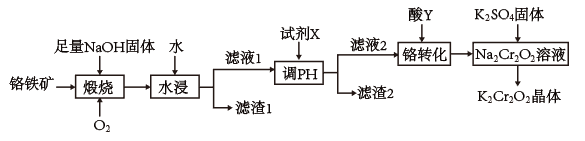
回答下列问题:
(1)煅烧前需将铬铁矿和NaOH固体粉碎后混合,其目的是___________ 。
(2)煅烧后铬铁矿转化为Na2CrO4和NaFeO2,已知NaFeO2遇水强烈水解,“水浸”时NaFeO2水解的离子方程式是___________ ;滤液1中的主要阴离子有CrO 、
、___________ 、___________ 。
(3)酸Y是___________ (填化学式,下同);流程中若去掉“调pH”这一操作,产品中可能含有的较多杂质是___________ 。
(4)为了防止铬对环境的污染,排出的含有Cr2O 的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O
的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O 转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
①室温下Ksp[Cr( OH)3]=___________ mol4•L﹣4。
②分离出的污泥可以加入到流程___________ (填工艺流程中的步骤名称)中,其回收的目的是___________ 。

回答下列问题:
(1)煅烧前需将铬铁矿和NaOH固体粉碎后混合,其目的是
(2)煅烧后铬铁矿转化为Na2CrO4和NaFeO2,已知NaFeO2遇水强烈水解,“水浸”时NaFeO2水解的离子方程式是
 、
、(3)酸Y是
(4)为了防止铬对环境的污染,排出的含有Cr2O
 的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O
的酸性废水需要处理,可用焦亚硫酸钠(Na2S2O5)将Cr2O 转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。
转化为毒性较低的Cr3+,室温下再调节pH=8,使Cr3+转化成Cr(OH)3而沉降,分离出污泥,检测到废水中Cr3+浓度约为2.6×10﹣8mg•L﹣1。①室温下Ksp[Cr( OH)3]=
②分离出的污泥可以加入到流程
更新时间:2021-01-08 19:36:38
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】炼铝厂的废料中主要含Al、Al2O3及少量SiO2和FeO·xFe2O3,可用于制备明矾[KAl(SO4)2·12H2O]。工艺流程如下:

(1)“酸浸”过程中的应选择___________ (写酸的化学式)。为提高浸出速率,除适当增大酸的浓度外,还可采取的措施有___________ 。(写出一条)
(2)操作Ⅰ是___________ ,操作Ⅱ是___________ 、___________ 、过滤、洗涤、干燥。
(3)在溶液A中加入高锰酸钾发生反应的离子方程式为(该条件下 转化为Mn2+)
转化为Mn2+)___________ 。已知:生成氢氧化物沉淀的pH如下表所示
调节pH=3的目的是___________ 。此步骤中,可以用H2O2代替KMnO4,写出H2O2的电子式___________ 。
(4)只用一种 试剂检验溶液A中是否存在Fe2+,该试剂是___________ (写名称)。

(1)“酸浸”过程中的应选择
(2)操作Ⅰ是
(3)在溶液A中加入高锰酸钾发生反应的离子方程式为(该条件下
 转化为Mn2+)
转化为Mn2+)| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
调节pH=3的目的是
(4)只用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】 用途广泛,可作颜料、催化剂、净水剂等。实验室制备
用途广泛,可作颜料、催化剂、净水剂等。实验室制备 流程如下,回答下列问题:
流程如下,回答下列问题:
I. 的制备:以废铁屑为原料进行制备,已知废铁屑表面有油污,且混有少量铜杂质,制备流程图如下:
的制备:以废铁屑为原料进行制备,已知废铁屑表面有油污,且混有少量铜杂质,制备流程图如下:

(1)步骤①中使用热纯碱的目的是_______ ,相比纯铁屑,步骤②中废铁屑与稀盐酸的反应产生气泡的速率更快,原因是_______ 。
(2)检验 溶液中是否残留
溶液中是否残留 可选用_______。
可选用_______。
(3)由 溶液获得
溶液获得 的操作为
的操作为_______ 、过滤、洗涤、干燥。
Ⅱ.由 制备无水
制备无水
 (亚硫酰氯)是一种液态化合物,沸点为
(亚硫酰氯)是一种液态化合物,沸点为 ,遇水剧烈反应生成两种酸性气体,其中一种能使品红溶液褪色。将
,遇水剧烈反应生成两种酸性气体,其中一种能使品红溶液褪色。将 与液体
与液体 混合共热,制得无水
混合共热,制得无水 ,装置如下图所示(夹持和加热装置略)。
,装置如下图所示(夹持和加热装置略)。

(4)写出 与水反应的化学方程式
与水反应的化学方程式_______ 。
(5)球形冷凝管的作用是_______ ,实验开始时,需向球形冷凝管中通入冷却水,冷却水应从_______ (填“a”或“b”)口进入冷凝管。
(6)仪器A的名称为_______ ,所装试剂为无水 ,作用是
,作用是_______ 。
 用途广泛,可作颜料、催化剂、净水剂等。实验室制备
用途广泛,可作颜料、催化剂、净水剂等。实验室制备 流程如下,回答下列问题:
流程如下,回答下列问题:I.
 的制备:以废铁屑为原料进行制备,已知废铁屑表面有油污,且混有少量铜杂质,制备流程图如下:
的制备:以废铁屑为原料进行制备,已知废铁屑表面有油污,且混有少量铜杂质,制备流程图如下:
(1)步骤①中使用热纯碱的目的是
(2)检验
 溶液中是否残留
溶液中是否残留 可选用_______。
可选用_______。A.氯水和 溶液 溶液 | B.酸性 溶液 溶液 |
| C.浓氨水 | D.铁氰化钾溶液 |
(3)由
 溶液获得
溶液获得 的操作为
的操作为Ⅱ.由
 制备无水
制备无水
 (亚硫酰氯)是一种液态化合物,沸点为
(亚硫酰氯)是一种液态化合物,沸点为 ,遇水剧烈反应生成两种酸性气体,其中一种能使品红溶液褪色。将
,遇水剧烈反应生成两种酸性气体,其中一种能使品红溶液褪色。将 与液体
与液体 混合共热,制得无水
混合共热,制得无水 ,装置如下图所示(夹持和加热装置略)。
,装置如下图所示(夹持和加热装置略)。
(4)写出
 与水反应的化学方程式
与水反应的化学方程式(5)球形冷凝管的作用是
(6)仪器A的名称为
 ,作用是
,作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。以硫铁矿(主要成分为 ,杂质不与盐酸反应)为原料制备三氯化铁晶体
,杂质不与盐酸反应)为原料制备三氯化铁晶体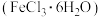 的工艺流程如图所示:
的工艺流程如图所示:
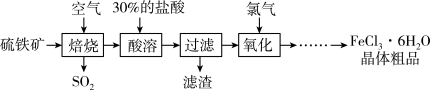
回答下列问题:
(1)“焙烧”过程中,理论上 ,被氧化转移
,被氧化转移 电子,则该反应的氧化产物为
电子,则该反应的氧化产物为_____________ 。
(2)现有试剂:①稀盐酸 ②稀硫酸 ③稀硝酸 ④氯气 ⑤硫氰化钾溶液 ⑥高锰酸钾溶液 ⑦氢氧化钠溶液。
为确认“酸溶”后的溶液中是否会含 ,另取“焙烧”后的烧渣少许,用
,另取“焙烧”后的烧渣少许,用________ (从上述试剂中选择,填标号)溶解,将所得溶液滴入______________ (从上述试剂中选择,填标号)中,若_________ ,则说明“酸溶”后的溶液中含 。
。
(3)从 溶液中得到
溶液中得到 的操作包括
的操作包括_______ 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________________ 。
(4)从 中得到无水
中得到无水 的操作方法为
的操作方法为____________________________ 。
(5)若以a吨硫铁矿为原料,最终制得b吨 ,不计生产过程中的损失,则该硫铁矿中
,不计生产过程中的损失,则该硫铁矿中 的含量为
的含量为_______________ (用含a、b的代数式表示)。
 ,杂质不与盐酸反应)为原料制备三氯化铁晶体
,杂质不与盐酸反应)为原料制备三氯化铁晶体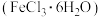 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“焙烧”过程中,理论上
 ,被氧化转移
,被氧化转移 电子,则该反应的氧化产物为
电子,则该反应的氧化产物为(2)现有试剂:①稀盐酸 ②稀硫酸 ③稀硝酸 ④氯气 ⑤硫氰化钾溶液 ⑥高锰酸钾溶液 ⑦氢氧化钠溶液。
为确认“酸溶”后的溶液中是否会含
 ,另取“焙烧”后的烧渣少许,用
,另取“焙烧”后的烧渣少许,用 。
。(3)从
 溶液中得到
溶液中得到 的操作包括
的操作包括(4)从
 中得到无水
中得到无水 的操作方法为
的操作方法为(5)若以a吨硫铁矿为原料,最终制得b吨
 ,不计生产过程中的损失,则该硫铁矿中
,不计生产过程中的损失,则该硫铁矿中 的含量为
的含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
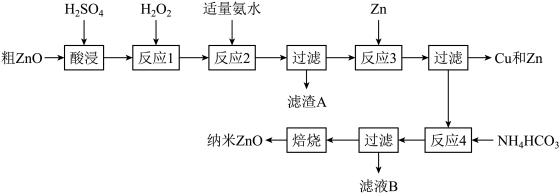
【推荐1】纳米ZnO的颗粒直径介于1~100nm之间,具有许多特殊的性能,可用于制造变阻器、图像记录材料、磁性材料和塑料薄膜等。一种利用粗ZnO(含FeO、Fe2O3、CuO)制备纳米ZnO的生产工艺流程如下图所示:
已知:① 生成氢氧化物沉淀时溶液的pH如下表:
② 25℃时,Fe(OH)3的溶度积常数Ksp=4.0×10-38。
请回答以以下问题:
(1)酸浸时,为了提高浸出率,可采取的措施有________ (填写两种);
(2)反应1中发生反应的离子方程式为______________ ,一种双氧水的质量分数为34.0 % (密度为1.13g/cm3) ,其浓度为_______ mol/L;
(3)反应2中加适量氨水的目的是_________ ,此时所需pH的范围为_________ ,当调节溶液pH=5时,溶液中的c(Fe3+)=__________ ;
(4)反应3的离子方程式为__________ ,反应类型为__________ ;
(5)从滤液B中可回收的主要物质是__________ ;
(6)经检验分析,反应4 所得固体组成为Zna(OH)bCO3,称取该固体22.4g,焙烧后得固体16.2g,则a=_________ 。
已知:① 生成氢氧化物沉淀时溶液的pH如下表:
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
| 完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
② 25℃时,Fe(OH)3的溶度积常数Ksp=4.0×10-38。
请回答以以下问题:
(1)酸浸时,为了提高浸出率,可采取的措施有
(2)反应1中发生反应的离子方程式为
(3)反应2中加适量氨水的目的是
(4)反应3的离子方程式为
(5)从滤液B中可回收的主要物质是
(6)经检验分析,反应4 所得固体组成为Zna(OH)bCO3,称取该固体22.4g,焙烧后得固体16.2g,则a=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
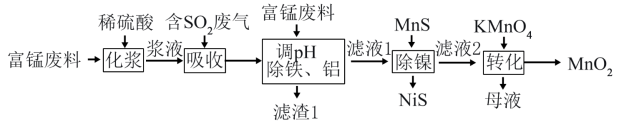
【推荐2】MnO2是常用的电极材料和催化剂。由富锰废料(含MnO2、MnCO3、Fe2O3和少量Al2O3、NiO)进行废气脱硫并制备MnO2的工艺流程如下:
已知:I.难溶物的溶度积常数如表所示。
II.溶液中离子浓度≤10-5mol·L-1时,认为该离子沉淀完全
回答下列问题:
(1)“化浆”时生成气体的电子式为_______ 。
(2)“吸收”时,浆液与含SO2废气通过逆流方式混合目的为_______ ;该过程中,MnO2发生反应的离子方程式为_______ 。
(3)“吸收”所得溶液中c(Fe2+)=0.04mol·L-1、c(Ni2+)=0.00017mol·L-1、c(A13+)=0.001mol·L-1、c(Mn2+)=0.12mol·L-1,滤液1中c(Mn2+)=0.2mol·L-1、c(Ni2+)=0.0002mol·L-1,则“调pH”的范围为_______ (溶液体积变化忽略不计,保留两位有效数字);从滤渣1中分离出Al(OH)3的方法为_______ 。
(4)“除镍”时,将Ni2+转化为NiS而不是Ni(OH)2的原因为_______ 。
(5)“转化"反应在pH=5的条件下进行,其主要反应中氧化剂与还原剂的物质的量之比为_______ 。

已知:I.难溶物的溶度积常数如表所示。
| 难溶物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Ni(OH)2 | Al(OH)3 | MnS | FeS | NiS |
| 溶度积常数(Ksp) | 4×10-38 | 2×10-16 | 2×10-13 | 2×10-16 | 1×10-33 | 1×10-15 | 6×10-18 | 1×10-24 |
回答下列问题:
(1)“化浆”时生成气体的电子式为
(2)“吸收”时,浆液与含SO2废气通过逆流方式混合目的为
(3)“吸收”所得溶液中c(Fe2+)=0.04mol·L-1、c(Ni2+)=0.00017mol·L-1、c(A13+)=0.001mol·L-1、c(Mn2+)=0.12mol·L-1,滤液1中c(Mn2+)=0.2mol·L-1、c(Ni2+)=0.0002mol·L-1,则“调pH”的范围为
(4)“除镍”时,将Ni2+转化为NiS而不是Ni(OH)2的原因为
(5)“转化"反应在pH=5的条件下进行,其主要反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】碳酸锶( SrCO3)主要用于制造磁性材料、电子元件等。利用锶渣(主要成分SrSO4,含少量CaCO3、Fe2O3、Al2O3、MgCO3杂质),工业上制备超细碳酸锶的工艺如图1所示:
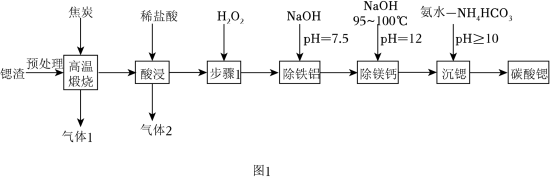
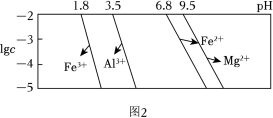
已知:①25°C时溶液中金属离子物质的量浓度c与溶液pH的关系如图2所示:
②Sr (OH)2、Ca(OH)2在不同温度下的溶解度表
回答下列问题:
(1)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为___________ 。
(2)不设置步骤1的后果是___________ 。
(3)“除铁铝”后溶液温度降至室温(25℃),溶液中c(Fe3+) 为___________ mol/L。
(4)“除镁钙”过程温度控制在95℃~100℃的目的是___________ 。
(5)“沉锶”的离子反应方程式为___________ 。
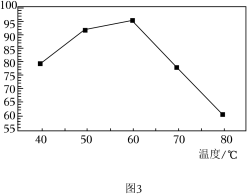
(6)“沉锶”过程中反应温度对锶转化率的影响如图3所示,温度高于60℃时,锶转化率降低的原因为___________ 。
(7)从平衡移动的角度分析“沉锶”过程中控制pH≥10的原因___________ 。

已知:①25°C时溶液中金属离子物质的量浓度c与溶液pH的关系如图2所示:

②Sr (OH)2、Ca(OH)2在不同温度下的溶解度表
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 90 | 100 |
| Ca(OH)2/g | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | 0.07 |
| Sr(OH)2/g | 0.91 | 1.77 | 3.95 | 8.42 | 20.20 | 44.50 | 91.20 |
(1)“高温煅烧”得到的主要产物为锶的硫化物和一种可燃性气体。则“高温煅烧”的主要反应化学方程式为
(2)不设置步骤1的后果是
(3)“除铁铝”后溶液温度降至室温(25℃),溶液中c(Fe3+) 为
(4)“除镁钙”过程温度控制在95℃~100℃的目的是
(5)“沉锶”的离子反应方程式为
(6)“沉锶”过程中反应温度对锶转化率的影响如图3所示,温度高于60℃时,锶转化率降低的原因为

(7)从平衡移动的角度分析“沉锶”过程中控制pH≥10的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:
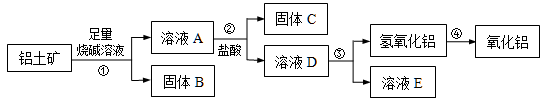
(1)固体B的主要用途有(写出1条即可)________________。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是 ; ;
第③步中,生成氢氧化铝的化学方程式是 。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是_______。(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol碳单质,转移1mol电子,反应的化学方程式是 。

(1)固体B的主要用途有(写出1条即可)________________。
(2)第①步,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是 ; ;
第③步中,生成氢氧化铝的化学方程式是 。
(3)将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是_______。(保留一位小数)
(4)工业上制取AlCl3用Al2O3与C、Cl2在高温条件下反应,每消耗0.5 mol碳单质,转移1mol电子,反应的化学方程式是 。
您最近一年使用:0次
【推荐2】硫酸镍是电镀工业必不可少的化工原料。从不锈钢废渣(主要含Fe42.35%、Cr9.67%、Ni5.1%、C4.7%、Si3.39%等)中制取硫酸镍晶体的工艺流程如图:
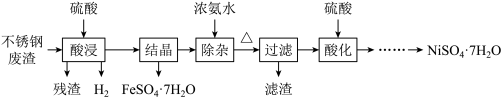 已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。
已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。
②Na2CrO4溶液中加酸调节pH为3.5时,CrO42-转化为Cr2O72-。
③相关物质在不同温度时溶解度如下表:
(1)“酸浸”后得到的溶液中主要含有FeSO4、NiSO4、Cr2(SO4)3,生成NiSO4的化学方程式为___ 。“酸浸”时需控制温度为90℃左右,可以采用的加热方式是___ 。
(2)“过滤”前,适当加热的目的是___ 。
(3)对“过滤”所得的滤渣进行洗涤,检验滤渣已洗涤干净的方法是___ 。
(4)“过滤”时产生的滤渣可用于制备Na2Cr2O7晶体。
①滤渣经干燥后与Na2CO3混合在空气中煅烧生成Na2CrO4和CO2,此反应的化学方程式为___ 。
②请补充完整上述煅烧后混合物制备Na2Cr2O7晶体(橙红色)的实验方案:水浸,过滤,___ ,烘干得Na2Cr2O7晶体(必须使用的试剂有:硫酸,蒸馏水)。
 已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。
已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。②Na2CrO4溶液中加酸调节pH为3.5时,CrO42-转化为Cr2O72-。
③相关物质在不同温度时溶解度如下表:
| 温度 溶解度/g 物质 | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 90℃ |
| Na2SO4 | 19.5 | 40.8 | 48.8 | 45.3 | 43.7 | 42.7 |
| Na2Cr2O7 | 183 | 198 | 215 | 269 | 376 | 405 |
(2)“过滤”前,适当加热的目的是
(3)对“过滤”所得的滤渣进行洗涤,检验滤渣已洗涤干净的方法是
(4)“过滤”时产生的滤渣可用于制备Na2Cr2O7晶体。
①滤渣经干燥后与Na2CO3混合在空气中煅烧生成Na2CrO4和CO2,此反应的化学方程式为
②请补充完整上述煅烧后混合物制备Na2Cr2O7晶体(橙红色)的实验方案:水浸,过滤,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】KNO3是重要的化工产品,下面是一种已获得专利的KNO3制备方法的主要步骤:
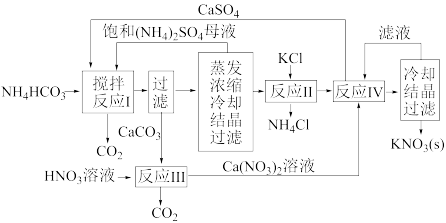
(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1∶2,该反应的化学方程式为________________ 。
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是_________________ 。从反应Ⅳ所得混合物中分离出CaSO4的方法是趁热过滤,趁热过滤的目的是______________________________ 。
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水,____________ 。
(4)整个循环流程中,需不断补充的原料除NH4HCO3外,还有____________ (填化学式)。

(1)反应Ⅰ中,CaSO4与NH4HCO3的物质的量之比为1∶2,该反应的化学方程式为
(2)反应Ⅱ需在干态、加热的条件下进行,加热的目的是
(3)检验反应Ⅱ所得K2SO4中是否混有KCl的方法是:取少量K2SO4样品溶解于水,
(4)整个循环流程中,需不断补充的原料除NH4HCO3外,还有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
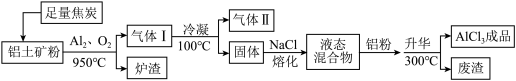
已知:
回答下列问题:
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是______ (只要求写出一种)。
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为_______ 。
(3)气体II的主要成分除了Cl2外,还含有_______ 。气体II常用过量冷的NaOH溶液吸收,吸收液中含有的阴离子主要有_______ 。
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是_______ 。
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl 和Al2Cl
和Al2Cl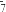 两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为_______ 。

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
(1)高温反应前,常在800℃焙烧铝土矿,使固体中水分挥发、气孔数目增多,其作用是
(2)高温反应后,铝土矿中的氧化物均转变为相应的氯化物,由Al2O3、C和Cl2反应生成AlCl3的化学方程式为
(3)气体II的主要成分除了Cl2外,还含有
(4)工业上为了降低生产成本,生产过程中需要控制加入铝粉的量,“废渣”的主要成分是
(5)AlCl3和NaCl的熔融盐常用于镀铝电解池,电镀时AlCl
 和Al2Cl
和Al2Cl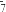 两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
两种离子在电极上相互转化,其它离子不参与电极反应,电镀时阴极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】水处理剂在生产生活中有重要的应用。
(1)聚合氯化铝晶体([Al2(OH)nCl6-n∙xH2O]m)是一种高效无机水处理剂,它的制备原理是通过调节增大A1C13溶液的pH,促进其水解而结晶析出。利用高岭土制备聚合氯化铝,其制备过程有如下两种途径:

说明:①高岭土的化学组成为:Al2O3、SiO2、Fe2O3及少量有机杂质和水分,
②高岭土在煅烧的过程中可除去有机杂质和水分。
①途径I和途径Ⅱ中最合理的是_________ 。
②途径I中加入铝粉最主要的目的是__________ (选填序号字母)。
a.中和过量的盐酸 b.将Fe3+还原为Fe2+
c.除去溶液中的铁元素 d.制备生成聚合氯化铝所需要的AlCl3
③加入碳酸钙调节溶液pH至4.0~4.5的目的是_______________________ 。
④蒸发浓缩过程中生成Al2(OH)nCl6-n∙xH2O的化学反应方程式是_______ 。
(2)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂。电解法制备Na2FeO4的装置如右图所示:

请根据图示回答:电解过程的化学方程式为_________ ;电路中每通过0.6 mol电子在Ni电极上产生的气体在标况下的体积为_________ ;隔膜应选择__________ (填“阳离子交换膜”或“阴离子交换膜”)。
(1)聚合氯化铝晶体([Al2(OH)nCl6-n∙xH2O]m)是一种高效无机水处理剂,它的制备原理是通过调节增大A1C13溶液的pH,促进其水解而结晶析出。利用高岭土制备聚合氯化铝,其制备过程有如下两种途径:

说明:①高岭土的化学组成为:Al2O3、SiO2、Fe2O3及少量有机杂质和水分,
②高岭土在煅烧的过程中可除去有机杂质和水分。
①途径I和途径Ⅱ中最合理的是
②途径I中加入铝粉最主要的目的是
a.中和过量的盐酸 b.将Fe3+还原为Fe2+
c.除去溶液中的铁元素 d.制备生成聚合氯化铝所需要的AlCl3
③加入碳酸钙调节溶液pH至4.0~4.5的目的是
④蒸发浓缩过程中生成Al2(OH)nCl6-n∙xH2O的化学反应方程式是
(2)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂。电解法制备Na2FeO4的装置如右图所示:

请根据图示回答:电解过程的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】氮化钙(Ca3N2)是一种重要的化工产品,遇水蒸气剧烈反应生成Ca(OH)2和NH3。某小组设计实验制备Ca3N2并探究其性质。先通过加热NaNO2溶液和饱和NH4Cl溶液的混合液制备N2,然后在加热条件下N2与Ca反应制得Ca3N2。
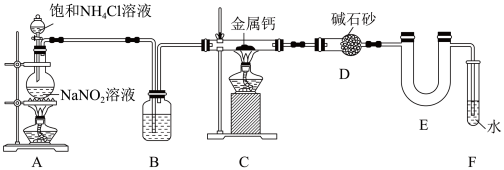
请回答下列问题:
(1)盛装 NaNO2溶液的仪器名称为_______ ;B装置中试剂是_______ (填名称)。
(2)写出A装置中发生反应的离子方程式:_______ 。
(3)实验过程中,先点燃_______ (填“A”或“C”,下同)处酒精灯,后点燃_______ 处酒精灯,这样操作的目的是_______ 。
(4)探究Ca3N2产品的性质。将Ca3N2产品溶于水中,根据题目信息,请写出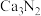 与水反应的化学方程式:
与水反应的化学方程式:_______ 。
(5)测定 Ca3N2产品(设杂质只有CaO)的纯度。取5.2g样品:溶于足量的水中,加入足量Na2CO3溶液,过滤、洗涤、干燥,称得固体质量为10g。该产品中Ca3N2的质量分数为_______ (保留三位有效数字)。

请回答下列问题:
(1)盛装 NaNO2溶液的仪器名称为
(2)写出A装置中发生反应的离子方程式:
(3)实验过程中,先点燃
(4)探究Ca3N2产品的性质。将Ca3N2产品溶于水中,根据题目信息,请写出
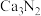 与水反应的化学方程式:
与水反应的化学方程式:(5)测定 Ca3N2产品(设杂质只有CaO)的纯度。取5.2g样品:溶于足量的水中,加入足量Na2CO3溶液,过滤、洗涤、干燥,称得固体质量为10g。该产品中Ca3N2的质量分数为
您最近一年使用:0次



