聚合硫酸铁[ ,Fe为+3价]是高效水处理剂。实验室用某冶金厂的废渣(主要成分为
,Fe为+3价]是高效水处理剂。实验室用某冶金厂的废渣(主要成分为 、
、 和少量
和少量 )制备聚合硫酸铁的流程如下:
)制备聚合硫酸铁的流程如下:
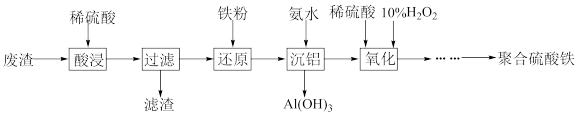
请回答下列问题:
(1)基态 核外电子排布式为
核外电子排布式为_______ ,“酸浸”时 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_______ 。
(2)“还原”后,检验溶液中是否还存在 的的试剂是
的的试剂是_______ 。
(3)不同金属离子生成氢氧化物开始沉淀和完全沉淀时的pH如下表所示:
①沉铝时应控制溶液pH的范围是_______ 。
②写出沉铝时反应的离子方程式:_______ 。
(4)聚合硫酸铁[ ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁溶于稀盐酸中,向所得溶液中滴加 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30g;
②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并,用0.500mol/L的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液32.00mL。该步反应为:
溶液32.00mL。该步反应为: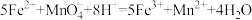 。
。
通过计算确定该聚合硫酸铁的化学式_______ (请写出计算过程)。
 ,Fe为+3价]是高效水处理剂。实验室用某冶金厂的废渣(主要成分为
,Fe为+3价]是高效水处理剂。实验室用某冶金厂的废渣(主要成分为 、
、 和少量
和少量 )制备聚合硫酸铁的流程如下:
)制备聚合硫酸铁的流程如下:
请回答下列问题:
(1)基态
 核外电子排布式为
核外电子排布式为 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(2)“还原”后,检验溶液中是否还存在
 的的试剂是
的的试剂是(3)不同金属离子生成氢氧化物开始沉淀和完全沉淀时的pH如下表所示:
| 金属阳离子 |  |  |  |
| 开始沉淀时的pH | 6.5 | 1.5 | 3.3 |
| 完全沉淀时的pH | 9.7 | 3.2 | 5.2 |
②写出沉铝时反应的离子方程式:
(4)聚合硫酸铁[
 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁溶于稀盐酸中,向所得溶液中滴加
 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30g;
溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体23.30g;②另称取与①等质量的聚合硫酸铁溶于稀硫酸中,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并,用0.500mol/L的
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液32.00mL。该步反应为:
溶液32.00mL。该步反应为: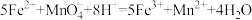 。
。通过计算确定该聚合硫酸铁的化学式
更新时间:2022-07-29 10:09:17
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如图:

试回答下列问题:
(1)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有__ 、玻璃棒和烧杯等;该步骤是为了除去___ (填相关物质的化学式)。
(2)检验步骤Ⅲ已经进行完全的操作是__ 。
(3)步骤V的反应温度一般需控制在35℃以下,其目的是___ ;该步骤中反应生成FeCO3的离子反应方程式为___ 。
(4)步骤Ⅵ中发生反应的化学反应方程式为___ 。
(5)欲测定硫铁矿矿渣中铁元素的质量分数,称取ag样品,充分“酸溶”“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中铁元素的质量分数为__ 。

试回答下列问题:
(1)实验室实现“步骤Ⅱ”中分离操作所用的玻璃仪器有
(2)检验步骤Ⅲ已经进行完全的操作是
(3)步骤V的反应温度一般需控制在35℃以下,其目的是
(4)步骤Ⅵ中发生反应的化学反应方程式为
(5)欲测定硫铁矿矿渣中铁元素的质量分数,称取ag样品,充分“酸溶”“水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中铁元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】一种用铝土矿和硫铁矿烧渣(配料中含Al2O3、Fe2O3、FeO及SiO2等)为原料制备无机高分子絮凝剂聚合碱式氯化铝铁的流程如下:

(1)配料中属于两性氧化物的是______ ,步骤Ⅱ酸溶时,Fe2O3被溶解的化学方程式为_____ 。
(2)“滤渣1”的主要成分为________ (填化学式),为检验“过滤1”后的溶液中是否含有Fe3+,可选用的化学试剂是_________ 。
(3)步骤Ⅳ加入H2O2溶液的目的是______ ,发生反应的离子方程式为__ 。
(4)步骤Ⅴ调节pH=3发生反应生成聚合碱式氯化铝铁,若溶液pH过大,可能造成的影响是_________ ;步骤Ⅵ包含的操作有过滤、________ 、干燥得到产品。
(5)测定聚合碱式氯化铝铁{可表示为[FeaAlb(OH)xCly]n}中n(Fe)/n(Al)的比值的步骤如下:
步骤1:准确称取产品5.710g溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体。
步骤2:另准确称取相同质量样品,溶于足量NaOH溶液,过滤,充分洗涤,将滤渣灼烧至质量不再变化,得到固体0.8000g。
计算产品中n(Fe)/n(Al)的比值。(写出计算过程)____________

(1)配料中属于两性氧化物的是
(2)“滤渣1”的主要成分为
(3)步骤Ⅳ加入H2O2溶液的目的是
(4)步骤Ⅴ调节pH=3发生反应生成聚合碱式氯化铝铁,若溶液pH过大,可能造成的影响是
(5)测定聚合碱式氯化铝铁{可表示为[FeaAlb(OH)xCly]n}中n(Fe)/n(Al)的比值的步骤如下:
步骤1:准确称取产品5.710g溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到3.350g固体。
步骤2:另准确称取相同质量样品,溶于足量NaOH溶液,过滤,充分洗涤,将滤渣灼烧至质量不再变化,得到固体0.8000g。
计算产品中n(Fe)/n(Al)的比值。(写出计算过程)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】工业上以软锰矿(主要成分为MnO2,还含有少量Fe2O3等)和辉铜矿(主要成分为Cu2S,还含有少量Si、Ni等氧化物)为原料,制备碳酸锰和胆矾的工艺流程如图所示。
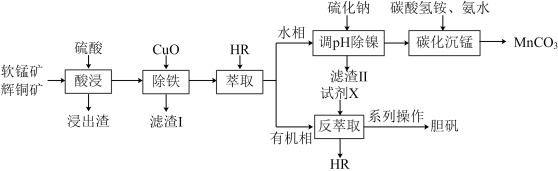
已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org) CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。
回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是________ (答出任意两条即可);已知浸出渣中含有单质S,写出“酸浸”时MnO2与Cu2S反应的离子方程式:________ 。
(2)得到“滤渣I”的操作:________ 。
(3)写出“碳化沉锰”过程中发生反应的离子方程式:________ 。
(4)试剂X为________ (填化学式);“系列操作”包括________ 、过滤、洗涤和干燥。

已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org)
 CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是
(2)得到“滤渣I”的操作:
(3)写出“碳化沉锰”过程中发生反应的离子方程式:
(4)试剂X为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】碳酸铈[Ce2(CO3)3]为白色粉末,难溶于水,主要用作生产铈的中间化合物。它可由氟碳酸铈精矿经如下流程。
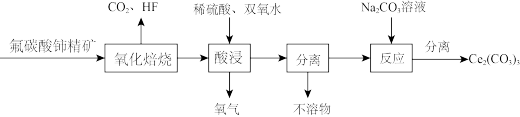
(1)氟碳酸铈的化学式为为CeFCO3,该化合物中,Ce的化合价为_____________ 。
(2)氧化焙烧生成的铈化合物为二氧化铈(CeO2),其在酸浸时发生反应的离子方程式为___________ 。
(3)试剂X是________________ 。
(4)若试剂X改为氢氧化钠溶液,则反应生成难溶物—一氢氧化铈(Ⅲ),其暴露于空气中时变成紫色,最终变成黄色的氢氧化高铈(Ⅳ)。氢氧化铈在空气中被氧化成氢氧化高铈的化学方程式为__________________________________________________ 。
(5)取(4)中得到的Ce(OH)4产品(质量分数为97%)1. 00 g,加硫酸溶解后,用0.1000mol·L-1的FeSO4溶液滴定至终点(铈被还原成Ce3+),则需要滴加标准溶液的体积为_________ mL。

(1)氟碳酸铈的化学式为为CeFCO3,该化合物中,Ce的化合价为
(2)氧化焙烧生成的铈化合物为二氧化铈(CeO2),其在酸浸时发生反应的离子方程式为
(3)试剂X是
(4)若试剂X改为氢氧化钠溶液,则反应生成难溶物—一氢氧化铈(Ⅲ),其暴露于空气中时变成紫色,最终变成黄色的氢氧化高铈(Ⅳ)。氢氧化铈在空气中被氧化成氢氧化高铈的化学方程式为
(5)取(4)中得到的Ce(OH)4产品(质量分数为97%)1. 00 g,加硫酸溶解后,用0.1000mol·L-1的FeSO4溶液滴定至终点(铈被还原成Ce3+),则需要滴加标准溶液的体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】“钢是虎,钒是翼,钢含钒犹如虎添翼”,金属钒被誉为“合金的维生素”。从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示: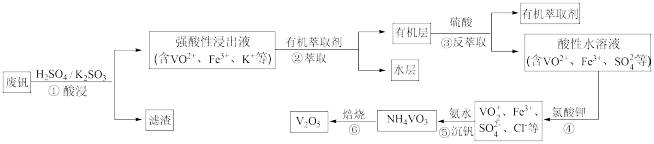
已知:步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)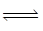 RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
回答下列问题:
(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为______________ 。
(2)萃取时应加入适量碱的作用是___________________ 。
(3)步骤④中反应的离子方程式为___________________ 。
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
通过表中数据分析,在实际生产中,⑤中加入氨水,调节溶液的最佳pH范围为______ ;
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<_____ mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为VO+,则V2O5与氢碘酸反应的离子方程式为_________________ 。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=_______ mol/L(萃取率=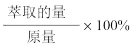 )
)

已知:步骤②、③中的变化过程可简化为:Rn+(水层)+nHA(有机层)
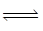 RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。
RAn(有机层)+nH+(水层)(式中Rn+表示VO2+或Fe3+,HA表示有机萃取剂)。回答下列问题:
(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为
(2)萃取时应加入适量碱的作用是
(3)步骤④中反应的离子方程式为
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3+)<
(5)V2O5是两性氧化物,在强酸性溶液中以VO2+形式存在,VO2+具有强氧化性,能将I-氧化为I2,本身被还原为VO+,则V2O5与氢碘酸反应的离子方程式为
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2+)=amol/L,步骤②和③每进行一次,VO2+萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2+)=
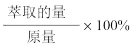 )
)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】苯胺是一种重要精细化工原料,在染料、医药等行业中具有广泛的应用。
(1)实验室以苯为原料制取苯胺,其原理简示如下:
第一步:______ ;
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。______ ;
②下列说法中正确的是______ (填字母);
A.浓硫酸可以降低该反应活化能
B.温度控制在50~60℃原因之一是减少副反应的发生
C.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
③粗硝基苯用5%NaOH溶液洗涤的目的是______ ;
(3)制取苯胺
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
步骤3:______ 。
步骤4:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
步骤5:______ ,得到较纯苯胺。
①补充完善步骤3和步骤5的相关实验操作。
②步骤4中,加入生石灰的作用是______ ;
| 物质 | 相对分子质量 | 沸点℃ | 密度g/mL | 溶解性 |
| 硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化 |
(1)实验室以苯为原料制取苯胺,其原理简示如下:
第一步:
第二步: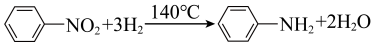
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。

②下列说法中正确的是
A.浓硫酸可以降低该反应活化能
B.温度控制在50~60℃原因之一是减少副反应的发生
C.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
③粗硝基苯用5%NaOH溶液洗涤的目的是
(3)制取苯胺
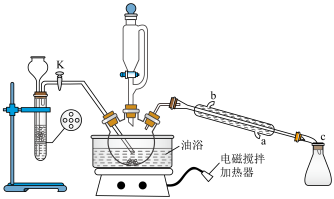
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计。
步骤3:
步骤4:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。
步骤5:
①补充完善步骤3和步骤5的相关实验操作。
②步骤4中,加入生石灰的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】三氯氧磷(POCl3)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化PCl3制备POCl3,反应原理为:P4(白磷)+6Cl2=4PCl3,2PCl3+O2=2POCl3。
已知:PCl3、POCl3的部分性质如下:
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):
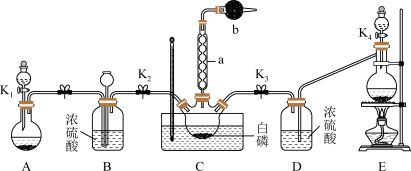
(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器a的名称为_______ ,b中盛放的药品是_______ 。
(2)装置E反应的离子方程式为_______ 。
(3)C反应温度控制在60~65℃,不能过高或过低的原因是_______ 。分离提纯获得POCl3的实验方法是_______ 。
(4)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入Comol/L-1的AgNO3溶液V0mL,使Cl-完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3),指示剂,用c1mol/L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为V1mL。
[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12]
滴定终点的现象:_______ 。实验过程中加入硝基苯的目的是_______ ,若无此操作,则所测POCI3的含量将_______ (填“偏高”“偏低”或“不变”)。
(5)产品中POCl3的质量分数为_______ 。
已知:PCl3、POCl3的部分性质如下:
| 熔点/℃ | 沸点/℃ | 相对分子质量 | 其它 | |
| PCl3 | -112 | 75.5 | 137.5 | 遇水生成H3PO3和HCl |
| POCl3 | 2 | 105.3 | 153.5 | 遇水生成H3PO4和HCl |

(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器a的名称为
(2)装置E反应的离子方程式为
(3)C反应温度控制在60~65℃,不能过高或过低的原因是
(4)通过测定三氯氧磷产品中氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取ag产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入Comol/L-1的AgNO3溶液V0mL,使Cl-完全沉淀,再加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3),指示剂,用c1mol/L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积为V1mL。
[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12]
滴定终点的现象:
(5)产品中POCl3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】过二硫酸盐[例:(NH4)2S2O8、Na2S2O8]都具有强氧化性,可作氧化剂和漂白剂,(NH4)2S2O8被广泛用于蓄电池工业,在照相工业上用来除去海波。
I:(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。

(1)仪器a的名称是_______ ,b的作用是_______ ,试剂X为_______ (填名称)。
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是_______ 。
(3)烘干产品时,用红外灯低温烘干,可能的原因是_______ 。
Ⅱ:(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下, 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为_______ mol。过二硫酸铵可用于检验废水中的Cr3+是否超标,如果超标,溶液会变成橙色(还原产物为 ),写出该反应的离子方程式:
),写出该反应的离子方程式:_______ 。
Ⅲ:标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的:(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为_______ ,所标定的(NH4)2S2O8的浓度为_______ mol·L-1.
I:(NH4)2S2O8的制备原理为H2O2+2H2SO4+2NH3=(NH4)2S2O8+2H2O。实验室模拟制备(NH4)2S2O8的装置如图所示。

(1)仪器a的名称是
(2)充分反应后,将B中混合液经一系列操作得到晶体,用无水乙醚洗涤,目的是
(3)烘干产品时,用红外灯低温烘干,可能的原因是
Ⅱ:(NH4)2S2O8的性质及应用。
(4)过二硫酸(H2S2O8)是一种强氧化性酸,在Ag+催化作用下,
 能与Mn2+在水溶液中发生反应生成
能与Mn2+在水溶液中发生反应生成 和
和 ,1mol
,1mol 能氧化的Mn2+的物质的量为
能氧化的Mn2+的物质的量为 ),写出该反应的离子方程式:
),写出该反应的离子方程式:Ⅲ:标定(NH4)2S2O8溶液的浓度。
(5)称取一定质量的:(NH4)2S2O8,配制成溶液,并用碘量法标定该溶液的浓度,移取20.00mL(NH4)2S2O8溶液于锥形瓶中,加入过量的KI,然后加入几滴淀粉溶液,再用0.1mol·L-1的Na2S2O3溶液滴定,发生反应:I2+2
 =2I-+
=2I-+ 。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
。重复上述操作三次,平均消耗Na2S2O3溶液的体积为18.40mL,滴定终点时的颜色变化为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】氯化亚砜(SOCl2)具有较强的巯基和羟基取代能力,广泛应用于有机合成中。工业上可以利用SO3与SCl2反应制得,装置如下图所示(夹持及加热装置已略去):

物质的相关性质如下表:
已知:H2SO4(浓) SO3+H2O;SCl2与SOCl2互溶。
SO3+H2O;SCl2与SOCl2互溶。
实验步骤如下:
①通入干燥的氮气(能够抑制三氧化硫气体逸出),观察A中气泡控制N2的流速;
②将P2O5固体置于烧瓶B中,向B中分多次缓慢加入5.44mL浓硫酸(密度为1.84g· cm-3,质量分数为98%),再向C中加入足量SCl2;
③冷凝管接入冷凝水后将烧瓶B升温至225℃,三氧化硫液体缓慢流入锥形瓶C中;
④反应完成后取下锥形瓶C,……(操作),得到高纯SOCl2产物。
回答下列问题:
(1)仪器a的名称为_______ ,锥形瓶C中生成氯化亚砜的方程式为_______ 。
(2)该制备SOCl2装置存在的缺陷为_______ 。
(3)实验步骤④中的操作为_______ (填名称)。
(4)将得到的SOCl2溶于水生成两种酸,反应的离子方程式为_______ ,取所得溶液体积的十分之一用0.5mol·L-1标准碘溶液滴定,选用_______ 做指示剂,滴定终点消耗标准碘溶液的体积为13.00mL,则SOCl2的产率为_______ ,若滴定后,滴定管尖嘴处有气泡,则测定结果_______ (填“偏高”“偏低”或“不变”)。

物质的相关性质如下表:
| 物质 | SO3 | SCl2 | SOCl2 |
| 熔点/℃ | 16.8 | -78 | -105 |
| 沸点/℃ | 44.8 | 60 | 78.8 |
| 与水反应 | 均能与水剧烈反应 | ||
 SO3+H2O;SCl2与SOCl2互溶。
SO3+H2O;SCl2与SOCl2互溶。实验步骤如下:
①通入干燥的氮气(能够抑制三氧化硫气体逸出),观察A中气泡控制N2的流速;
②将P2O5固体置于烧瓶B中,向B中分多次缓慢加入5.44mL浓硫酸(密度为1.84g· cm-3,质量分数为98%),再向C中加入足量SCl2;
③冷凝管接入冷凝水后将烧瓶B升温至225℃,三氧化硫液体缓慢流入锥形瓶C中;
④反应完成后取下锥形瓶C,……(操作),得到高纯SOCl2产物。
回答下列问题:
(1)仪器a的名称为
(2)该制备SOCl2装置存在的缺陷为
(3)实验步骤④中的操作为
(4)将得到的SOCl2溶于水生成两种酸,反应的离子方程式为
您最近一年使用:0次



