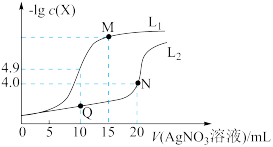
t℃时,将0.1 mol·L-1AgNO3溶液分别滴加到10. 00 mL0.1 mol·L-1KCl、10.00 ml0.1 mol· L-1K2CrO4溶液中,AgNO3溶液体积(V)与-lg c(X)(X为Cl-或 )的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 )的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
)的变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
| A.曲线L2表示-lg c(Cl-)与V(AgNO3溶液)的变化关系 |
| B.t℃时,铬酸银的溶度积常数为4.0 ×10-12 |
| C.若仅将c(K2CrO4)改为0.05 mol·L-1,则曲线L2中N点移到Q点 |
D.M点溶液中:c( )>c(K+ )>c(Ag+ )>c(OH- )>c(H+ ) )>c(K+ )>c(Ag+ )>c(OH- )>c(H+ ) |
更新时间:2022-08-10 17:28:25
|
【知识点】 难溶电解质的溶解平衡
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列操作中不存在水解平衡过程的是
| A.用泡沫灭火器灭火 |
| B.实验室保存FeCl3溶液时,加入稀HCl溶液 |
| C.用稀H2SO4溶液溶解固体FeS |
| D.向Mg(OH)2沉淀中滴加NH4Cl溶解,使其溶解 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在平衡体系Ca(OH)2(s) Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
 Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是| A.加入少量MgCl2固体 | B.加入少量Na2CO3固体 |
| C.加入少量KCl固体 | D.加入少量稀H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7;p(Ni)=-lgc(Ni2+),p(B)=-lgc(S2-)或-lgc(CO32-)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示(已知两种沉淀的溶解度随温度升高而增大)。下列说法错误的是( )
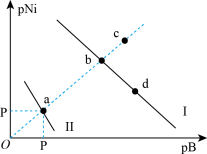

| A.常温下NiCO3的溶解度大于NiS的溶解度 |
| B.向d点对应的溶液中加入Na2S固体,d点向b点移动 |
| C.对于曲线I,在b点加热,b点向c点移动 |
| D.P为3.5且对应的阴离子是CO32- |
您最近一年使用:0次



