关于CS2,SO2,NH3三种物质的说法中正确的是
| A.CS2在水中的溶解度很小,是由于其属于极性分子 |
| B.NH3在水中溶解度很大只是由于NH3分子有极性 |
| C.CS2为非极性分子,所以在三种物质中熔沸点最低 |
| D.SO2和NH3均易溶于水,原因之一是它们都是极性分子 |
更新时间:2022-04-06 13:45:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】臭氧通常存在于距离地面25km左右的高层大气中,它能有效阻挡紫外线,保护人类健康。但是在近地面,臭氧却是一种污染物。已知O3的空间结构为V形,分子中正电中心和负电中心不重合。下列说法不正确的是
| A.O3和O2互为同素异形体 | B.在水中的溶解度:O3>O2 |
| C.O3是极性分子,O2是非极性分子 | D.O3分子中的共价键是非极性键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】肼(H2N-NH2)和偏二甲肼[H2N-N(CH3)2]均可用作火箭燃料。查阅资料得知,肼是一种良好的极性溶剂,沿肼分子球棍模型的N—N键方向观察,看到的平面图如下图所示。下列说法不正确的是


| A.肼分子中的氮原子采用sp3杂化 | B.肼分子中既有极性键又有非极性键 |
| C.肼分子是非极性分子 | D.肼与偏二甲肼互称同系物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法不正确的是
| A.HCl、HBr、HI的熔点沸点升高与范德华力大小有关 |
| B.H2O的熔点沸点大于H2S的是由于H2O分子之间存在氢键 |
| C.乙醇与水互溶可以用相似相溶原理解释 |
| D.甲烷与水分子间不能形成氢键这种化学键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中正确的是( )
| A.NO2、SO2、BF3、NCl3分子中没有一个分子的原子最外层电子都满足8电子稳定结构 |
| B.P4和CH4都是正四面体分子且键角都为109°28′ |
C.NH4+的电子式为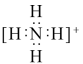 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
| D.用CCl4提取碘水中的碘单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法不正确的是
①N2H4分子中既含极性键又含非极性键
②F2、Cl2、Br2、I2熔点逐渐增大
③NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
④固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑤HF分子很稳定是由于HF分子之间能形成氢键
①N2H4分子中既含极性键又含非极性键
②F2、Cl2、Br2、I2熔点逐渐增大
③NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
④固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑤HF分子很稳定是由于HF分子之间能形成氢键
| A.③⑤ | B.②⑤ | C.④⑤ | D.①②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】前四周期主族元素X、Y、Z、W的原子序数依次增大,它们形成的一种物质的结构如图所示,其中所有原子都形成了8电子稳定结构,四种元素中仅X、Y在同周期。下列推断中错误的是
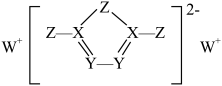

A.简单离子半径: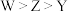 | B. 分子的空间构型为直线形 分子的空间构型为直线形 |
C.最简单氢化物的沸点: | D.Y与氧元素形成的化合物不止3种 |
您最近一年使用:0次

 和
和
 和
和
 和
和
 和
和







