下列各组物质中,都是由极性键构成的极性分子的是
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
更新时间:2024-03-23 14:49:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】研究发现一种关于电催化氮活化制氨的方法,由于不同的氢化顺序,反应历程可分为远端路径和交替路径,反应机理如图所示(cat表示有机酶催化剂),下列说法错误的是
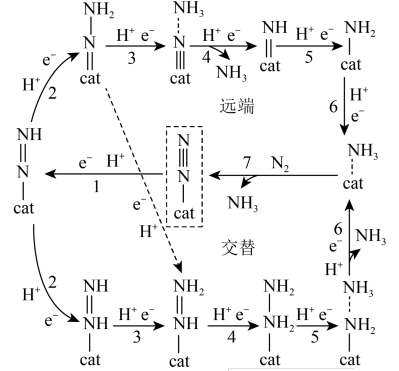
| A.在交替路径中,两个氮原子将交替进行氢化反应 |
B. 和 和 中两端氮原子均可能优先进行氢化反应 中两端氮原子均可能优先进行氢化反应 |
| C.反应过程中存在非极性键的断裂与生成 |
D.反应历程的总反应为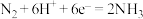 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示K2S的形成: |
| B.用离子方程式表示A1(OH)3溶于烧碱溶液:Al(OH)3+OH-=[Al(OH)4]- |
C.用电子云轮廓图表示H-H的s-sσ键形成示意图: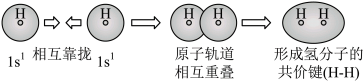 |
D.用球棍模型表示H2O的分子构型: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M、Q五种短周期元素,原子序数依次增大。X只有1个 能级的电子。
能级的电子。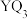 是一种平面正三角形分子。Z的p能级电子半充满。M元素焰色试验焰色呈黄色。下列说法不正确的是
是一种平面正三角形分子。Z的p能级电子半充满。M元素焰色试验焰色呈黄色。下列说法不正确的是
 能级的电子。
能级的电子。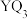 是一种平面正三角形分子。Z的p能级电子半充满。M元素焰色试验焰色呈黄色。下列说法不正确的是
是一种平面正三角形分子。Z的p能级电子半充满。M元素焰色试验焰色呈黄色。下列说法不正确的是A.电负性: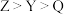 ,第一电离能:M>Z>Y ,第一电离能:M>Z>Y |
B.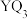 与 与 能通过配位键化合 能通过配位键化合 |
C. 是分子晶体,结构与苯相似 是分子晶体,结构与苯相似 |
D. 是一种离子化合物,溶于水能放出氢气 是一种离子化合物,溶于水能放出氢气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W、R为核电荷数依次增大的五种短周期元素。下列说法不正确的是


| 元素 | 元素性质或原子结构 |
| X | 电子只有一种自旋取向 |
| Y | 基态原子的最外层有2个未成对电子,次外层有2个电子 |
| Z | 基态原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| W | 基态原子最高能层的上的电子数是电子层数的2倍 |
| R | 基态原子只有一个未成对电子 |
| A.由于Y2X4分子中的π键不如σ键稳定,所以Y2X4易与氢气发生加成反应 |
| B.YZR2分子中Y原子的杂化类型为sp2,分子中有1个π键,分子空间构型为平面三角形 |
| C.如图为Y的某种单质的晶胞,每个Y原子均处于其它4个与之相邻的Y原子围成的正四面体的空隙处 |
| D.X2Z比X2W更稳定,是由于X2Z分子之间存在氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于物质结构的命题中,错误的个数为
① 中碳原子的杂化类型有
中碳原子的杂化类型有 和
和 两种
两种
②元素Ge位于周期表第四周期ⅣA族,核外电子排布式为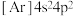 ,属于p区元素
,属于p区元素
③非极性分子往往具有高度对称性,如 、
、 、
、 、
、 这样的分子
这样的分子
④ 、
、 中阴、阳离子个数比不同
中阴、阳离子个数比不同
⑤氨水中大部分 与
与 以氢键(用“∙∙∙”表示)结合成
以氢键(用“∙∙∙”表示)结合成 ,根据氨水的性质可知
,根据氨水的性质可知 的结构式可写为
的结构式可写为
⑥HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
①
 中碳原子的杂化类型有
中碳原子的杂化类型有 和
和 两种
两种②元素Ge位于周期表第四周期ⅣA族,核外电子排布式为
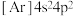 ,属于p区元素
,属于p区元素③非极性分子往往具有高度对称性,如
 、
、 、
、 、
、 这样的分子
这样的分子④
 、
、 中阴、阳离子个数比不同
中阴、阳离子个数比不同⑤氨水中大部分
 与
与 以氢键(用“∙∙∙”表示)结合成
以氢键(用“∙∙∙”表示)结合成 ,根据氨水的性质可知
,根据氨水的性质可知 的结构式可写为
的结构式可写为
⑥HF晶体沸点高于HCl,是因为HCl共价键键能小于HF
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】六氟化硫(SF6)分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是( )

| A.SF6各原子均达到最外层8电子稳定结构 |
| B.SF6易燃烧生成SO2 |
| C.SF6分子是含有极性键的非极性分子 |
| D.SF6是原子晶体 |
您最近一年使用:0次

 代表阿伏加德罗常数的数值。下列说法中,正确的是
代表阿伏加德罗常数的数值。下列说法中,正确的是 碳酸钠和碳酸氢钠的混合物含有的氧原子数为
碳酸钠和碳酸氢钠的混合物含有的氧原子数为
 乙炔中
乙炔中 键数为
键数为 键数为
键数为
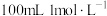 醋酸溶液中含有的氢离子数为
醋酸溶液中含有的氢离子数为
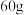 二氧化硅晶体中含有
二氧化硅晶体中含有 键数为
键数为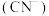 和
和 的结构:氰离子:
的结构:氰离子: 氰:
氰: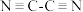 下列说法
下列说法 中N为负价
中N为负价 键
键 分子中的4个原子在一条直线上
分子中的4个原子在一条直线上

