 、
、 都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是
都是造成水体污染的因素,可以利用沉淀法除去。如图a、b分别是Mg3(AsO4)2、Mg3(PO4)2的沉淀溶解平衡曲线。下列说法错误的是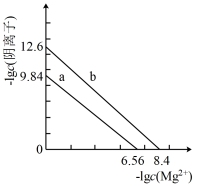
| A.Ksp[Mg3(AsO4)2]=10-19.68 |
B.若Mg3(AsO4)2(s)+2 (aq) (aq) Mg3(PO4)2(s)+2 Mg3(PO4)2(s)+2 (aq)成立,则平衡常数K=104.52 (aq)成立,则平衡常数K=104.52 |
C.向浓度相等的Na3AsO4、Na3PO4的废水中同时滴加相同浓度的Mg(NO3)2溶液, 先沉淀 先沉淀 |
D.要使废水中 、 、 离子浓度不大于10-6mol·L-1,则Mg2+浓度至少为10-2.56mol·L-1 离子浓度不大于10-6mol·L-1,则Mg2+浓度至少为10-2.56mol·L-1 |
更新时间:2022-04-06 12:52:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】t℃时,AgBr在水中的沉淀溶解平衡曲线如图。又知t℃时AgCl的Ksp=4.9×10-10,下列说法不正确的是( )
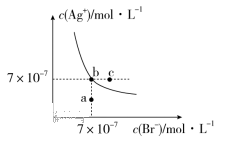

| A.图中a点对应的是AgBr的不饱和溶液 |
| B.在t℃时,Ksp(AgBr)=4.9×10-13 |
C.在t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K=1000 AgBr(s)+Cl-(aq)的平衡常数K=1000 |
| D.在AgBr的饱和溶液中加入NaBr固体,可使溶液由b点到c点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】二氧化碳的过量排放可对海洋环境造成影响,原理如图所示。下列叙述错误的是


A.海水酸化引起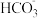 浓度增大 浓度增大 |
| B.海水酸化促进CaCO3的溶解、珊瑚礁减少 |
C.CO2引起海水酸化主要因为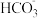  H++ H++ |
| D.使用太阳能等新能源有利于改善海洋环境 |
您最近一年使用:0次
【推荐1】25°C时,-1gc(X)与pH的关系如图所示,X代表Zn2+或Fe2+或 ,下列说法正确的是
,下列说法正确的是

已知:常温下,Fe(OH)2的Ksp=-8.1×10-16;强碱性溶液中Zn元素主要以 的形式存在。
的形式存在。
 ,下列说法正确的是
,下列说法正确的是
已知:常温下,Fe(OH)2的Ksp=-8.1×10-16;强碱性溶液中Zn元素主要以
 的形式存在。
的形式存在。| A.曲线②代表-lgc(Zn2+)与pH的关系 |
| B.常温下,Zn(OH)2的Ksp的数量级为10-18 |
| C.向等浓度的ZnCl2和FeCl2的混合溶液中滴入NaOH溶液,Zn2+先沉淀 |
D.向c[ ]=0.1mol·L-1的溶液中加入等体积0.1mol·L-1的HCl后,体系中Zn元素只以Zn(OH)2的形式存在 ]=0.1mol·L-1的溶液中加入等体积0.1mol·L-1的HCl后,体系中Zn元素只以Zn(OH)2的形式存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列离子方程式或电极反应式正确且符合题意的是
A.以铁为电极,电解熔融 ,阳极反应式: ,阳极反应式: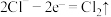 |
B.向 白色浊液中滴加 白色浊液中滴加 溶液产生黑色沉淀: 溶液产生黑色沉淀: |
C. 溶液中, 溶液中, 水解方程式: 水解方程式: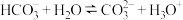 |
D.向含苯酚钠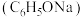 的废水中通入少量 的废水中通入少量 ,溶液变浑浊: ,溶液变浑浊: |
您最近一年使用:0次



