为验证氧化性 ,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
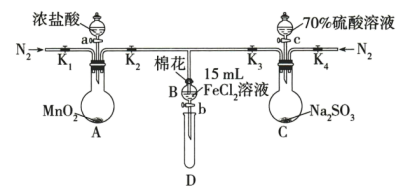
实验过程:
Ⅰ.打开止水夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1,K3,K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸溶液,一段时间后关闭K3。
Ⅵ.更换试管D,重复过程Ⅳ,检验B中溶液的离子。
(1)过程Ⅰ的目的是_______ 。
(2)若向过程ⅢB中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式:_______ 。
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为_______ 。
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性 的是
的是_______ (填“甲”“乙”或“丙”)。
(5)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入22.4LCl2(标准状况下),若溶液中有1/2的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_______ 。
 ,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。
实验过程:
Ⅰ.打开止水夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1,K3,K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸溶液,一段时间后关闭K3。
Ⅵ.更换试管D,重复过程Ⅳ,检验B中溶液的离子。
(1)过程Ⅰ的目的是
(2)若向过程ⅢB中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式:
(3)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(4)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性
 的是
的是| 过程为Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有 |
| 丙 | 有Fe3+无Fe2+ | 有 |
21-22高一·全国·单元测试 查看更多[1]
更新时间:2022-08-17 16:03:26
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
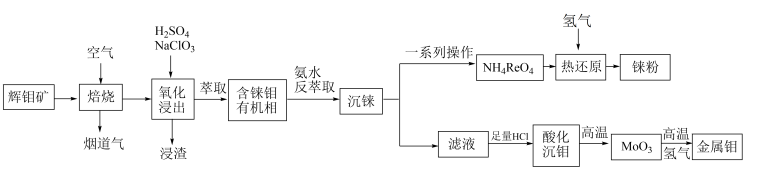
【推荐1】钼和铼都是过渡金属,钼可用来生产特种钢,是电子工业的重要材料,铼是国家战略紧缺资源,是制造航空发动机的关键金属。铼资源常与钼资源伴生,一种从辉钼矿[主要成分有 、
、 及少量铁、铜、硅化合物]中提取钼和铼的工艺流程如图所示:
及少量铁、铜、硅化合物]中提取钼和铼的工艺流程如图所示:
已知:Ⅰ.“焙烧”后的烟道灰主要成分有: 、
、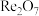 、
、 、
、 、CuO、
、CuO、 ;
;
Ⅱ.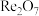 易溶于水,溶于水生成一元强酸高铼酸;
易溶于水,溶于水生成一元强酸高铼酸;
Ⅲ.高铼酸铵微溶于冷水,易溶于热水。
(1)“焙烧”过程中采用“多层逆流(空气从炉底进入,辉钼矿经粉碎后从炉顶进入)焙烧”,其优点是___________ 。
(2)烟道气成分除氮气外主要还有___________ 。
(3)氧化浸出过程中 反应的离子方程式为
反应的离子方程式为___________ 。
(4)“沉铼”时,为使沉淀充分析出并分离得到纯净的 晶体,“一系列操作”包括
晶体,“一系列操作”包括___________ 、___________ 、洗涤、干燥。
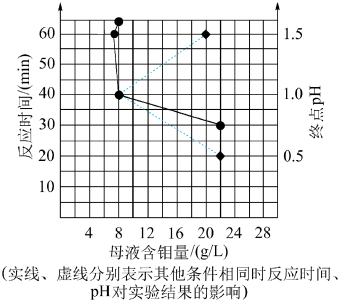
(5)“酸化沉钼”过程溶液终点pH和反应时间对钼酸的析出有很大影响,根据图中数据判断最佳的“酸化沉钼”条件:反应时间为___________ min;终点pH为___________ 。
(6)钼精矿的应用非常广泛,可以制备无公害型冷却水系统金属缓蚀剂钼酸钠晶体( )。在制备过程中需加入
)。在制备过程中需加入 固体除去
固体除去 ,若溶液中
,若溶液中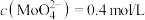 ,
, ,常温下,当
,常温下,当 即将开始沉淀时,
即将开始沉淀时, 的去除率为
的去除率为___________ [忽略溶液体积变化。已知:常温下,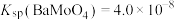 ,
,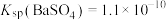 ]。
]。
 、
、 及少量铁、铜、硅化合物]中提取钼和铼的工艺流程如图所示:
及少量铁、铜、硅化合物]中提取钼和铼的工艺流程如图所示:
已知:Ⅰ.“焙烧”后的烟道灰主要成分有:
 、
、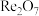 、
、 、
、 、CuO、
、CuO、 ;
;Ⅱ.
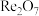 易溶于水,溶于水生成一元强酸高铼酸;
易溶于水,溶于水生成一元强酸高铼酸;Ⅲ.高铼酸铵微溶于冷水,易溶于热水。
(1)“焙烧”过程中采用“多层逆流(空气从炉底进入,辉钼矿经粉碎后从炉顶进入)焙烧”,其优点是
(2)烟道气成分除氮气外主要还有
(3)氧化浸出过程中
 反应的离子方程式为
反应的离子方程式为(4)“沉铼”时,为使沉淀充分析出并分离得到纯净的
 晶体,“一系列操作”包括
晶体,“一系列操作”包括(5)“酸化沉钼”过程溶液终点pH和反应时间对钼酸的析出有很大影响,根据图中数据判断最佳的“酸化沉钼”条件:反应时间为

(6)钼精矿的应用非常广泛,可以制备无公害型冷却水系统金属缓蚀剂钼酸钠晶体(
 )。在制备过程中需加入
)。在制备过程中需加入 固体除去
固体除去 ,若溶液中
,若溶液中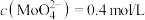 ,
, ,常温下,当
,常温下,当 即将开始沉淀时,
即将开始沉淀时, 的去除率为
的去除率为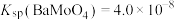 ,
,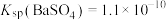 ]。
]。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
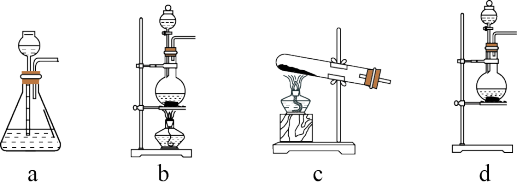
【推荐2】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体。某研究小组用下图所示的实验装置,利用浓氨水、干冰等作原料制备氨基甲酸铵。
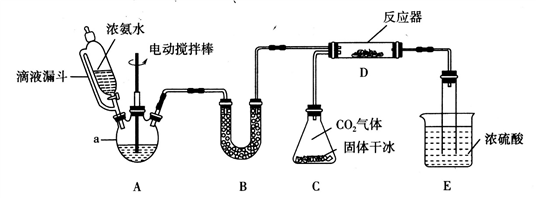
(1)仪器a的名称是____________ ;与分液漏斗相比,使用滴液漏斗的优点是:______________________________________ 。
(2)装置B中盛装药品的名称是________________ 。
(3)写出装置D中发生反应的化学方程式:__________________________________ 。
(4)装置E的作用之一是控制原料气按反应计量系数充分反应。若反应初期观察到装置内浓硫酸中产生气泡,应该______ (填“加快”、“减慢”或“不改变”)产生氨气的流速;装置E的作用还有___________________________________________________ 。
(5)已知氨基甲酸铵可完全水解为碳酸氢铵。为测定氨基甲酸铵样品的纯度,取样品1.600g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000g。
①写出碳酸氢铵与足量石灰水反应的离子方程式:______________________________ 。
②样品中氨基甲酸铵的质量分数为_____________ %。

(1)仪器a的名称是
(2)装置B中盛装药品的名称是
(3)写出装置D中发生反应的化学方程式:
(4)装置E的作用之一是控制原料气按反应计量系数充分反应。若反应初期观察到装置内浓硫酸中产生气泡,应该
(5)已知氨基甲酸铵可完全水解为碳酸氢铵。为测定氨基甲酸铵样品的纯度,取样品1.600g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000g。
①写出碳酸氢铵与足量石灰水反应的离子方程式:
②样品中氨基甲酸铵的质量分数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】按要求完成下列问题。
(1)某温度(t℃)时水的图象如图所示,a点离子积K=_______ ,在该温度下, 的溶液显
的溶液显_______ 性(填“酸”“碱”或“中”);在该温度下,将 的苛性钠溶液V1L与
的苛性钠溶液V1L与 的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
_______ 。

(2)25℃时,向 氨水中加入少量
氨水中加入少量 固体,当固体溶解后,测得溶液pH会
固体,当固体溶解后,测得溶液pH会_______ 。(填“增大”“减小”或“不变”)
(3)25℃时,等浓度的 溶液和
溶液和 溶液等体积混合,
溶液等体积混合, ,则混合溶液中各种离子浓度大小关系为
,则混合溶液中各种离子浓度大小关系为_______ 。
(4)已知:HClO的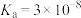 ,
, 的
的 ,
, ,写出往NaClO溶液中通入少量
,写出往NaClO溶液中通入少量 的离子方程式:
的离子方程式:_______ 。
(1)某温度(t℃)时水的图象如图所示,a点离子积K=
 的溶液显
的溶液显 的苛性钠溶液V1L与
的苛性钠溶液V1L与 的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则

(2)25℃时,向
 氨水中加入少量
氨水中加入少量 固体,当固体溶解后,测得溶液pH会
固体,当固体溶解后,测得溶液pH会(3)25℃时,等浓度的
 溶液和
溶液和 溶液等体积混合,
溶液等体积混合, ,则混合溶液中各种离子浓度大小关系为
,则混合溶液中各种离子浓度大小关系为(4)已知:HClO的
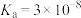 ,
, 的
的 ,
, ,写出往NaClO溶液中通入少量
,写出往NaClO溶液中通入少量 的离子方程式:
的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】次氯酸(HClO)消毒液高效安全,适用于一般物体表面消毒、手部消毒,以及地面、空间和环境消毒。如图,在装置D中制得颜色类似于氯气的 气体,装置E中得到次氯酸(HClO),已知
气体,装置E中得到次氯酸(HClO),已知 气体在42℃以上会发生分解,与水反应生成HClO。
气体在42℃以上会发生分解,与水反应生成HClO。
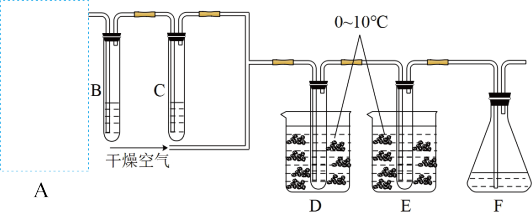
(1)图中,装置A是采用 与浓盐酸反应制取氯气的装置,则装置A中发生反应的化学方程式为
与浓盐酸反应制取氯气的装置,则装置A中发生反应的化学方程式为_______ ,装置A为_______ (填标号),
(2)在实验室通过 与浓盐酸常温下反应也可制取氯气,据此推
与浓盐酸常温下反应也可制取氯气,据此推 、
、 、
、 三种物质的氧化性由强到弱的顺序为
三种物质的氧化性由强到弱的顺序为_______ (用化学式表示),
(3)装置B的作用为除去HCl气体,则其中盛装的试剂的名称为_______ ;装置C中盛装的试剂为浓硫酸,其作用为_______ 。
(4)装置F中盛装的试剂为NaOH溶液,则装置F中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)实验时,需持续通入干燥的空气,其体积大约是氯气的3倍,主要作用是_______ ,同时通过气流降低温度,抑制 的分解,保证实验安全。
的分解,保证实验安全。
 气体,装置E中得到次氯酸(HClO),已知
气体,装置E中得到次氯酸(HClO),已知 气体在42℃以上会发生分解,与水反应生成HClO。
气体在42℃以上会发生分解,与水反应生成HClO。
(1)图中,装置A是采用
 与浓盐酸反应制取氯气的装置,则装置A中发生反应的化学方程式为
与浓盐酸反应制取氯气的装置,则装置A中发生反应的化学方程式为
(2)在实验室通过
 与浓盐酸常温下反应也可制取氯气,据此推
与浓盐酸常温下反应也可制取氯气,据此推 、
、 、
、 三种物质的氧化性由强到弱的顺序为
三种物质的氧化性由强到弱的顺序为(3)装置B的作用为除去HCl气体,则其中盛装的试剂的名称为
(4)装置F中盛装的试剂为NaOH溶液,则装置F中
 发生反应的离子方程式为
发生反应的离子方程式为(5)实验时,需持续通入干燥的空气,其体积大约是氯气的3倍,主要作用是
 的分解,保证实验安全。
的分解,保证实验安全。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
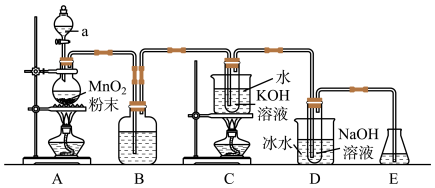
【推荐2】已知氯气与碱反应时,产物受温度的影响。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
(1)仪器a的名称是:___________ 。
(2)装置D的离子方程式为___________ 。
(3)装置B中的试剂为___________ 。
(4)根据题目已知信息,氯气通入到一定温度的KOH溶液中,溶液中含Cl元素的离子且满足比例关系正确的有___________ (填标号)。
A.含有Cl-和ClO ;且c(Cl-):c(ClO
;且c(Cl-):c(ClO )=1:5
)=1:5
B.含有Cl-、ClO 和ClO-;且c(Cl-):c(ClO
和ClO-;且c(Cl-):c(ClO ):c(ClO-)=(5b+c):b:c
):c(ClO-)=(5b+c):b:c
C.含有ClO 和ClO- ;且c(ClO
和ClO- ;且c(ClO ):c(ClO-)=1:5
):c(ClO-)=1:5
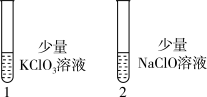
(5)探究KClO3、NaClO的氧化能力 。
。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色,1、2号试管均未检测到IO 。
。
结论:该条件下氧化能力KClO3___________ NaClO(填“大于”或“小于”)。
(1)仪器a的名称是:
(2)装置D的离子方程式为
(3)装置B中的试剂为
(4)根据题目已知信息,氯气通入到一定温度的KOH溶液中,溶液中含Cl元素的离子且满足比例关系正确的有
A.含有Cl-和ClO
 ;且c(Cl-):c(ClO
;且c(Cl-):c(ClO )=1:5
)=1:5 B.含有Cl-、ClO
 和ClO-;且c(Cl-):c(ClO
和ClO-;且c(Cl-):c(ClO ):c(ClO-)=(5b+c):b:c
):c(ClO-)=(5b+c):b:c C.含有ClO
 和ClO- ;且c(ClO
和ClO- ;且c(ClO ):c(ClO-)=1:5
):c(ClO-)=1:5(5)探究KClO3、NaClO的氧化能力
 。
。现象:1号试管溶液颜色不变,2号试管溶液变为棕色,1、2号试管均未检测到IO
 。
。结论:该条件下氧化能力KClO3
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
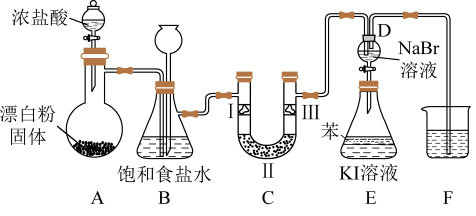
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是___________ ,请写出该反应相应的化学方程式___________ 。
(2)装置B中饱和食盐水的作用是___________ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:___________ 。
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是___________ ,该现象___________ (填“能”或“不能")说明溴单质的氧化性强于碘,原因是___________ 。
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为___________ 。

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是
(2)装置B中饱和食盐水的作用是
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是
(4)若向100mLFeBr2若液中通入2.24LCl2(标准状况下),若溶液中有
 的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
的Br-被氧化成单质Br2,则原FeBr2的物质的量浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】 常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含
常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含 ,还含少量
,还含少量 )以为原料制取
)以为原料制取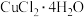 晶体的流程如下图所示:
晶体的流程如下图所示:
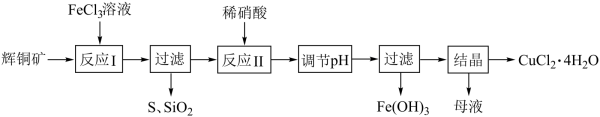
(1)反应Ⅰ中有 、
、 等物质生成。写出该反应的离子方程式:
等物质生成。写出该反应的离子方程式:_______ 。
(2) 是一种常见氧化剂和消毒剂。
是一种常见氧化剂和消毒剂。
①反应Ⅱ可以将稀硝酸换成稀盐酸和 的混合液。写出改为稀盐酸和
的混合液。写出改为稀盐酸和 的混合液后所发生反应的离子方程式:
的混合液后所发生反应的离子方程式:_______ 。
②反应Ⅱ还可以将稀硝酸换成 。与使用稀硝酸和
。与使用稀硝酸和 相比,使用稀盐酸和
相比,使用稀盐酸和 的混合液的优点是
的混合液的优点是_______ 。
(3)调节 的目的是将溶液中的
的目的是将溶液中的 转化为
转化为 沉淀。检验沉淀后的上层清液中是否含有
沉淀。检验沉淀后的上层清液中是否含有 的方法是
的方法是_______ 。
 常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含
常用作催化剂、杀虫剂等。一种辉铜矿(难溶于水,主要含 ,还含少量
,还含少量 )以为原料制取
)以为原料制取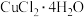 晶体的流程如下图所示:
晶体的流程如下图所示:
(1)反应Ⅰ中有
 、
、 等物质生成。写出该反应的离子方程式:
等物质生成。写出该反应的离子方程式:(2)
 是一种常见氧化剂和消毒剂。
是一种常见氧化剂和消毒剂。①反应Ⅱ可以将稀硝酸换成稀盐酸和
 的混合液。写出改为稀盐酸和
的混合液。写出改为稀盐酸和 的混合液后所发生反应的离子方程式:
的混合液后所发生反应的离子方程式:②反应Ⅱ还可以将稀硝酸换成
 。与使用稀硝酸和
。与使用稀硝酸和 相比,使用稀盐酸和
相比,使用稀盐酸和 的混合液的优点是
的混合液的优点是(3)调节
 的目的是将溶液中的
的目的是将溶液中的 转化为
转化为 沉淀。检验沉淀后的上层清液中是否含有
沉淀。检验沉淀后的上层清液中是否含有 的方法是
的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】按下面的实验过程完成下题:

(1)写出上述过程颜色变化(a)________ ;(b)______ ;(d)________ 。
(2)写出上述反应的化学方程式:(1)____________ ;(3)_________ 。

(1)写出上述过程颜色变化(a)
(2)写出上述反应的化学方程式:(1)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知A为常见的金属单质,根据如图所示的关系,请回答下列问题。
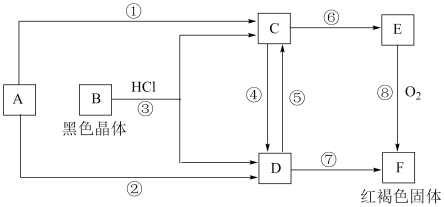
(1)写出下列物质的化学式A:___________ 、B:___________ 、D:___________ 、F:___________ 。
(2)写出反应③的离子方程式:___________ 。
(3)写出反应⑧的化学方程式:___________ 。
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:___________ 。
(5)检验D中金属阳离子操作方法是___________ 。

(1)写出下列物质的化学式A:
(2)写出反应③的离子方程式:
(3)写出反应⑧的化学方程式:
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:
(5)检验D中金属阳离子操作方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。某校研究性学习小组拟设计下列实验验证这一事实。
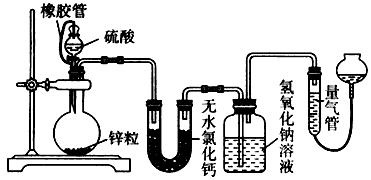
(1)该小组设计了如上图所示的实验装置,检查该装置气密性的操作是______________________ 。
(2)若1.30 g锌粒完全溶解,氢氧化钠洗气瓶增重0.64 g(烧瓶中残留气体忽略不计,下同),则圆底烧瓶中发生反应的化学方程式为________________________________ 。
(3)是否使用橡胶管,对实验结果___________ (填“有”或“无”)影响。

(1)该小组设计了如上图所示的实验装置,检查该装置气密性的操作是
(2)若1.30 g锌粒完全溶解,氢氧化钠洗气瓶增重0.64 g(烧瓶中残留气体忽略不计,下同),则圆底烧瓶中发生反应的化学方程式为
(3)是否使用橡胶管,对实验结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某校化学兴趣小组拟探究碳、硅元素的非金属性的相对强弱,实验装置如下:
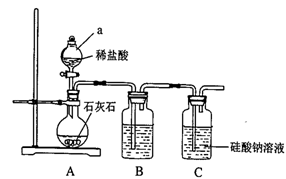
(1)连接好装置后,实验前必须进行的一步操作是_________ 。仪器a的名称为______ 。
(2)B装置中盛放的试剂是_________ ,C中发生反应的化学方程式为_________ 。
(3)该兴趣小组设计此实验通过_________ (填实验现象),可判断碳的非金属性强于硅的非金属性。
(4)该小组的一位同学认为,利用此实验装置及药品,也可以证明非金属性Cl>C>Si,你是否同意该同学的观点?_________ (填“同意”或“不同意”)。

(1)连接好装置后,实验前必须进行的一步操作是
(2)B装置中盛放的试剂是
(3)该兴趣小组设计此实验通过
(4)该小组的一位同学认为,利用此实验装置及药品,也可以证明非金属性Cl>C>Si,你是否同意该同学的观点?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
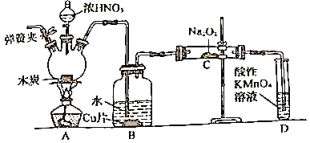
【推荐3】亚硝酸钠(NaNO2)在漂白、电镀等方面应用广泛。以木炭浓硝酸、水和铜为原料制备亚硝酸钠的装置如图所示:
已知:
室温下,①2NO+Na2O2===2NaNO2
②3NaNO2+3HCl===3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2ˉ都能与MnO4ˉ反应生成NO3ˉ和Mn2+
回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N2的作用是________________________________________ 。
(2)装置B中观察到的主要现象为________________________________________ ,发生反应离子方程式是_____________ 。
(3)装置D的作用是______________________________ ,发生反应的离子方程式是________________________________________ 。
(4)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和__________ (写化学式)。为避免产生这些副产物,应在装置B、C间增加干燥管,则干燥管中盛放的试剂为__________ (写名称)。
(5)利用改进后的装置将3.12gNa2O2完全转化为NaNO2,理论上至少需要木炭__________ g

已知:
室温下,①2NO+Na2O2===2NaNO2
②3NaNO2+3HCl===3NaCl+HNO3+2NO↑+H2O
③酸性条件下,NO或NO2ˉ都能与MnO4ˉ反应生成NO3ˉ和Mn2+
回答下列问题:
(1)检查完该装置的气密性,装入药品后,实验开始前通入一段时间N2,然后关闭弹簧夹,再滴加浓硝酸,加热。通入N2的作用是
(2)装置B中观察到的主要现象为
(3)装置D的作用是
(4)预测C中反应开始阶段,固体产物除NaNO2外,还含有的副产物有Na2CO3和
(5)利用改进后的装置将3.12gNa2O2完全转化为NaNO2,理论上至少需要木炭
您最近一年使用:0次



