已知A为常见的金属单质,根据如图所示的关系,请回答下列问题。
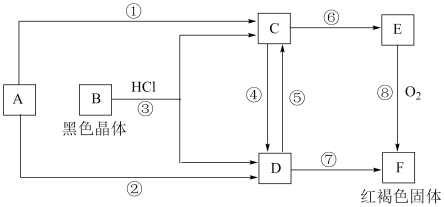
(1)写出下列物质的化学式A:___________ 、B:___________ 、D:___________ 、F:___________ 。
(2)写出反应③的离子方程式:___________ 。
(3)写出反应⑧的化学方程式:___________ 。
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:___________ 。
(5)检验D中金属阳离子操作方法是___________ 。

(1)写出下列物质的化学式A:
(2)写出反应③的离子方程式:
(3)写出反应⑧的化学方程式:
(4)若由D→C加入的为铁粉,写出反应⑤的离子方程式:
(5)检验D中金属阳离子操作方法是
更新时间:2023/07/17 22:04:15
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】室温下,单质A、单质B、单质C分别为固体、黄绿色气体、无色气体。在一定条件下,它们之间的转化关系如图所示,已知E溶液是无色的。请回答下列问题:
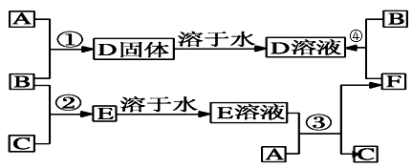
(1)反应①的化学方程式为___ 。
(2)反应③的化学方程式为____ 。
(3)反应④的化学方程式为___ 。

(1)反应①的化学方程式为
(2)反应③的化学方程式为
(3)反应④的化学方程式为
您最近一年使用:0次
【推荐2】I.字母 A~K 代表常见物质,在一定条件下能发生如图所示变化
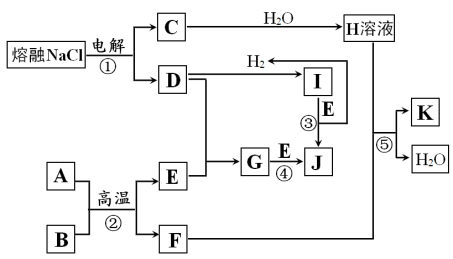
已知:反应②中A为红棕色粉末,B为金属单质,且n(A):n(B)=1:2,反应③和反应④均在水溶液中进行。
(1)保存 J 的方法是:_____ 。
(2)写出反应②的化学方程式:_____ 。
II.某研究性学习小组的同学以 Fe(NO3)3溶液来探究 Fe3+能否氧化 Ag 为题。他们选用少量的Fe(NO3)3溶液与做过银镜反应的试管进行实验。现象:银镜部分溶解,试管上方出现少量淡淡的红棕色气体。
(1)出现少量淡淡的红棕色气体,该气体是_____ 。
(2)若 Fe3+能否氧化 Ag,只需证明:_____ 方法是:_____
Ⅲ. 铁红是一种红色颜料,其成分是 Fe2O3,将一定量的铁红溶于 180mL 5mol·L-1盐酸中,在加入一定量铁粉恰好溶解,收集到 3.36L(标准状况)气体。
(1)按反应顺序写出离子方程式_____
(2)反应后的溶液中一定没有 Fe3+,理由是_____
(3)参加反应的铁粉的质量为_____ g。

已知:反应②中A为红棕色粉末,B为金属单质,且n(A):n(B)=1:2,反应③和反应④均在水溶液中进行。
(1)保存 J 的方法是:
(2)写出反应②的化学方程式:
II.某研究性学习小组的同学以 Fe(NO3)3溶液来探究 Fe3+能否氧化 Ag 为题。他们选用少量的Fe(NO3)3溶液与做过银镜反应的试管进行实验。现象:银镜部分溶解,试管上方出现少量淡淡的红棕色气体。
(1)出现少量淡淡的红棕色气体,该气体是
(2)若 Fe3+能否氧化 Ag,只需证明:
Ⅲ. 铁红是一种红色颜料,其成分是 Fe2O3,将一定量的铁红溶于 180mL 5mol·L-1盐酸中,在加入一定量铁粉恰好溶解,收集到 3.36L(标准状况)气体。
(1)按反应顺序写出离子方程式
(2)反应后的溶液中一定没有 Fe3+,理由是
(3)参加反应的铁粉的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】中学常见单质A、B和甲、乙、丙三种化合物有如图所示的转换关系(部分产物未列出),单质A常作为食品包装材料,甲是两性氧化物。
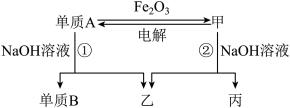
根据图示转化关系回答:
(1)写出单质A与Fe2O3反应的化学方程式__________________________________
(2)写出电解甲制单质A的化学方程式__________________________________
(3)实验室完成单质A与Fe2O3反应实验,需要的试剂还有_______ 。
a.KCl b.KClO 3 c.MnO2 d.Mg
(4)利用单质A与Fe2O3反应的原理,工业上可用于___________

根据图示转化关系回答:
(1)写出单质A与Fe2O3反应的化学方程式
(2)写出电解甲制单质A的化学方程式
(3)实验室完成单质A与Fe2O3反应实验,需要的试剂还有
a.KCl b.KClO 3 c.MnO2 d.Mg
(4)利用单质A与Fe2O3反应的原理,工业上可用于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.化合物X由四种元素组成,X具有光学活性,见光分解生成A和B。A中含有两种酸根相同的盐,F是工业部门不可缺少的一种金属,可用作营养增补剂。E溶于水形成强碱,焰色反应是紫色,取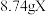 按如下流程进行实验(气体体积已转化为标准状况下的体积)
按如下流程进行实验(气体体积已转化为标准状况下的体积)
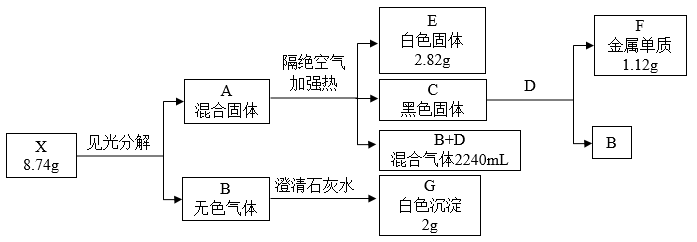
(1)组成X的四种元素是________ ,X的化学式是________ 。
(2)X见光分解的化学方程式是_______ 。
(3)气体D与金属F在高温下能反应生成一种配合物,其中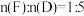 ,该反应的化学方程式是
,该反应的化学方程式是______________ 。
Ⅱ.某兴趣小组为制取纯净的硫酸铜进行实验,如图,实验中观察到的现象:蒸馏烧瓶中产生红棕色气体,烧杯中可观察到红棕色气体消失。
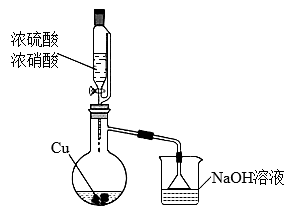
(4)用浓硫酸和浓硝酸的混合溶液制备硫酸铜的原因是________ (请写出两点)。
(5)已知烧杯中NaOH与NO2反应产生NaNO2,请设计方案检验 的存在:
的存在:________
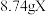 按如下流程进行实验(气体体积已转化为标准状况下的体积)
按如下流程进行实验(气体体积已转化为标准状况下的体积)
(1)组成X的四种元素是
(2)X见光分解的化学方程式是
(3)气体D与金属F在高温下能反应生成一种配合物,其中
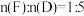 ,该反应的化学方程式是
,该反应的化学方程式是Ⅱ.某兴趣小组为制取纯净的硫酸铜进行实验,如图,实验中观察到的现象:蒸馏烧瓶中产生红棕色气体,烧杯中可观察到红棕色气体消失。

(4)用浓硫酸和浓硝酸的混合溶液制备硫酸铜的原因是
(5)已知烧杯中NaOH与NO2反应产生NaNO2,请设计方案检验
 的存在:
的存在:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某铁的氧化物粉末可能含有FeO、 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
(已知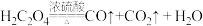 )
)

(1)装置甲的作用是______________________________ 。
(2)装置丁中的实验现象是______________________________________ 。
(3)若丙中铁的氧化物的化学式为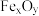 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为________ 。若丙中铁的氧化物质量为 3. 92 g,且完全反应,丁中生成沉淀的质量为13. 79 g,试确定该氧化物中x:y=_________ 。
(4)实验评价:该装置存在缺点__________ ,改进的方法________ 。
 中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
中的一种或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:(已知
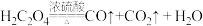 )
)
(1)装置甲的作用是
(2)装置丁中的实验现象是
(3)若丙中铁的氧化物的化学式为
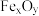 ,则丙中反应的化学方程式为
,则丙中反应的化学方程式为(4)实验评价:该装置存在缺点
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。
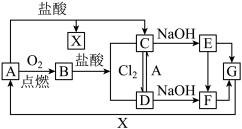
(1)写出A、C、F、G的化学式:A_______ ,C_______ ,F_______ ,G_______ 。
(2)写出B与盐酸反应的离子方程式_______
(3)检验D中阳离子的方法_______ 。
(4)制取F胶体的方法_______ 。
(5)①写出下列转化的离子方程式C→D:_______ ,
②由E转化为F的现象是_______ 。
③并写出的化学方程式E→F:_______

(1)写出A、C、F、G的化学式:A
(2)写出B与盐酸反应的离子方程式
(3)检验D中阳离子的方法
(4)制取F胶体的方法
(5)①写出下列转化的离子方程式C→D:
②由E转化为F的现象是
③并写出的化学方程式E→F:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】以下物质相互转化
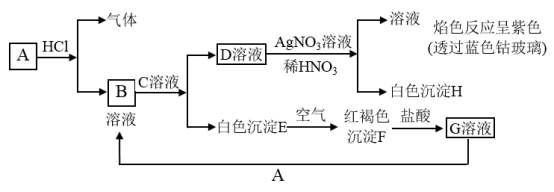
试回答:
(1)写出B的化学式__________ ;D的名称_________ 。
(2)写出由E转变成F的化学方程式____ 。
(3)写出用KOH鉴别G溶液的离子方程式____ ;向G溶液加入A的有关离子方程式___________ 。

试回答:
(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)写出用KOH鉴别G溶液的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种物质(或离子)均含有同一种元素,其中A是常见单质,它们之间存在如图所示的转化关系:

(1)若B、C均属于盐类,B溶液呈黄色,遇氨水能形成红褐色沉淀;D是一种不溶性碱;B、C中的阴离子均是 ,则A只有与
,则A只有与________ (填分子式)反应才能得到B;实验室制备的D物质不稳定,相应反应的化学方程式为__________________ 。
(2)若B具有强氧化性, 时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为____________ ,实验室可用D制备少量的C,反应的化学方程式为__________

(1)若B、C均属于盐类,B溶液呈黄色,遇氨水能形成红褐色沉淀;D是一种不溶性碱;B、C中的阴离子均是
 ,则A只有与
,则A只有与(2)若B具有强氧化性,
 时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某溶液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为
中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验:
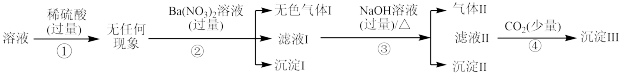
回答下列问题:
(1)通过过程①判断溶液中一定不存在___________ (填离子符号)。
(2)气体Ⅰ为___________ (填化学式,下同),沉淀Ⅰ为___________ 。
(3)过程③中生成气体的离子方程式为___________ 。
(4)下列说法正确的是___________ (填标号)。
a.滤液Ⅰ中一定含有 、
、 ,滤液Ⅰ中一定含有
,滤液Ⅰ中一定含有 、
、
b.将沉淀Ⅲ加入足量的稀盐酸中,无气泡产生
c.沉淀Ⅱ可溶于强酸,也可溶于强碱
(5)实验结束后,该同学得出结论,该溶液中一定含有___________ (填离子符号,下同),判断的理由是___________ ,该溶液中一定没有___________ 。
(6)根据(5)的结论,取少量该溶液于烧杯中,加入足量的烧碱溶液,观察到溶液中的现象是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为
中的若干种离子(忽略和水的反应以及水的电离),离子浓度均为 。某同学进行了如下实验:
。某同学进行了如下实验: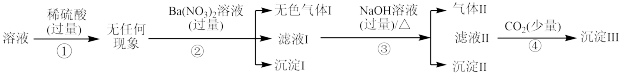
回答下列问题:
(1)通过过程①判断溶液中一定不存在
(2)气体Ⅰ为
(3)过程③中生成气体的离子方程式为
(4)下列说法正确的是
a.滤液Ⅰ中一定含有
 、
、 ,滤液Ⅰ中一定含有
,滤液Ⅰ中一定含有 、
、
b.将沉淀Ⅲ加入足量的稀盐酸中,无气泡产生
c.沉淀Ⅱ可溶于强酸,也可溶于强碱
(5)实验结束后,该同学得出结论,该溶液中一定含有
(6)根据(5)的结论,取少量该溶液于烧杯中,加入足量的烧碱溶液,观察到溶液中的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】铁及其化合物在生产、生活中有重要用途。某化学兴趣小组的同学设计了以下实验探究铁及其化合物的性质。
Ⅰ.下图为探究“铁与水反应”的实验装置(夹持装置已略去):___________ 。
(2)装置B中发生反应的化学方程式为___________ 。
(3)装置E中发生反应的化学方程式为___________ 。
Ⅱ.模拟用溶液腐蚀镀铜电路板并从废液中回收 和溶液,流程如下图所示:
和溶液,流程如下图所示: 溶液与镀铜电路板上的铜反应的离子方程式
溶液与镀铜电路板上的铜反应的离子方程式___________ 。
(5)试剂X为___________ 、试剂Y为___________ (填化学式)。
(6)加入Z时发生反应的离子方程式为___________ 。
(7)检验滤液中是否含有 的实验操作及现象为
的实验操作及现象为___________ 。
Ⅰ.下图为探究“铁与水反应”的实验装置(夹持装置已略去):
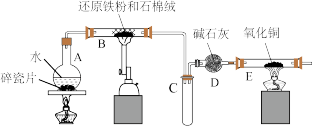
(2)装置B中发生反应的化学方程式为
(3)装置E中发生反应的化学方程式为
Ⅱ.模拟用溶液腐蚀镀铜电路板并从废液中回收
 和溶液,流程如下图所示:
和溶液,流程如下图所示: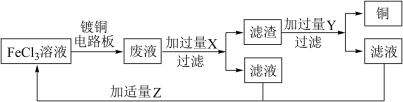
 溶液与镀铜电路板上的铜反应的离子方程式
溶液与镀铜电路板上的铜反应的离子方程式(5)试剂X为
(6)加入Z时发生反应的离子方程式为
(7)检验滤液中是否含有
 的实验操作及现象为
的实验操作及现象为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
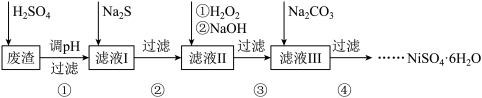
【推荐2】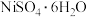 是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电泡等。可由电镀废渣(除镍元素外,还含有Cu、Zn、Fe、Cr等元素杂质)为原料获得。工艺流程如下:
是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电泡等。可由电镀废渣(除镍元素外,还含有Cu、Zn、Fe、Cr等元素杂质)为原料获得。工艺流程如下:
已知:①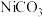 是一种不溶于水易溶于强酸的沉淀
是一种不溶于水易溶于强酸的沉淀
②已知 ,
, 的
的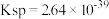
(1)Ni的原子序数为28,则它在周期表中的位置为______ ,写出H2O2的结构式______ 。
(2)步骤①,用稀硫酸溶解废渣时,为了提高浸取率可采取的措施有______ (任写一点)。
(3)步骤②,向滤液I中加入适量 溶液的目的是除去Cu2+和
溶液的目的是除去Cu2+和 ,其中除去Cu2+的离子方程式为
,其中除去Cu2+的离子方程式为______ ;加 之前需控制pH不能太低的目的是
之前需控制pH不能太低的目的是______ 。
(4)步骤③的目的是除去Fe和Cr,温度不能太高的原因是__ 。若在 时,调
时,调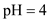 除去铁,此时溶液中
除去铁,此时溶液中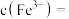
__ 。
(5)滤液Ⅲ中溶质的主要成分是______ ,检验滤液Ⅲ中是否还有铁元素的试剂是______ 。
(6)粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度镍,下列叙述正确的是__ (已知:氧化性Fe2+<Ni2+<Cu2+)
A.粗镍作阳极,纯镍作阴极
B.阳极发生还原反应,其电极反应式: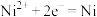
C.电解过程中,阳极质量的减少与阴极质量的增加相等
D.电解后,溶液中存在的金属阳离子只有Cu2+和
E.电解后,电解槽底部的阳极泥中只有Cu和Pt
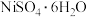 是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电泡等。可由电镀废渣(除镍元素外,还含有Cu、Zn、Fe、Cr等元素杂质)为原料获得。工艺流程如下:
是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电泡等。可由电镀废渣(除镍元素外,还含有Cu、Zn、Fe、Cr等元素杂质)为原料获得。工艺流程如下:
已知:①
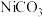 是一种不溶于水易溶于强酸的沉淀
是一种不溶于水易溶于强酸的沉淀②已知
 ,
, 的
的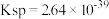
(1)Ni的原子序数为28,则它在周期表中的位置为
(2)步骤①,用稀硫酸溶解废渣时,为了提高浸取率可采取的措施有
(3)步骤②,向滤液I中加入适量
 溶液的目的是除去Cu2+和
溶液的目的是除去Cu2+和 ,其中除去Cu2+的离子方程式为
,其中除去Cu2+的离子方程式为 之前需控制pH不能太低的目的是
之前需控制pH不能太低的目的是(4)步骤③的目的是除去Fe和Cr,温度不能太高的原因是
 时,调
时,调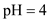 除去铁,此时溶液中
除去铁,此时溶液中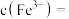
(5)滤液Ⅲ中溶质的主要成分是
(6)粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度镍,下列叙述正确的是
A.粗镍作阳极,纯镍作阴极
B.阳极发生还原反应,其电极反应式:
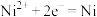
C.电解过程中,阳极质量的减少与阴极质量的增加相等
D.电解后,溶液中存在的金属阳离子只有Cu2+和

E.电解后,电解槽底部的阳极泥中只有Cu和Pt
您最近一年使用:0次
【推荐3】某校研究性学习小组在进行铁与水蒸气反应所得固体物质的成分、性质及再利用的实验探究,请回答下列问题。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。___________ 。
(2)证明铁与水蒸气反应有 生成的实验现象:
生成的实验现象:___________ 。
(3)待硬质玻璃管B冷却后,取其中少许固体于试管中,加入足量稀硫酸待其充分溶解后,再滴加KSCN溶液,溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:___________ 。
探究二:按照如图实验流程用硬质玻璃管B中固体制备 纳米材料。
纳米材料。
(4)已知:浊液B中铁元素以FeOOH形式存在,生成浊液B的离子方程式:___________ 。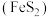 煅烧反应为:
煅烧反应为: 。消耗120 g
。消耗120 g  ,转移的电子数为
,转移的电子数为___________ 。
(6)在滤液A转化为浊液B反应完成后需再加热一段时间除去剩余 ,目的是
,目的是___________ 。
探究一:设计如图所示装置进行“铁与水蒸气反应”的实验(夹持仪器略)。
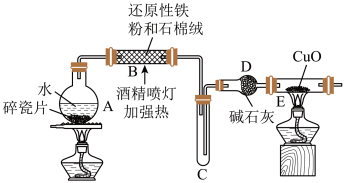
(2)证明铁与水蒸气反应有
 生成的实验现象:
生成的实验现象:(3)待硬质玻璃管B冷却后,取其中少许固体于试管中,加入足量稀硫酸待其充分溶解后,再滴加KSCN溶液,溶液未变红色,请从硬质玻璃管B中固体物质的成分分析可能的原因:
探究二:按照如图实验流程用硬质玻璃管B中固体制备
 纳米材料。
纳米材料。(4)已知:浊液B中铁元素以FeOOH形式存在,生成浊液B的离子方程式:
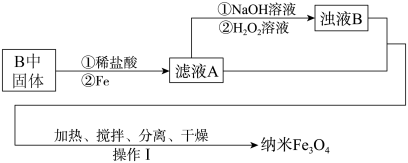
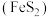 煅烧反应为:
煅烧反应为: 。消耗120 g
。消耗120 g  ,转移的电子数为
,转移的电子数为(6)在滤液A转化为浊液B反应完成后需再加热一段时间除去剩余
 ,目的是
,目的是
您最近一年使用:0次



