已知A是一种红棕色金属氧化物,B、D是金属单质,C是两性金属氧化物,J是一种难溶于水的白色化合物,受热后容易发生分解。
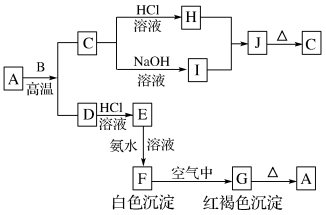
(1)写出下列物质的化学式:A______ 、C______ 。
(2)按要求写方程式:
①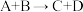 的化学方程式:
的化学方程式:________ ;
② 的化学方程式:
的化学方程式:________ ;
③ 的离子方程式:
的离子方程式:_______ ;
④B与 溶液反应的离子方程式:
溶液反应的离子方程式:_________ 。.
(3)同温同压下,相同质量的金属B和D分别与足量的盐酸反应,所生成的气体体积比为_______ 。

(1)写出下列物质的化学式:A
(2)按要求写方程式:
①
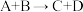 的化学方程式:
的化学方程式:②
 的化学方程式:
的化学方程式:③
 的离子方程式:
的离子方程式:④B与
 溶液反应的离子方程式:
溶液反应的离子方程式:(3)同温同压下,相同质量的金属B和D分别与足量的盐酸反应,所生成的气体体积比为
更新时间:2022-08-17 13:14:32
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知反应①、②、③中都涉及到MnO2,反应关系如图所示,其中E、M、H为中学化学常见的气体单质,E为黄绿色,M、H均为无色。G有漂白性,N的焰色反应为紫色(透过蓝色钻玻璃观察)。
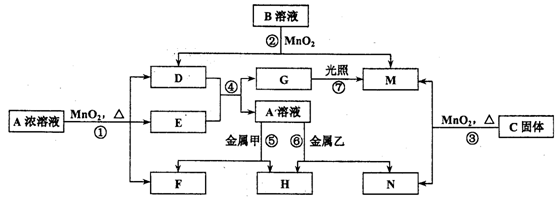
请回答:
(l)在反应①、②中,MnO2的作用分别是_________ 、________ 。
(2)在图中反应①~⑦中,属于氧化还原反应的是______ (填序号)
a.除④外 b. 除①⑤⑥外 c.除④⑦外 d.全部
(3)请写出下列反应的离子方程式:
反应①______________ ;反应④______________ ;反应⑥______________ ;
(4)若amolE气体、b molM气体、cmolH气体,在一定条件下恰好完全反应,得到A溶液,则a、b、c的关系为___________ 。(用含有a、b、c的代数式表示)

请回答:
(l)在反应①、②中,MnO2的作用分别是
(2)在图中反应①~⑦中,属于氧化还原反应的是
a.除④外 b. 除①⑤⑥外 c.除④⑦外 d.全部
(3)请写出下列反应的离子方程式:
反应①
(4)若amolE气体、b molM气体、cmolH气体,在一定条件下恰好完全反应,得到A溶液,则a、b、c的关系为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图表示某些常见物质之间的转化关系(反应条件已略去),其中A、D为气态非金属单质,B、C为金属单质,B为红色,E、F、G、H为化合物,G为无色液体,甲、乙、丙、丁、戊为溶液,丙为强酸的稀溶液。①、②均为工业冶炼B的反应。

请回答下列问题:
(1)F由同族两种元素组成,可用于食物增白,也是大气污染物之一,污染来源主要是 ,它在大气中可形成丙,反应的化学方程式为 。反应④也可以生成丙,反应的离子方程式为 ;
(2)由反应①制得的金属B含杂质,工业上用 方法将B提纯至99.95%以上。利用热还原制得的金属C,也含杂质,在潮湿的中性环境中,C较易发生腐蚀,化学方程式为 ,C经反应③的处理,表面生成黑色晶体H后,可减缓蚀;
(3)检验溶液丁中金属离子的方法是 ;
(4)E可由单质直接化合得到,则E的化学式为 ,反应①的化学方程式为 。

请回答下列问题:
(1)F由同族两种元素组成,可用于食物增白,也是大气污染物之一,污染来源主要是 ,它在大气中可形成丙,反应的化学方程式为 。反应④也可以生成丙,反应的离子方程式为 ;
(2)由反应①制得的金属B含杂质,工业上用 方法将B提纯至99.95%以上。利用热还原制得的金属C,也含杂质,在潮湿的中性环境中,C较易发生腐蚀,化学方程式为 ,C经反应③的处理,表面生成黑色晶体H后,可减缓蚀;
(3)检验溶液丁中金属离子的方法是 ;
(4)E可由单质直接化合得到,则E的化学式为 ,反应①的化学方程式为 。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有常见金属A、B,它们之间存在如下的转化关系(图中有些反应的产物和反应的条件没有全部标出),其中G、H为白色沉淀。请回答下列问题:

(1)写出金属A和物质D的名称或化学式:__________ 、__________ 。
(2)写出E转化为G的离子方程式______________________________________ ;
(3)写出H放在空气中的现象:________________________________________ 。

(1)写出金属A和物质D的名称或化学式:
(2)写出E转化为G的离子方程式
(3)写出H放在空气中的现象:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某课外兴趣小组为探究某种合金(含Mg、Al)中铝的含量,设计如图装置进行实验。

(1)如何检查该装置的气密性?___________________ 。
(2)写出该合金与氢氧化钠溶液反应的离子方程式:_________________ 。
(3)使足量氢氧化钠溶液与a g合金(固体M)充分反应,进入量气管的气体体积为V mL(已换算成标准状况,下同)。若a=0.036,V=22.4,该合金中铝的质量分数是_______ 。
(4)若将装置中的氢氧化钠溶液替换为足量的盐酸,与a g合金粉末充分反应,则进入量气管内的气体体积_______ (填“>”、“<”或“=”)V mL;利用测得的气体体积能否对合金中的Al含量进行计算?_______ (填“能”或“否”)。

(1)如何检查该装置的气密性?
(2)写出该合金与氢氧化钠溶液反应的离子方程式:
(3)使足量氢氧化钠溶液与a g合金(固体M)充分反应,进入量气管的气体体积为V mL(已换算成标准状况,下同)。若a=0.036,V=22.4,该合金中铝的质量分数是
(4)若将装置中的氢氧化钠溶液替换为足量的盐酸,与a g合金粉末充分反应,则进入量气管内的气体体积
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A_____________ 、B___________ 、C______________ 、F_____________ 、 H____________ 、乙______________
(2)写出下列反应化学方程式:
反应①_________________________________________________
反应⑤_________________________________________________
反应⑥_________________________________________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应化学方程式:
反应①
反应⑤
反应⑥
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】由短周期元素组成的三种单质A、B、C和甲、乙、丙、丁四种化合物有下图所示转化关系,甲是典型的两性氧化物,也是工业上制取A的主要原料。

请回答:
(1)写出下列物质的化学式:单质C__________ ,化合物甲___________ 。
(2)写出A与NaOH溶液反应生成乙和C的化学方程式____________ 。
(3)写出丁与氨水反应的离子方程式_____________ 。
(4)写出上述反应中既属于氧化还原反应,又属于化合反应的反应方程式,并表示出电子转移的方向和数目_____________ 。

请回答:
(1)写出下列物质的化学式:单质C
(2)写出A与NaOH溶液反应生成乙和C的化学方程式
(3)写出丁与氨水反应的离子方程式
(4)写出上述反应中既属于氧化还原反应,又属于化合反应的反应方程式,并表示出电子转移的方向和数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下图是无机物A到M在一定条件下的转化关系(部分产物及反应条件未列出)。其中, I 是由第三周期元素组成的单质中,熔点最高的金属。K是一种红棕色气体。

请回答下列问题
(1)M、F、E、G 四种物质中所含同一种元素,其名称是_____________ 。
(2)写出反应⑩(溶液 J + G)的离子反应方程式__________________________________ 。
(3)反应④中被还原的离子和被氧化的离子的物质的量之比是___________ 。
(4)向M的溶液中直接滴加 NaOH 溶液,现象是______________________ ,写出相应的化学方程式_____________________________ ,_______________________________ 。
(5)将化合物 D 与 KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂 K2FeO4(高铁酸钾),同时还生成 KNO2和 H2O 。该反应的的化学方程式是___________________________ 。
(6)共有120 t 硫铁矿(FeS2)参与反应①冶炼化合物D,最终得到化合物D共16 t,则冶炼D的转化率为_____ 。

请回答下列问题
(1)M、F、E、G 四种物质中所含同一种元素,其名称是
(2)写出反应⑩(溶液 J + G)的离子反应方程式
(3)反应④中被还原的离子和被氧化的离子的物质的量之比是
(4)向M的溶液中直接滴加 NaOH 溶液,现象是
(5)将化合物 D 与 KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂 K2FeO4(高铁酸钾),同时还生成 KNO2和 H2O 。该反应的的化学方程式是
(6)共有120 t 硫铁矿(FeS2)参与反应①冶炼化合物D,最终得到化合物D共16 t,则冶炼D的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】铝是重要的金属,有诸多用途.回答下列问题:
(1)利用铝与氧化铁可以焊接钢轨,写出发生反应的化学方程式__________ 。
(2)如图1为金属铝与1L盐酸反应生成氢气的物质的量与反应时间的关系。
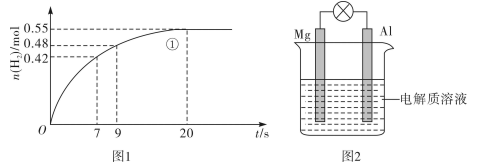
①0~20s范围内用盐酸浓度的变化表示该反应的平均速率为___________ (假定反应前后溶液体积不变);
②从图可以看出,0~7s反应速率最大,其原因是____________________ 。
(3)以Al、Mg为电极,可以组装一种原电池装置(如图2所示)。
①若电解质溶液为稀硫酸时,则Mg电极上发生的电极反应式为____________ ,当外电路有0.3mol电子转移时,Al电极上生成__________ L(标准状况)H2;
②若电解质溶液为NaOH溶液,则外电路中的电子_________ (填“流出”或“流入”)Al电极。
(1)利用铝与氧化铁可以焊接钢轨,写出发生反应的化学方程式
(2)如图1为金属铝与1L盐酸反应生成氢气的物质的量与反应时间的关系。

①0~20s范围内用盐酸浓度的变化表示该反应的平均速率为
②从图可以看出,0~7s反应速率最大,其原因是
(3)以Al、Mg为电极,可以组装一种原电池装置(如图2所示)。
①若电解质溶液为稀硫酸时,则Mg电极上发生的电极反应式为
②若电解质溶液为NaOH溶液,则外电路中的电子
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。请回答下列问题:
Ⅰ.(1)引发铝热反应的实验操作是_____________________
(2)做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是_________________
(3)反应的化学方程式为_____________
Ⅱ.已知:Al、Fe的熔、沸点数据如下:
(1)某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?____________ (填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:_____________________
Ⅰ.(1)引发铝热反应的实验操作是
(2)做铝热反应时,内层纸漏斗底部剪一小孔用水润湿的目的是
(3)反应的化学方程式为
Ⅱ.已知:Al、Fe的熔、沸点数据如下:
| 物质 | Al | Fe |
| 熔点(℃) | 660 | 1 535 |
| 沸点(℃) | 2 467 | 2 750 |
您最近一年使用:0次



