16. 某班同学用如下实验探究Fe
2+、Fe
3+的性质。回答下列问题:
(1)分别取一定量硫酸铁、硫酸亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeSO
4溶液时需加入少量铁屑,其目的是
__。
(2)甲组同学取2mLFeSO
4溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl
2可将Fe
2+氧化。FeSO
4溶液与氯水反应的离子方程式为
___。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeSO
4溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
__。
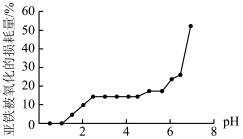
(4)丙组同学研究pH对FeSO
4稳定性的影响,得到如图所示结果,增强Fe
2+稳定性的措施为
__。(写出一条即可)
(5)丁组同学为了探究Fe
2(SO
4)
3与Cu的反应,做了如图所示实验:
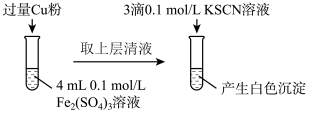
①Fe
3+与Cu反应的离子方程式为
__。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I
-相似;
ii.2Cu
2++4I
-=2CuI↓+I
2。
填写实验方案:
| 实验方案 | 现象 |
| 步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。 | 无明显现象 |
| 步骤2:取4mL_mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。 | 产生白色沉淀 |
Cu
2+与SCN
-反应的离子方程式为
__。