根据信息回答下列问题:
Ⅰ.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
已知:两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
(1)通过分析电负性的变化规律,确定 元素电负性的最小范围
元素电负性的最小范围_______ 。
(2)判断下列物质是离子化合物还是共价化合物:
A. B.
B. C.
C. D.SiC
D.SiC
①属于共价化合物的是_______ (填字母)。
② 易与水反应生成生成一种刺激性气味的气体,写出反应的化学方程式
易与水反应生成生成一种刺激性气味的气体,写出反应的化学方程式_______ 。
(3) 溶液在实验室里可以用来制备
溶液在实验室里可以用来制备 ,写出制备
,写出制备 的离子方程式
的离子方程式_______ 。
Ⅱ.元素原子的第一电离能 随原子序数呈周期性变化,请回答:
随原子序数呈周期性变化,请回答:
(4) 的第一电离能小于
的第一电离能小于 ,从原子结构的角度解释其原因
,从原子结构的角度解释其原因_______ 。
(5)与 同一周期,第一电离能最大的元素是
同一周期,第一电离能最大的元素是_______ (写名称)。
Ⅰ.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
| 元素 |  |  |  | C |  |  |  | N |  | O | H |
| 电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
(1)通过分析电负性的变化规律,确定
 元素电负性的最小范围
元素电负性的最小范围(2)判断下列物质是离子化合物还是共价化合物:
A.
 B.
B. C.
C. D.SiC
D.SiC①属于共价化合物的是
②
 易与水反应生成生成一种刺激性气味的气体,写出反应的化学方程式
易与水反应生成生成一种刺激性气味的气体,写出反应的化学方程式(3)
 溶液在实验室里可以用来制备
溶液在实验室里可以用来制备 ,写出制备
,写出制备 的离子方程式
的离子方程式Ⅱ.元素原子的第一电离能
 随原子序数呈周期性变化,请回答:
随原子序数呈周期性变化,请回答:(4)
 的第一电离能小于
的第一电离能小于 ,从原子结构的角度解释其原因
,从原子结构的角度解释其原因(5)与
 同一周期,第一电离能最大的元素是
同一周期,第一电离能最大的元素是
更新时间:2022-09-07 14:05:29
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】已知X、Y、Z、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X是空气中含量最高的元素,Z 基态原子核外K、L、M三层电子数之比为1:4:2,R基态原子的 3d 原子轨道上的电子数是 4s 原子轨道上的4 倍,Y基态原子的最外层电子数等于Z、R基态原子的最外层电子数之和。(答题时:X、Y、Z、R 用所对应的元素符号表示)
(1)X、Y、Z 的第一电离能由小到大的顺序为_______ ,写出一种与ZY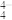 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_______ 。
(2)元素R 在周期表中的位置为_______ , R3+ 基态核外电子排布式为_______ 。
(3)化合物 Z3X4熔点高达 1900℃以上,硬度很大。该物质的晶体类型是_______ 。

(4)Y、Z 形成的某晶体的晶胞结构如图所示,则该化合物的化学式为_______ 。
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的做目为_______ 。
(1)X、Y、Z 的第一电离能由小到大的顺序为
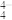 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(2)元素R 在周期表中的位置为
(3)化合物 Z3X4熔点高达 1900℃以上,硬度很大。该物质的晶体类型是

(4)Y、Z 形成的某晶体的晶胞结构如图所示,则该化合物的化学式为
(5)R2+与过量的氨水形成的配离子的化学式为[R(NH3)6]2+,1mol[R(NH3)6]2+中含有σ键的做目为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中基态A原子的电子分布在3个能级,且每个能级所含的电子数相同;C的原子核外最外层有 6 个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物的水化物酸性最强;基态F原子核外最外层只有一个电子,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)元素 A、 B、 C 的第一电离能由小到大的是__________________ (用元素符号表示)。
(2)E的最高价含氧酸中 E 原子的杂化方式为_____________ 。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为_________________ 。
(3)F原子的外围电子排布式为_______________________ ,
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为__________ 。
(5)通常情况下,D单质的熔沸点比G单质高,原因是_________________________ 。
(6)已知 DE 晶体的晶胞如图所示:
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏伽德罗常数),则该晶胞中含有_________ 个 A 原子,该晶体的密度是_______ g·cm-3(列式表示)。
(1)元素 A、 B、 C 的第一电离能由小到大的是
(2)E的最高价含氧酸中 E 原子的杂化方式为
(3)F原子的外围电子排布式为
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为
(5)通常情况下,D单质的熔沸点比G单质高,原因是
(6)已知 DE 晶体的晶胞如图所示:
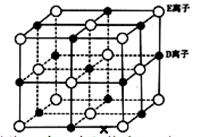
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏伽德罗常数),则该晶胞中含有
您最近一年使用:0次
【推荐3】铁、钴、镍等单质及化合物的应用广泛。
(1)LiFePO4是锂离子电池材料,画出Fe2+的价层电子排布图____________ ,其中PO43-的立体构型是____________ 。
(2)化合物“钴酞菁”能显著提升二次电池的充放电效率,下图是改性“氨基钴酞菁”分子的结构图。
①写出氨基钴酞菁中N原子的杂化轨道类型____________ ;
②写出一种与氨基阴离子NH2-互为等电子体的中性分子____________ ;
③将“钴酞菁”改性为“氨基钴酞菁”后,能使其水溶性得到有效改善,请简述其原因:____________
(3)1mol[Co(NO2)6]3-中所含的σ键数目是____________ 。K3[Co(NO2)6]中四种元素的第一电离能由大到小的顺序是____________ 。
(4)如图所示为NiO晶体的晶胞结构示意图:
①该晶胞中占有阴阳离子总数是____________ ;
②已知在NiO晶体中Ni2+的半径为a pm,O2-的半径为bpm,它们在晶体中是紧密接触的,则在NiO晶体中原子的空间利用率为____________ 。(用含字母a、b的计算式表达)
(1)LiFePO4是锂离子电池材料,画出Fe2+的价层电子排布图
(2)化合物“钴酞菁”能显著提升二次电池的充放电效率,下图是改性“氨基钴酞菁”分子的结构图。
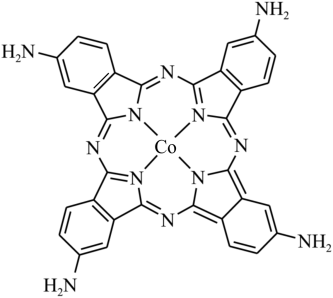
①写出氨基钴酞菁中N原子的杂化轨道类型
②写出一种与氨基阴离子NH2-互为等电子体的中性分子
③将“钴酞菁”改性为“氨基钴酞菁”后,能使其水溶性得到有效改善,请简述其原因:
(3)1mol[Co(NO2)6]3-中所含的σ键数目是
(4)如图所示为NiO晶体的晶胞结构示意图:
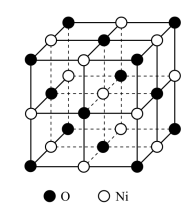
①该晶胞中占有阴阳离子总数是
②已知在NiO晶体中Ni2+的半径为a pm,O2-的半径为bpm,它们在晶体中是紧密接触的,则在NiO晶体中原子的空间利用率为
您最近一年使用:0次
【推荐1】金属钛被誉为“二十一世纪金属”,具有广泛的应用前景。回答下列问题:
(1)Ti原子最高能层电子的电子云轮廓图的形状为___________ 。与Ti同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为___________ 。
(2)已知电离能: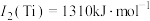 ,
,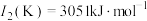 ,
,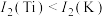 ,原因
,原因___________ 。
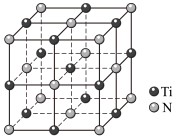
(3)已知TiN晶体的晶胞结构如图所示,则该晶体结构中与N原子距离最近且相等的Ti原子有___________ 个;若该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞中Ti原子与N原子的最近距离为
,晶胞中Ti原子与N原子的最近距离为___________ pm(用含 、
、 的代数式表示)。
的代数式表示)。
(4)由金红石( )制取单质Ti的步骤为:
)制取单质Ti的步骤为: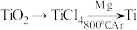
已知:Ⅰ.
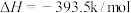
Ⅱ.

Ⅲ.
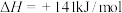
①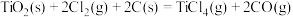 的
的
___________ 。在某温度下,反应①的恒容体系已经达到平衡,若向其中加入少量炭, 的体积分数将
的体积分数将___________ ;若加入少量氯气, 的体积分数将
的体积分数将___________ 。
A.减少 B.不变 C.增大
②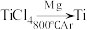 过程中,在Ar气氛中进行的理由是
过程中,在Ar气氛中进行的理由是___________ 。
(1)Ti原子最高能层电子的电子云轮廓图的形状为
(2)已知电离能:
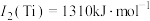 ,
,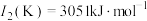 ,
,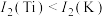 ,原因
,原因(3)已知TiN晶体的晶胞结构如图所示,则该晶体结构中与N原子距离最近且相等的Ti原子有
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞中Ti原子与N原子的最近距离为
,晶胞中Ti原子与N原子的最近距离为 、
、 的代数式表示)。
的代数式表示)。
(4)由金红石(
 )制取单质Ti的步骤为:
)制取单质Ti的步骤为: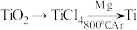
已知:Ⅰ.

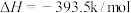
Ⅱ.


Ⅲ.

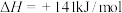
①
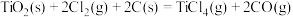 的
的
 的体积分数将
的体积分数将 的体积分数将
的体积分数将A.减少 B.不变 C.增大
②
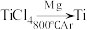 过程中,在Ar气氛中进行的理由是
过程中,在Ar气氛中进行的理由是
您最近一年使用:0次
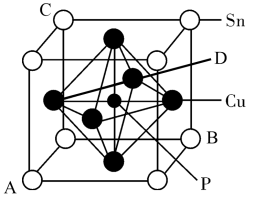
【推荐2】环烷酸金属(Cu、Ni、Co、Sn、Zn)盐常作为合成聚氨酯过程中有效催化剂,回答下列问题:
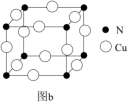
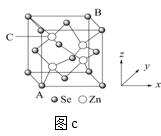
(1)基态Cu原子的价电子排布____ ,金属Cu晶体采取的是____ 堆积方式。如图a所示,(●代表Cu原子,○代表O原子),一个Cu2O晶胞中Cu原子的数目为___ 。N和Cu形成的化合物的晶胞结构如图b所示,该化合物的相对分子质量为M,NA为阿伏加德罗常数。若该晶胞的边长为apm,则该晶体的密度是____ g•cm-3。硒化锌晶胞结构如图c所示,其晶胞参数为apm。已知原子坐标:A点为(0,0,0),B点为(1,1,1),则C点的原子坐标____ 。

(2)镍的氨合离子[Ni(NH3)6]2+中存在的化学键有____ 。
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(3)写出Cu2+的外围电子排布式____ ;比较铁与锰的第三电离能(I3):铁____ 锰(填“>”、“=”或“<”),原因是____ 。
(1)基态Cu原子的价电子排布



(2)镍的氨合离子[Ni(NH3)6]2+中存在的化学键有
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(3)写出Cu2+的外围电子排布式
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志看我国航天技术向前迈出了一大步,其制造材料中包含了Cu、Ti、Cr、Ni、Si、N、O等多种元素。回答下列问题:
(1)基态铬原子的价电子排布式为___________ ,基态钛原子的核外电子有___________ 种空间运动状态。
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性、疏水性、生理惰性和较小的表面张力,可用于飞船零件保护,其结构如图所示。硅油中碳原子的杂化方式为___________ 杂化,C、Si、O的第一电离能由小到大的顺序是___________ 。O—Si键的键能比C—Si键的键能___________ (填“大”或“小”)。
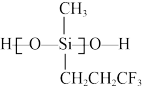
(3)Cu催化烯烃硝化反应过程中会产生 。键角:
。键角:
___________ (填“<”或“>”) ,其原因是
,其原因是___________ 。
(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。 可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
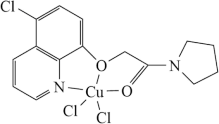
①溶液中的水存在 、
、 等微粒形式,
等微粒形式, 可看作是
可看作是 与
与 通过氢键形成的离子,写出
通过氢键形成的离子,写出 的结构式:
的结构式:___________ 。
②1 mol该配合物中通过鳌合作用形成的配位键有___________ mol。
(5)磷青铜晶体的晶胞结构如图所示。原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0)、B为(1,1,0)、C为(0,1,1),则D原子的分数坐标为___________ 。晶体中P原子位于由Cu原子形成的___________ 空隙中,该晶体中两个距离最近的Cu原子的核间距为a nm,则晶体密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态铬原子的价电子排布式为
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性、疏水性、生理惰性和较小的表面张力,可用于飞船零件保护,其结构如图所示。硅油中碳原子的杂化方式为

(3)Cu催化烯烃硝化反应过程中会产生
 。键角:
。键角:
 ,其原因是
,其原因是(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。
 可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
①溶液中的水存在
 、
、 等微粒形式,
等微粒形式, 可看作是
可看作是 与
与 通过氢键形成的离子,写出
通过氢键形成的离子,写出 的结构式:
的结构式:②1 mol该配合物中通过鳌合作用形成的配位键有
(5)磷青铜晶体的晶胞结构如图所示。原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0)、B为(1,1,0)、C为(0,1,1),则D原子的分数坐标为
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】钛是一种银白色过渡金属,在高科技社会中得到了广泛的应用。可以从钛铁矿( )中提取
)中提取 ,并常用Na置换熔融
,并常用Na置换熔融 来获得单质Ti。
来获得单质Ti。
(1)基态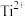 的价电子排布式为
的价电子排布式为___________ ,其核外能量最高的电子所在的能层符号为___________ ,其核外共有___________ 种运动状态不同的电子。
(2)Ti的配合物有多种。在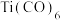 、
、 和
和 三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是
三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是___________ (填写元素名称), 中
中
___________ (填“大于”、“小于”或“等于”)单个水分子中 ,原因是
,原因是___________ 。
(3) 的球棍结构如图,Ti的配位数是
的球棍结构如图,Ti的配位数是___________ ,N原子的杂化方式为___________ ,与 互为等电子体的分子为
互为等电子体的分子为___________ (写分子式)。 和
和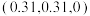 ,则微粒3的原子分数坐标为
,则微粒3的原子分数坐标为___________ ;若阿伏加德罗常数的值为 ,金红石的密度为
,金红石的密度为___________  (列出计算表达式)。
(列出计算表达式)。
 )中提取
)中提取 ,并常用Na置换熔融
,并常用Na置换熔融 来获得单质Ti。
来获得单质Ti。(1)基态
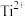 的价电子排布式为
的价电子排布式为(2)Ti的配合物有多种。在
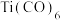 、
、 和
和 三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是
三种微粒的配体中,所含原子电负性由大到小排序后,排第3位的元素是 中
中
 ,原因是
,原因是(3)
 的球棍结构如图,Ti的配位数是
的球棍结构如图,Ti的配位数是 互为等电子体的分子为
互为等电子体的分子为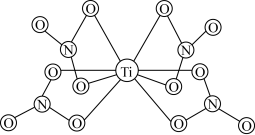
 和
和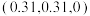 ,则微粒3的原子分数坐标为
,则微粒3的原子分数坐标为 ,金红石的密度为
,金红石的密度为 (列出计算表达式)。
(列出计算表达式)。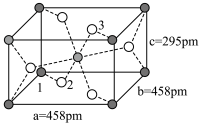
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】【选修3:物质结构与性质】
工业上用合成气(CO和H2)制取乙醇的反应为2CO+4H2 CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
(1)Ti基态原子核外电子排布式为_______ 。和O同一周期且元素的第一电离能比O大的有_____ (填元素符号),和O同一周期且基态原子核外未成对电子数比O多的有____ (填元素符号)。
(2)在用合成气制取乙醇反应所涉及的4种物质中,沸点从低到高的顺序为______________ 。
(3)工业上以CO、O2、NH3为原料,可合成氮肥尿素[CO(NH2)2],CO(NH2)2分子中含有的σ键与π键的数目之比为_________ 。
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。
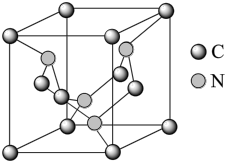
①该晶体的化学式为______ ;其硬度超过金刚石的原因是___________ 。
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加 德罗常数,则该晶胞的空间利用率为__________________ (用含d、r1、r2、NA的代数式表示)。
工业上用合成气(CO和H2)制取乙醇的反应为2CO+4H2
 CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:
CH3CH2OH+H2O。研究发现,使用TiO2作为载体负载铑基催化剂具有较高的乙醇产量。回答下列问题:(1)Ti基态原子核外电子排布式为
(2)在用合成气制取乙醇反应所涉及的4种物质中,沸点从低到高的顺序为
(3)工业上以CO、O2、NH3为原料,可合成氮肥尿素[CO(NH2)2],CO(NH2)2分子中含有的σ键与π键的数目之比为
(4)C元素与N元素形成的某种晶体的晶胞如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),该晶体硬度超过金刚石,成为首屈一指的超硬新材料。

①该晶体的化学式为
②已知该晶胞的密度为d g/cm3,N原子的半径为r1cm,C原子的半径为r2cm,设NA为阿伏加 德罗常数,则该晶胞的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】12月 17日凌晨,嫦娥五号完成“ 挖土” 之旅返回地球。查阅资料,月球玄武岩是构成月球的岩石之一,主要由辉石(主要成分硅酸盐)和钛铁矿(主要成分 FeTiO3)等组成。回答下列问题:
(1)基态铁原子的价电子排布式为:______ 。
(2)与 Fe同周期,且最外层电子数相同的主族元素是______ (填元素符号)。
(3)基态 Ti原子核外电子占据的最高能层符号为______ ;其最外层电子的电子云轮廓图为______ 。
(4)1molFe3[Fe(CN)6]2中含有 σ键数为______ ,[Fe(CN)6]3-中配体为______ ,其中 C原子的杂化轨道类型为______ ,H、C、N、Si四种元素的电负性由大到小的顺序为______ 。
(5)FeTiO3的结构如图 1所示,其中由 O围成的______ (填“ 四面体空隙” 或“ 八面体空隙” )被 Fe占据。在图 2中画出 FeTiO3结构的另一种表示______ (要求:Fe处于晶胞的顶点),Ti的配位数为______ 。
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=______ pm。(列出计算表达式)
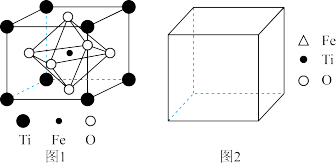
(1)基态铁原子的价电子排布式为:
(2)与 Fe同周期,且最外层电子数相同的主族元素是
(3)基态 Ti原子核外电子占据的最高能层符号为
(4)1molFe3[Fe(CN)6]2中含有 σ键数为
(5)FeTiO3的结构如图 1所示,其中由 O围成的
(6)已知该晶胞的密度为 ρg/cm3,NA表示阿伏加德罗常数的值。计算晶胞参数 a=

您最近一年使用:0次



